Dofetilde:新しいクラスIII抗不整脈
Volume III,Number4|September/October2000
Jodie Zalewski,Pharm.D.
薬物療法更新インデックスに戻る
はじめに
ドフェチリド(Tikosyn®)は、正常洞への変換および維持に使用される新しいクラスIII抗不整脈薬である。高度に症候性心房細動/フラッターを有する患者におけるリズム。 それは伝導システムに対する効果無しで選択的なカリウムチャネルの封鎖を、表わすこと他のクラスIIIのantiarrhythmicsと異なっています。 ドフェチリドは、心房および心室の再分極の両方を延長し、したがって、心筋内の不応期を増加させる。 他のクラスIII抗不整脈剤は、追加の抗不整脈特性を有する。 ソタロール(a β遮断薬)とアミオダロンはA v結節伝導を減少させる。 従って、アミオダロンの器官の毒性とつながれて(例えば。 肺線維症、甲状腺および肝機能障害)、これらの薬剤は、すべての患者に適していません。 Dofetilideの選択的なメカニズムはクラスの他の代理店よりよいようです;但し、dofetilideはまだ悪影響が注意して原因で使用されなければなりません。
副作用
ドフェチリドはカリウムチャネルに作用し、活動電位を広げるため、qt間隔の延長が起こり、これはtorsades de pointesに関連する。 QT間隔の延長は、ドフェチリドの用量および血漿濃度に直接関連する。 薬物相互作用または腎機能の低下により、濃度が上昇することがあります。 従って、dofetilideは非常に徴候の患者のだけ使用のために予約されます。
FDAはdofetilide、ファイザーの製造業者に、適切な使用を保証し、投薬を訂正するために厳密な指針を課すように義務付けました。 刺激は薬剤誘発のtorsades de pointesのための潜在性の高められた意識でした(市場からのastemizole、terfenadineおよびcisaprideの取り外しによって示される)。 ドフェチリド療法を開始するためには、患者は心臓モニタリングのために少なくとも72時間認定病院に入院しなければならない。 病院が認定施設になる前に、ファイザーの教育プログラムの完了をスタッフが確認するフォームが会社に提出されている必要があります。
患者評価
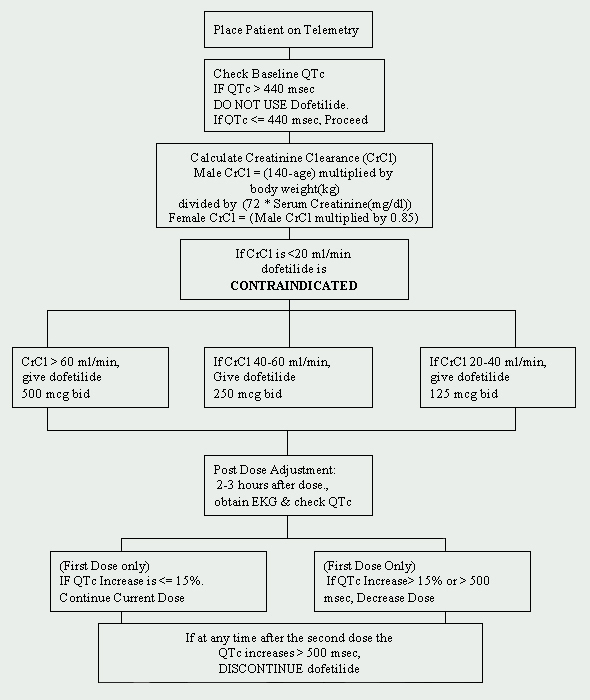
クリーブランドクリニック財団では、ドフェチリドは心臓病科に制限されています。 Dofetilideの開始のための議定書は実行され、製造業者の課された規則に従ってあります(図1を見て下さい)。 Dofetilideで始まるべき患者は心電図の(EKG)の監視のための公認の遠隔測定工学の単位に是認されなければならない。 このようなモニタリングは、QT延長の存在を決定するために必要である。 ベースラインQTc(修正されたQT間隔:QTc=QTMsec/rr secの平方根)測定が必要であり、qtcが440msec(心室伝導異常の患者では500Msec)を超える場合、ドフェチリドは禁忌である。
もう一つの重要なベースライン評価は腎機能です。 Dofetilideがrenally除去されるので、悪い腎臓機能は(クレアチニンの整理によって測定される)dofetilideの蓄積をもたらし、従って、不整脈のための危険を高めることがで ドフェチリドの初期用量は、クレアチニンクリアランスによって決定される(表1参照)。 正常な腎機能を有する患者(CrCl>60ml/分)は、1日2回経口投与された500mcgで開始される。 ドフェチリドは、クレアチニンクリアランスが<20ml/分の患者には禁忌である。表1
: Initial Dofetilide Dose
| Calculated CrCl (ml/min) | Dofetilide Dose |
|---|---|
| >60 | 500 mcg twice daily |
| 40-60 | 250 mcg twice daily |
| 20-39 | 125 mcg twice daily |
| <20 | 125 mcg twice daily |
ベースラインベーシックメタボリックパネル(BMP)も取得する必要があります。 低カリウム血症および低マグネシウム血症は、患者を不整脈の影響を受けやすくする可能性があるため、ドフェチリドを開始する前に電解質異常を 血清カリウム(K+)が<4mEq/Lおよび/または血清マグネシウム(Mg++)が<2mEq/Lの場合、ドフェチリドを投与する前に欠乏症を補充し、再
薬物相互作用は、ドフェチリド療法を開始する前に対処する必要があります。 Verapamil(Calan(登録商標)、Calan SR(登録商標)、Covera-HS(登録商標)、Isoptin(登録商標)、Isoptin SR(登録商標)、Verelan(登録商標)、Verelan PM(登録商標))、シメチジン(Tagamet(登録商標))、トリメトプリム(Proloprim(登録商標)、Trimpex(登録商標)、またはbactrim(登録商標)、Septra(登録商標))、ケトコナゾール(Nizoral(登録商標))、プロクロロペラジン(Compazine(登録商標))およびメゲストロール(Megace(登録商標))とドフェチリドとの併用は禁忌である。 これらの薬剤はドフェチリドのレベルの増加をもたらす腎臓の輸送システムの禁止によってドフェチリドの除去を遅らせます。 さらに、阻害しないが、この経路を介して分泌される薬物は注意して使用すべきである(例えば、、トリアムテレン、メトホルミン、アミロリド)。 避けるべきである他の薬剤はqt間隔を、phenothiazines、cisapride、bepridil、三環系抗鬱剤、エリスロマイシンおよびクラスI(例えば、quinidine、procainamide、lidocaine、flecainide)およびクラスIIIのantiarrhythmic代理店のような延長する 最後に、利尿薬などの低カリウム血症または低マグネシウム血症を引き起こす薬剤も注意して使用する必要があります。
投薬、投与およびモニタリング
患者にすべての禁忌がない場合、ドフェチリドを開始することができる。 Qtc間隔を評価するために、最初の投与の2〜3時間後にEKGを繰り返し実施する。 QTc間隔が>15%増加した場合、またはQTcが>500msec(心室伝導異常を有する患者では550msec)である場合、ドフェチリドの用量 一般に、用量は半分になる(表2参照)。 72時間の開始期間の残りのために、EKGの監視はドフェチリドの各々のそれに続く線量の後の二から三時間に行われます。 QTc間隔に基づいて追加の用量の削減は推奨されません。 2回目の投与後にQTcが>500msec(心室伝導異常患者では550Msec)になった場合は、ドフェチリドを中止する必要があります。 遠隔測定法による連続的な心臓監視は、通常の洞調律への電気的または薬理学的変換後の最低72時間、または12時間のいずれか大きい方の間継続される。表2
: QT延長調整テーブル
| CrClに基づく開始用量 | 調整用量(QT延長のための) |
|---|---|
| 500Mcg毎日二回 | 250mcg毎日二回 |
| 250mcg毎日二回 | 125mcg毎日二回 |
| 125mcg一日二回 | 125mcg一日一回 |
ファイザーは、fdaと組み合わせて、撮影しています dofetilideの適切な使用を保証するもう一つのステップ。 米国で唯一の薬局(通信販売)、ペンシルベニア州のStatlanders薬局は、dofetilideを分配します。 治療の中断を防ぐために、患者の退院前に薬局サービス登録フォームに記入し、Statlandersにファックスする必要があります。 退院時に、患者は薬物の一週間の供給を受ける。 この供給は、彼らの通信販売の処方箋が配信されるまで、患者に十分な薬を与えます。
結論
ドフェチリドは症候性心房細動/フラッターに対する有効な抗不整脈薬であるが、注意して開始する必要がある。 患者の安全を確保するためには、FDAが義務付けているガイドラインを厳格に遵守する必要があります。