dofetilde: A New Class III Antiarytmic
Volume III, Number 4 | September/October 2000
Jodie Zalewski, Pharm.D.
Return to Pharmacotherapy Update Index
Introduction
dofetilidi (Tikosyn®) on uusi luokka III rytmihäiriölääke, jota käytetään normaalin sinusrytmin muuttamiseen ja ylläpitämiseen potilailla, joilla on erittäin oireinen eteisvärinä/ – lepatus. Se eroaa muista luokan III rytmihäiriölääkkeistä siinä, että sillä on selektiivinen kaliumkanavan salpaus, jolla ei ole vaikutusta johtumisjärjestelmään. Dofetilidi pidentää sekä eteisen että kammion repolarisaatiota ja lisää siten tulenkestävää aikaa sydänlihaksessa. Muilla luokan III rytmihäiriölääkkeillä on muita rytmihäiriölääkkeitä. Sotaloli (ß-salpaaja) ja amiodaroni vähentävät av-solmukohtien johtumista. Tästä syystä yhdessä amiodaronin elintoksisuuden kanssa (esim. keuhkofibroosia, kilpirauhasen ja maksan toimintahäiriöitä), nämä lääkeaineet eivät sovellu kaikille potilaille. Dofetilidin selektiivinen mekanismi näyttää olevan parempi kuin muiden saman luokan lääkeaineiden; dofetilidin käytössä on kuitenkin noudatettava varovaisuutta sen haittavaikutusten vuoksi.
haittavaikutukset
koska dofetilidi vaikuttaa kaliumkanavaan ja laajentaa aktiopotentiaalia, QT-aika pitenee, mikä liittyy kääntyvien kärkien takykardiaan. QT-ajan piteneminen riippuu suoraan dofetilidin annoksesta ja pitoisuudesta plasmassa. Pitoisuus voi kohota lääkkeiden yhteisvaikutusten tai huonon munuaistoiminnan vuoksi. Siksi dofetilidi on varattu vain erittäin oireisille potilaille.
FDA on antanut dofetilidin valmistajalle, Pfizerille, tehtäväksi antaa tiukat ohjeet asianmukaisen käytön ja oikean annostelun varmistamiseksi. Sysäyksenä oli lisääntynyt tietoisuus lääkkeiden aiheuttaman kääntyvien kärkien takykardian mahdollisuudesta (osoituksena astemitsolin, terfenadiinin ja sisapridin poistaminen markkinoilta). Jotta dofetilidihoito voidaan aloittaa, potilaan on oltava hyväksytyssä sairaalassa vähintään 72 tuntia sydämen seurantaa varten. Ennen kuin sairaala on sertifioitu laitos, lomake, jolla varmistetaan Pfizerin koulutusohjelman loppuun saattaminen henkilöstön jäsenillä, on oltava yrityksen tiedostossa.
potilaan arviointi
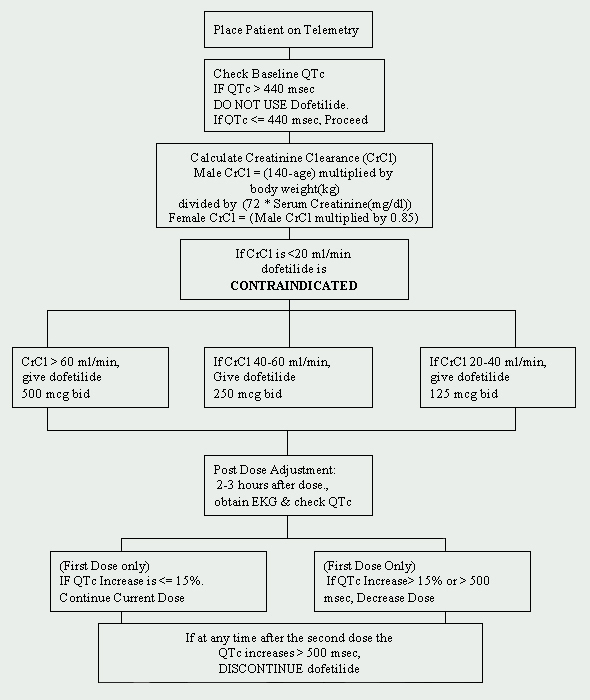
Cleveland Clinic Foundationin dofetilidi rajoittuu kardiologian osastoon. Dofetilidin aloittamista koskeva protokolla on pantu täytäntöön, ja se on valmistajan asettamien määräysten mukainen (KS.Kuva 1). Dofetilidihoidon aloittavat potilaat on otettava hyväksyttyyn telemetriayksikköön EKG-seurantaa varten. Tällainen seuranta on tarpeen QT-ajan pitenemisen määrittämiseksi. Lähtötason QTc (korjattu QT-aika: QTc = QTMsec / RR sec: n neliöjuuri ) mittaukset on tehtävä, ja jos QTc on yli 440Msec (500 MS potilailla, joilla on kammiojohtumishäiriöitä), dofetilidi on vasta-aiheinen.
toinen tärkeä lähtötilanteen arviointi on munuaisten toiminta. Koska dofetilidi eliminoituu munuaisten kautta, huono munuaisten toiminta (kreatiniinipuhdistumalla mitattuna ) voi johtaa dofetilidin kertymiseen ja siten lisätä rytmihäiriöiden riskiä. Dofetilidin aloitusannos määräytyy kreatiniinipuhdistuman mukaan (ks.Taulukko 1). Potilaat, joiden munuaistoiminta on normaali (CrCl > 60 ml/min) aloitetaan annoksella 500 mikrog suun kautta kahdesti vuorokaudessa. Dofetilidi on vasta-aiheinen potilailla, joiden kreatiniinipuhdistuma on < 20 ml/min.
Taulukko 1: Initial Dofetilide Dose
| Calculated CrCl (ml/min) | Dofetilide Dose |
|---|---|
| >60 | 500 mcg twice daily |
| 40-60 | 250 mcg twice daily |
| 20-39 | 125 mcg twice daily |
| <20 | 125 mcg twice daily |
on myös otettava perusaineenvaihduntapaneeli (BMP). Elektrolyyttihäiriöt on korjattava ennen dofetilidin aloittamista, koska hypokalemia ja hypomagnesemia voivat altistaa potilaat rytmihäiriöille. Jos seerumin kalium (K+) on < 4 mEq/L ja/tai seerumin magnesium (Mg++) on < 2 mEq/L, puutteet on korjattava ja tarkistettava uudelleen ennen dofetilidin antamista.
lääkkeiden yhteisvaikutukset on myös selvitettävä ennen dofetilidihoidon aloittamista. Verapamiilin (Calan®, Calan sr®, Cover-HS®, Isoptin®, Isoptin SR®, Verelan®, Verelan PM®), simetidiinin (Tagamet®), trimetopriimin (Proloprim®, Trimpex® tai Yhdistelmätuotteissa Bactrim®, Septra®), ketokonatsolin (Nizoral®), proklooriperatsiinin (Compazine®) ja megestrolin (Megace®) samanaikainen käyttö dofetilidin kanssa on vasta-aiheista. Nämä aineet hidastavat dofetilidin eliminaatiota estämällä munuaiskuljetusjärjestelmää, mikä johtaa dofetilidipitoisuuden nousuun. Lisäksi lääkkeitä, jotka eivät inhiboi, mutta joita erittyy muuten tämän reitin kautta, tulee käyttää varoen (esim., triamtereeni, metformiini, amiloridi). Muita vältettäviä aineita ovat QT-aikaa pidentävät aineet, kuten fentiatsiinit, sisapridi, bepridiili, trisykliset masennuslääkkeet, erytromysiini ja luokan I lääkkeet (esim.kinidiini, prokaiiniamidi, lidokaiini, flekainidi) ja luokan III rytmihäiriölääkkeet. Lopuksi, aineita, jotka aiheuttavat hypokalemiaa tai hypomagnesemiaa, kuten diureetteja, tulee myös käyttää varoen.
annostus, anto ja seuranta
Jos potilaalta puuttuvat kaikki vasta-aiheet, dofetilidihoito voidaan aloittaa. EKG toistetaan 2-3 tunnin kuluttua ensimmäisestä annoksesta QTc-ajan arvioimiseksi. Jos QTc-aika on pidentynyt > 15% tai jos QTc on > 500Msec (550msec potilailla, joilla on kammiojohtumishäiriöitä), dofetilidin annosta on pienennettävä. Yleensä annos puolitetaan (KS.Taulukko 2). Loput 72 tuntia kestäneestä aloitusjaksosta EKG-seuranta suoritetaan kahden-kolmen tunnin kuluttua jokaisesta seuraavasta dofetilidiannoksesta. Annoksen pienentämistä ei suositella QTc-ajan perusteella. Jos QTc muuttuu milloin tahansa toisen annoksen jälkeen > 500Msec (550 MS potilailla, joilla on kammiojohtumishäiriöitä), dofetilidihoito tulee lopettaa. Sydämen jatkuvaa telemetriaseurantaa jatketaan vähintään 72 tunnin ajan tai 12 tunnin ajan sen jälkeen, kun sähköinen tai farmakologinen sinusrytmi on vaihdettu normaaliin sinusrytmiin, sen mukaan kumpi on suurempi.
Taulukko 2: QT-ajan pitenemisen Säätötaulukko
| aloitusannos perustuu CrCl: ään | mukautettu annos (QT-ajan pitenemiseen) |
|---|---|
| 500 mikrogrammaa kahdesti päivässä | 250 mikrogrammaa kahdesti päivässä |
| 250 mikrogrammaa kahdesti päivässä | 125 mikrogrammaa kahdesti päivittäin |
| 125 mikrog kahdesti päivässä | 125 mikrog kerran päivässä |
Pfizer on yhdessä FDA: n kanssa ottanut toinen askel dofetilidin asianmukaisen käytön varmistamiseksi. Vain yksi apteekki (postimyynti) Yhdysvalloissa, Statlandersin Apteekki Pennsylvaniassa, annostelee dofetilidiä. Apteekkipalvelujen ilmoittautumislomake on täytettävä ja faksattava Statlandersille ennen potilaan kotiuttamista hoidon häiriöiden estämiseksi. Kotiutuksen jälkeen potilaat saavat yhden viikon lääkeannoksen. Tämä tarjonta antaa potilaalle tarpeeksi lääkitystä, kunnes postimyyntiresepti on toimitettu.
johtopäätös
vaikka dofetilidi on tehokas rytmihäiriölääke oireiseen eteisvärinään / flutteriin, sen antamisessa on noudatettava varovaisuutta. FDA: n määräämien ohjeiden tiukka noudattaminen on tarpeen potilasturvallisuuden varmistamiseksi.