é um composto químico inorgânico que existe naturalmente como um mineral raro. Pode dissolver-se igualmente em uma solução de ácido forte ou base e é chamado de composto anfotérico. Em condições aquosas, o composto dissocia-se em iões de zinco e hidróxido.
Zinco, hidróxido de Identificação
número CAS: 20427-58-1
PubChem: 9812759
ChemSpider: 7988510
Zinco, hidróxido de Fórmula
a Sua fórmula química é Zn (OH)2.
propriedades do hidróxido de zinco
as seguintes propriedades são algumas das propriedades únicas do composto:
aparência
geralmente aparece como um sólido branco.
massa Molar
pesa cerca de 99.424 g / mol.
estabilidade
é estável e não reativo em condições normais.
densidade
sua massa por volume é de cerca de 3.053 g / cm3.
Ponto de fusão
decompõe-se a 125 Graus Celsius.solubilidade solubilidade
é moderadamente solúvel em água e absolutamente insolúvel em álcool. O seu produto de solubilidade (Ksp) é de 3.0 x 10-17.
dissolução
hidróxido de zinco dissolve-se em amoníaco aquoso para formar um complexo de aminas incolor e solúvel em água. Quando o amoníaco é adicionado em excesso, os íons de hidróxido que se dissociam do Zn(OH)2 reage com ele para formar um complexo tetra positivamente carregado com um número de coordenação de 4. O produto resultante é rodeado por ligando amoníaco, o que resulta em dissolução.
hidróxido de zinco Termoquímica
sua entalpia padrão de formação ou calor padrão de formação é -642 kJ.mol-1.
estrutura do hidróxido de zinco
Aqui está a estrutura do composto anfotérico.
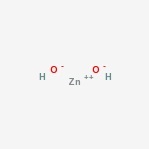
ocorrência de hidróxido de zinco
ocorre como três minerais de terras raras: Vulfingite, ashoverite e ruteeta. Estes minerais raros são na verdade os polimorfos naturais de Zn (OH)2. Na ciência da matéria, qualquer material sólido é polimórfico se existir em mais de uma forma, como ortorrômbico ou tetragonal.é geralmente preparado adicionando uma quantidade moderada de solução de hidróxido de sódio a uma solução de sal de zinco como cloreto de zinco ou sulfato de zinco. Estes dois compostos reagem em condições normais para formar um precipitado branco de Zn (OH)2. A solução diluída de hidróxido de sódio deve ser utilizada nesta reacção para evitar a dissolução do composto inorgânico. Em condições normais, o sal de zinco dissocia-se para formar um íon de zinco que se associa com dois íons hidróxido da solução de hidróxido de sódio para formar hidróxido de zinco.
Zn2++ 2OH- → Zn(OH)2
Se o excesso de hidróxido de sódio é adicionado à solução de sal, o precipitado de Zn (OH)2 que é formado, inicialmente, irá dissolver-se para formar um formulário de uma solução incolor de zincate de iões, como visto abaixo:
Zn (OH)2 + 2OH– → Zn(OH)42-
Esta propriedade de hidróxido de zinco é amplamente usado para detectar a presença de iões de zinco em solução. No entanto, não é um método único para testar como existem muitos compostos de alumínio e chumbo que se comportam de uma maneira muito semelhante.
a propriedade dissolvente do hidróxido de zinco pode ser contribuído para a presença de ligantes de água que normalmente cercam o íon. Quando o excesso de hidróxido de sódio é adicionado à solução, os dois íons de hidróxido reduzem-no a um complexo carregado negativamente, tornando-o assim solúvel.algumas das utilizações comuns de Zn (OH)2 são: pensos cirúrgicos, pensos cirúrgicos, pensos cirúrgicos, pensos cirúrgicos, etc. Ligaduras grandes que são usados pós-cirurgia são revestidos com o composto de zinco para absorver o sangue da ferida.o aço e o ferro são mais frequentemente aplicados com um revestimento de zinco através de um processo chamado galvanização. Sob condições úmidas, uma camada de hidróxido de zinco Forma sobre estes metais galvanizados, a fim de evitar que eles sejam enferrujados.o hidróxido de zinco é muito gelatinoso (semelhante a gelatina) e funciona geralmente como mordente que tinge vários tecidos ou tecidos. Corante é geralmente um reagente químico, que forma um complexo metálico com Zn(OH)2 e fortemente ligado aos revestimentos de tecido.
pesticidas
It is often used as an intermediate for commercial production of pesticides and pigments.

soluções tópicas
combinação de Zn (OH)2 com óxido de zinco é amplamente utilizado em cremes calamínicos, pomadas, pó para bebé, loções cutâneas e cosméticos. Reage com bases fortes, devido à sua natureza anfotérica, formando zincados que são utilizados como drogas orais para tratar vários distúrbios.
baterias elétricas
também é usado em baterias elétricas de alta energia que são recarregáveis através de uma reação reversível.
composição de Borracha
Zn (OH)2 é utilizado na composição ou mistura de diferentes ingredientes de borracha para otimizar as propriedades de uso final, de acordo com o consumidor precisa.compostos de zinco, como óxido de zinco, sulfato de zinco e nitrato de zinco, são produzidos comercialmente com a ajuda do produto químico inorgânico.é geralmente não inflamável e não apresenta riscos para os trabalhadores. Contudo, o composto não deve ser provado nem engolido, pois pode conter poucos ingredientes toxicológicos.