se on epäorgaaninen kemiallinen yhdiste, joka esiintyy luonnostaan harvinaisena mineraalina. Se voi liueta yhtä lailla vahvan hapon tai emäksen liuokseen ja sitä kutsutaan amfoteeriseksi yhdisteeksi. Yhdiste hajoaa vesiolosuhteissa sinkki-ja hydroksidi-ioneiksi.
Sinkkihydroksidin tunnistus
CAS-numero: 20427-58-1
PubChem: 9812759
ChemSpider: 7988510
Sinkkihydroksidin kaava
sen kemiallinen kaava on Zn (OH)2.
Sinkkihydroksidin ominaisuudet
seuraavat ovat joitakin yhdisteen ainutlaatuisia ominaisuuksia:
ulkonäkö
se esiintyy yleensä valkoisena kiinteänä aineena.
moolimassa
se painaa noin 99,424 g / mol.
Stabiilisuus
se on stabiili ja ei-reaktiivinen normaaliolosuhteissa.
tiheys
sen massa tilavuutta kohti on noin 3, 053 g / cm3.
sulamispiste
se hajoaa 125 celsiusasteessa.
Liukoisuus
se liukenee niukasti veteen ja täysin liukenematon alkoholiin. Sen liukoisuustuote (Ksp) on 3,0 x 10-17.
liukeneminen
Sinkkihydroksidi liukenee ammoniakin vesiliuokseen muodostaen värittömän, vesiliukoisen ammiinikompleksin. Kun ammoniakkia lisätään liikaa, Zn: stä(OH)2 irtoavat hydroksidi-ionit reagoivat sen kanssa muodostaen positiivisesti varautuneen tetrakompleksin, jonka koordinaatioluku on 4. Tuloksena olevaa tuotetta ympäröi ammoniakkiligandi, joka johtaa liukenemiseen.
Sinkkihydroksidin Termokemia
sen muodostumisindalpia tai standardilämpö on -642 kJ.mol-1.
Sinkkihydroksidin rakenne
tässä on amfoteerisen yhdisteen rakenne.
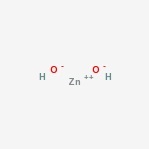
Sinkkihydroksidin esiintyminen
se esiintyy kolmena harvinaisena maametallina: Wulfingiittina, ashoveriittina ja sweetiittinä. Nämä harvinaiset mineraalit ovat itse asiassa Zn (OH)2: n luonnollisia polymorfeja. Materiaalitieteessä mikä tahansa kiinteä aine on polymorfista, jos se esiintyy useammassa kuin yhdessä muodossa, kuten ortorombisena tai tetragonaalisena.
Sinkkihydroksidivalmiste
sitä valmistetaan yleensä lisäämällä sinkkisuolaliuokseen kuten sinkkikloridiin tai sinkkisulfaattiin kohtalainen määrä natriumhydroksidiliuosta. Nämä kaksi yhdistettä reagoivat normaaliolosuhteissa muodostaen valkoisen saostuman Zn (OH) 2. Reaktiossa tulee käyttää laimeaa natriumhydroksidiliuosta, jotta epäorgaaninen yhdiste ei liukene. Normaaliolosuhteissa sinkkisuola hajoaa muodostaen sinkki-ionin, joka yhdistyy kahden hydroksidi-ionin kanssa natriumhydroksidiliuoksesta muodostaen sinkkihydroksidia.
Zn2++ 2oh- → Zn(OH)2
Jos suolaliuokseen lisätään ylimääräistä natriumhydroksidia, aluksi muodostuva Zn (OH)2– sakka liukenee värittömäksi tsincaatti-ioniliuokseksi, kuten alla on esitetty:
Zn (OH)2 + 2OH – → Zn(OH)42 –
tätä sinkkihydroksidin ominaisuutta käytetään laajasti sinkki-ionien läsnäolon havaitsemiseen liuoksessa. Se ei kuitenkaan ole ainutlaatuinen testausmenetelmä, sillä siellä on monia alumiinin ja lyijyn yhdisteitä, jotka käyttäytyvät hyvin samalla tavalla.
sinkkihydroksidin liukeneva ominaisuus voi vaikuttaa siihen, että Ionia tavallisesti ympäröivät vesiligandit. Kun liuokseen lisätään ylimääräistä natriumhydroksidia, kaksi hydroksidi-Ionia pelkistää sen negatiivisesti varautuneeksi kompleksiksi, jolloin se liukenee.
Sinkkihydroksidi käyttää
joitakin Zn (OH)2: n yleisiä käyttötarkoituksia ovat:
kirurgiset sidokset
sitä käytetään kirurgisiin sidoksiin, joissa se toimii imukykyisenä. Suuret siteet, joita käytetään leikkauksen jälkeen, päällystetään sinkkiyhdisteellä veren imemiseksi haavasta.
suojapinnoite
teräs ja rauta levitetään useimmiten sinkityllä pinnoitteella galvanoinniksi kutsutun prosessin kautta. Kosteissa olosuhteissa näiden galvanoitujen metallien päälle muodostuu kerros sinkkihydroksidia, jotta ne eivät ruostuisi.
Mordantti
Sinkkihydroksidi on hyvin hyytelömäistä (hyytelömäistä) ja toimii yleensä peitteenä, joka asettaa väriaineita eri kankaille tai kudoksille. Väriaine on yleensä kemiallinen reagenssi, joka muodostaa metallikompleksin Zn(OH)2: n kanssa ja kiinnittyy voimakkaasti kangasvuoriin.
torjunta-aineet
sitä käytetään usein välituotteena kaupallisessa torjunta-aineiden ja pigmenttien tuotannossa.

ajankohtaiset liuokset
Zn (OH)2: n ja sinkkioksidin yhdistelmää käytetään laajalti kalamiinivoiteissa, voiteissa, vauvapuutereissa, ihovoiteissa ja kosmetiikassa. Se reagoi vahvojen emästen kanssa amfoteerisen luonteensa vuoksi muodostaen tsincaatteja, joita käytetään suun kautta otettavina lääkkeinä useiden häiriöiden hoitoon.
Sähköakkuja
sitä käytetään myös suurienergisissa sähköakkuissa, jotka ovat palautuva reaktio.
kumin seostusta
Zn (OH)2 käytetään kumin eri ainesosien seostamiseen tai sekoittamiseen loppukäyttöominaisuuksien optimoimiseksi kuluttajan tarpeen mukaan.
sinkkiyhdisteitä
monenlaisia sinkkiyhdisteitä kuten sinkkioksidia, sinkkisulfaattia ja sinkkinitraattia valmistetaan kaupallisesti epäorgaanisen kemikaalin avulla.
Sinkkihydroksidi MSD
se on yleensä syttymätöntä eikä aiheuta vaaraa työntekijöille. Yhdistettä ei kuitenkaan pidä maistaa tai niellä, sillä se saattaa sisältää vain vähän toksikologisia ainesosia.