beskytter cellen og opretholder sin form, bakterier kan kategoriseres efter deres cellevægstype:
grampositive vægge er tykke med lidt lipid.
gramnegative vægge er meget tyndere med to lag. Nogle bakterier har et slimet lag af polysaccharider og polypeptider, så de kan fastgøres til genstande og yde beskyttelse.
70s ribosomer
disse er til udførelse af proteinsyntese. De er mindre end 80 ‘ erne ribosomer i eukaryote celler. Flagellum en anden valgfri funktion er en projektion, der bevæger sig rundt for at lade cellen bevæge sig. En celle kan have flere flageller arrangeret omkring den.
nukleart materiale
en foldet masse af DNA og RNA, også kaldet kerneområdet-indeholdende alle de gener, der kræves til vitale funktioner. Plasmid er yderligere ringe af genetisk materiale, der ikke er afgørende for cellen, indeholder ofte gener for antibiotikaresistens.
Mesosom
en indfoldning af membranen, der er respirationsstedet (som en mitokondrion) – dens form forbedrer overfladearealet. Eksistensen af mesosomet er omstridt, og de fleste forskere mener, at det er en fejl i elektronmikroskopteknikken.
derudover har bakterier en afgørende struktur, der omgiver hele cellen, Peptidoglycan (PG), som danner en sacculus omkring bakteriecellen, er en essentiel cellevægspolymer, da interferens med dens syntese eller struktur fører til tab af celleform og integritet efterfulgt af bakteriel død.
peptidoglycanlaget som vist i figur 2 består af en matrice af polysaccharidkæder sammensat af alternerende (kursiv) N-acetylmuraminsyre (MurNAc) N-acetylglucosamin (GlcNAc) sukkerdele tværbundet gennem pentapeptid sidekæder.
klassificering
Hans christian gram: en dansk mikrobiolog, havde udviklet Gram-pletterne for lettere at visualisere bakterier under mikroskop. Baseret på farvningsmønsteret er patogene bakterier klassificeret i to hovedkategorier, nemlig. Gram ( + ) og Gram ( – ) bakterier. Skematisk billede af cellevæggen efter gramfarvning er vist i figur 3 .
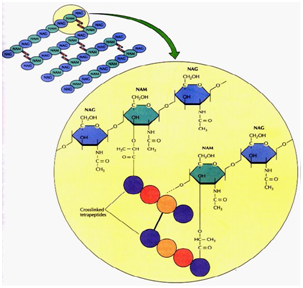
figur 2: Peptidoglycan lag.
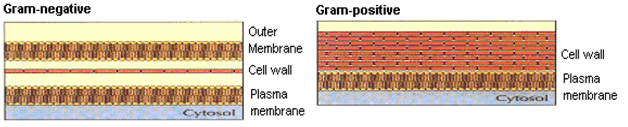
figur 3: Gram+Ve og Gram-Ve cellevæg.
cellevæggen af gram (+): bakterier, selvom de er komplekse nok, er enklere end Gram (-) organismer. På selve ydersiden af cellen er der sat antigene determinanter, som hjælper med at klæbe til en bestemt målcelle. Den næste barriere er cellevæggen, svampet, geldannende lag, dvs. peptidoglycan lag uden for cytoplasmatisk membran og tegner sig for 50% af den tørre vægt af bakterien. Under dette lag er den lipoide cytoplasmatiske cellemembran, f .eks. Staphylococci aureus, Streptococci pneumoniae, Bacillus subtilis.
Med gram ( – ): bakterier er cellevæggen mere kompleks og mere lipoidal. Disse celler indeholder normalt en yderligere ydre membran, som indeholder komplekse lipopolysaccharider, der koder for antigene reaktioner. Under dette ligger, mindre imponerende, lag af peptidoglycan dette efterfølges af en phospholipidrig cytoplasmisk membran. F. eks. Escherichia Coli, Haemophilus, Pseudomonas aeruginosa .
mikroorganismer er en gruppe af organismer, der omfatter levende (f.eks. B) bakterier, svampe, protosoer, alger osv.) såvel som ikke-levende organismer (f. eks. (V) Virus).
bakterier: bakterier er encellede organismer, der findes i naturen på alle levende og ikke-levende ting ved temperaturområde fra under nul (psykrofiler) til op til 1000C (termofile). Bakterier klassificeres efter formen af cellen, på temperatur, hvor de vokser, på grundlag af gruppe af celler, afhængigt af patogenecity og farvning. På grund af farvning klassificeres de yderligere som Gram-positive (Gram+ve) og Gram-negative (Gram-ve). Gram-positive bakterier viser violet farve, og Gram-negative bakterier viser lyserød farve i en procedure kaldet Gram-farvning udviklet af C. Gram. Baseret på patogenicitet er klassificeringen patogen sygdom/infektion, der forårsager dvs.infektiøs og ikke-patogen-ikke infektiøs. I medicinsk kemi er denne klassificering vigtig.
svampe: svampe er universelle i distribution. Mange er jordbaserede og trives bedst i jorden. Nogle lever i væv af planter og dyr, mens resten findes i akvatiske steder. Mange svampe vokser på madvarer som brød, syltetøj, pickles, frugt og grøntsager. Svampe er saprofytiske og parasitære. Saprofytter vokser på dødt organisk materiale, mens parasitter lever på levende kroppe af andre dyr. Parasitiske svampe inkluderer Candida albicans, som er det forårsagende middel til Candiditis.
Protosoer: Protosoer er minut og acellulære dyrk uden væv og organer, der har en eller flere kerner. De lever frit, eller de forbliver i forbindelse med dyr og planter. Nogle protosoer, der er parasitære, inkluderer amøbe, der forårsager amoebiasis og Plasmodium, der forårsager Malaria.
Vira: Vira er acellulære mikroorganismer, som er intracellulære obligatoriske parasitter. De indtager position mellem levende og ikke-levende. Virus er værtsspecifikke og afhænger af værter som planter, dyr og bakterier for deres overlevelse. Virus er iboende intracellulære parasitter af levende celler. tidligere. M. poliomyelitis forårsager Poliomyelitis, HIV forårsager AIDS.
infektioner af patogene mikrober: Mange mikroorganismer eller mikrober er patogene for planter, dyr og menneskeliv, der forårsager forskellige sygdomme, hvilket resulterer i omfattende dødelighed og sygelighed. Patogene mikrober er mikroorganismer, der forårsager smitsomme sygdomme. Disse involverede organismer inkluderer patogene bakterier, der forårsager sygdomme som pest, tuberkulose og miltbrand; protosoer, der forårsager sygdomme som malaria, sovesyge og toksoplasmose; og også svampe, der forårsager sygdomme som ringorm, candidiatis eller histoplasmose. Imidlertid er andre sygdomme som influens, gul feber eller AIDS forårsaget af patogene vira, som ikke er levende organismer. Patogene bakterier bidrager til andre globalt vigtige sygdomme som lungebetændelse forårsaget af streptokokker og Pseudomonas og fødevarebårne sygdomme, som kan være forårsaget af bakterier som Shigella, Campylobacter og Salmonella. Patogene bakterier forårsager også infektioner som stivkrampe, tyfusfeber, difteri, syfilis og spedalskhed . Hver parasitisk art har en karakteristisk interaktion med deres værter. Mikroorganismer som Staphylococcus eller Streptococcus arter, der forårsager hudinfektioner lungebetændelse, meningitis og andre former for overfladeinfektioner. På den anden side er mange organismer en del af normal flora af menneskekroppen, der findes på hud, næse, urinveje, tarm osv. uden at forårsage sygdom. Men nogle gange blev disse opportunistiske parasit og førte til infektioner . Obligatoriske intracellulære parasitter som Rickettesia og Chlamydia er i stand til at vokse og reproducere kun inden for værtsceller. Nogle arter som Pseudomonas aeruginosa, Burkholderia cenocepacia og Mycobacterium avium er parasitære, når de lider af immunundertrykkelse eller cystiske fibroseceller . Udvikling af nye terapeutiske midler til behandling eller bekæmpelse af denne infektion/infektiøse mikroorganisme er en kontinuerlig proces i den kliniske medicin. Med fremkomsten af antibiotikaresistente stammer er syntese af nye lægemidler blevet et af hovedmålene for forskere over hele kloden.
antifungale midler: Et antisvampemiddel er et lægemiddel, kemikalier eller andre stoffer, der selektivt eliminerer svampepatogener fra en vært med minimal toksicitet for værten, som oftest findes på hud, hår og negle. Svampen er en eukaryot organisme, der er klassificeret som et separat rige fra planter, dyr og bakterier. Svampe indeholder encellede, multinucleate og multicellulære former de klassificeres på grundlag af deres reproduktive sporer og arten af hyfer. De deler sig seksuelt eller aseksuelt eller på begge måder. Svampe er næsten udelukkende multicellulære med undtagelse af gær Saccharomyces cerviseae, som er fremtrædende encellet svamp. Svampe er heterotrofe og får deres energi fra en anden organisme, hvad enten de er levende eller døde. Svampe er eukaryote protista, der adskiller sig fra bakterier på mange måder, da de besidder stiv cellevæg indeholdende chitin, mannan, andre polysaccharider, og deres cytoplasmatiske membran indeholder sterol. Den største forskel mellem svampeceller og plantecelle er, at svampecellevægge indeholder chitin, mens planter indeholder cellulose .
antifungale midler klassificeres efter deres måde at interferere med:
- cellevægssyntese,
- Plasmamembranintegritet,
- nukleinsyresyntese,
- Ribosomal funktion (Figur 4). hvis det er nødvendigt, er det nødvendigt at tage hensyn til, at der ikke er nogen risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko for, at der opstår en risiko.Echinocandin: Capsofungin, Anidulafungin, Micafungin.antimetabolit: flucytosin (5-FCEN).Nikkomycin.
topiske svampedræbende stoffer: polyenantibiotika: Amphotericin B, Nystatin, Hamycin, Natamycin, Rimocidin, Hitachimycin, Filipin.hvis du er i tvivl om, hvorvidt du er i stand til at gøre dette, skal du være opmærksom på, at du ikke er i stand til at gøre det. hvilken: Tolnaftat, Undecyklinsyre, Povidonjod, Triacetin, ensianviolet, natriumthiosulfat, Cicloporoksolamin, Bensonsyre, Kinidochlor.
- systemiske antifungale lægemidler til overfladiske infektioner:
- heterocykliske bensofuraner: Corticofunvin, Griseofulvin.allylamin: Terbinafin, butenafin, naftifin.
mykologi: biologiens disciplin, der er afsat til studiet af svampe, er kendt som mykologi. Mykologi beskæftiger sig med den systematiske undersøgelse af svampe, herunder deres genetiske og biokemiske egenskaber. Mykoser, der påvirker mennesker, kan opdeles i fire grupper baseret på penetrationsniveauet i kroppens væv som .
- overfladiske mykoser: forårsaget af svampe, der kun vokser på den yderste overflade af huden eller håret. Et eksempel på en svampeinfektion er Tinea Versicolor, en svampeinfektion, der ofte påvirker huden hos unge mennesker, især brystet, ryggen, overarmene og benene.
- kutane mykoser eller dermatomycoser: Forårsaget af svampe vokser kun i de overfladiske lag af hud, negle og hår forårsager infektioner almindeligvis kendt som fodsvamp, jock kløe og ringorm.
- subkutane mykoser: forårsaget af svampe, der trænger ind under huden i det subkutane, bindevæv og knoglevæv. Den mest almindelige er sporotrichose, der forekommer blandt gartnere og landmænd, der kommer i direkte kontakt med jord.
- systemiske eller dybe mykoser: er forårsaget af primære patogene og opportunistiske svampepatogener. De primære patogene svampe forårsager infektion i en normal vært; mens opportunistiske patogener kræver immundepressant vært for at etablere infektion (f.eks. kræft, kirurgi og AIDS). De primære patogener får normalt adgang til værten via luftvejene og inkluderer Coccidioides immitis, Histoplasma capsulatum, Blastomyces dermatitidis og Paracoccidioides brasiliensis. De opportunistiske svampe invaderer via luftvejene og fordøjelseskanalen, og omfatter Cryptococcus neoformans, Candida spp., Aspergillus spp., Penicillium marneffei, Gygomyceter, Trichosporon beigelii og Fusarium spp.
mykologi-patogene svampe: Undersøgelsen af patogene svampe kaldes medicinsk mykologi. Patogene svampe forårsager sygdom hos mennesker eller andre organismer. De almindeligt observerede patogene svampe er optaget nedenfor,
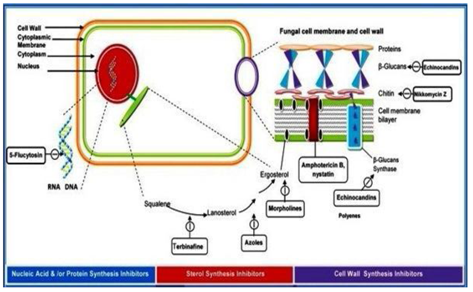
figur 4: klassificering af antifungale midler ved deres virkningsmåde.
Candida: Candida-arter er vigtige humane patogener, der forårsager opportunistiske infektioner hos immunkompromitterede værter (AIDS-patienter, kræftpatienter og transplantationspatienter). Infektioner forårsaget af Candida-arten er vanskelige at behandle og kan være dødelige. Candida-arter alene tegner sig for 30-40% dødstilfælde forårsaget af de systemiske infektioner. Svampearter af slægten Candida lever generelt i fællesskab på og i den menneskelige krop. Der er en stigning i udviklingen af lægemiddelresistens fra Candida-arter til nuværende terapier, der motiverer forskere til at forstå deres genetik og opdage nye terapeutiske mål.
Aspergillus: de aerosoliserede Aspergillus-sporer findes næsten overalt omkring mennesket og har generelt ikke sundhedsmæssige problemer. Men Aspergillus er stadig i stand til at forårsage sygdom på tre hovedmåder: ved produktion af mykotoksiner; ved induktion af allergifremkaldende reaktioner; og endelig ved de lokaliserede eller systemiske infektioner. Aspergillus flavus producerer mykotoksiner, aflatoksin, der kan fungere som både toksin og kræftfremkaldende, har evnen til at forurene fødevarer såsom nødder.
Cryptococcus: flertallet af Cryptococcus-arter findes i jorden og forårsager generelt ikke sygdom hos mennesker. Undtagelse er Cryptococcus neoformans, der forårsager sygdom hos immundæmpende patienter som AIDS, hvilket forårsager en alvorlig form for meningitis og meningo-encephalitis.Histoplasma capsulatum kan forårsage histoplasmose hos mennesker, hunde og katte. Infektionen skyldes normalt indånding af forurenet luft og er udbredt.
Pneumocystis: Pneumocystis jirovecii kan forårsage en form for lungebetændelse hos mennesker med svækket immunsystem, såsom ældre, AIDS-patienter og for tidligt fødte børn.
Stachybotrys: Stachybotrys chartarum kan forårsage åndedrætsskader og svær hovedpine i huse, der er vedvarende fugtige.
svampeinfektion fremtrædende i særlige sygdomme: foreningen af mest forekommende svampe sammen med patienten, der lider af den særlige sygdom, er optaget nedenfor,
- Candida arter, Aspergillus arter, Phycomyces arter: leukopeni.Diabetes er en af de mest almindelige årsager til diabetes.
- Candida, Cryptococcus, Histoplasma: maligniteter og Hodgkins sygdom.
- Candida, Cryptococcus, Histoplasma: AIDS.
klinisk signifikante svampe og det sted, de påvirker: patogeniciteten og virulensen af svampe, der forårsager infektioner, hos mennesker er stor bekymring i den kliniske verden, der fokuserer på de vigtigste årsagsmidler til sygdom, især Candida, Cryptococcus og Aspergillus spp. Den store mangfoldighed af potentielt skadelige svampe, der findes uden for disse grupper, selvom sjældne stadig kan have potentiale til at være vigtigere end de almindelige kliniske svampe. Det sted, der er påvirket af de klinisk signifikante svampe, er tilmeldt som nedenfor,
- malassesia furfur og Eksophiala verneckii: Superficial skin.
- Piedraia hortae and Trichosporon beigelii: Hair.
- Microsporum species: Skin and hair.
- Epidermophyton species: Skin and nails.
- Trichophyton species: Skin, hair and nails.
- Sporothrix schenckii, Cladosporium species: Chromoblastomycosis.
- Histoplasma capsulatum, Penicillium species: Systemic respiratory.
- Blastomyces dermatitidis: Subcutaneous/respiratory.
- Cryptococcus neoformans: Respiratory/CNS.
Antifungal resistance: Udviklingen af lægemiddelresistens i svampe er et bredt begreb, der beskriver svigt i den nuværende svampedræbende behandling for at overvinde svampeinfektionen. De antifungale terapier er designet til at udrydde svampeinfektion ved forskellige virkningsmekanismer, som ved at forstyrre deres reproduktive evner, ødelægge cellevæggene eller ved at modificere svampens DNA og ændre cellens funktion. Antifungal resistens er traditionelt klassificeret som tre typer
- primær (iboende),
- sekundær (erhvervet),
- klinisk resistens.
i det sidste årti bliver mikroorganismer lægemiddelresistente i en meget hurtigere hastighed end hastigheden for opdagelse af nye lægemidler. Svampes lægemiddelresistens observeres importunately hos patienter med svagt immunsystem, der lider af sygdomme som AIDS og kræft. Forskerne står således over for en stor udfordring med at udvikle nye, sikre og mere effektive svampemidler under hensyntagen til stigningen i opportunistiske infektioner i den immunkompromitterede vært. Dette kan overvindes ved opdagelsen af nye lægemidler, der virker ved nye virkningsmekanismer .
historisk perspektiv: I 1903 var de Beurmann og Gougerot de første til at diskutere brugen af kaliumiodid til behandling af sporotrichose. Hvidmark i 1907 behandlede overfladiske svampeinfektioner ved hjælp af salve. I midten af 1940 ‘ erne blev sulfonamider brugt til behandling af paracoccidioido mycosis, selvom de havde begrænset effektivitet over for fungistatiske egenskaber og krævede længere tid til behandling med høj tilbagefaldshastighed. Dette blev efterfulgt af den kommercielle brug af penicillin i 1940 ‘ erne. I 1944 blev opdagelsen og udviklingen af streptomycin opdaget i 1944. Det blev efterfulgt af opdagelserne af Chloramphenicol i 1947 og chlortetracyclin i 1948. I 1948 blev et antiprotosalt middel med antifungal virkning anvendt til behandling af blastomycosis. I 1951 opdagede han det første polyenantibiotikum kaldet nystatin, almindeligt anvendt topisk og oral polyen. I 1952 blev substituerede forbindelser fundet at have antifungale egenskaber. Makroliderne blev udviklet i 1952 med bakteriostatiske egenskaber. I 1956 guld et al. rapporterede de antifungale egenskaber af polyen amphotericin B, som var den første signifikant effektive systemiske antifungale. Det blev standard og snart det erstattet hydroksy stilbamidin. Amphotericin B nød den primære status som kun antisvampemiddel, der var tilgængeligt til behandling af systemiske mykoser i næsten årti, mod hvilke nyere terapier for systemiske mykoser blev sammenlignet. I 1957 flucytosin, blev udviklet som et svampedræbende middel, der havde undladt at give gunstige resultater for anvendelsen som cytostatisk middel. Anvendelsen af offlucytosin som monodrug udviklede ofte svampebestandighed, hvilket førte til anvendelse i kombination med Amphotericin B for at overvinde modstanden. Det første signifikante orale svampedræbende middel Griseofulvin blev udviklet i 1958, som blev tilgængelig til behandling af overfladiske mykoser. Før Griseofulvin var behandlingen af overfladiske Dermatophytoser kun af de topiske lægemidler, som ikke var særlig effektive mod Tinea capitis og Onychomycosis. De halvsyntetiske penicilliner, cephalosporiner og glycopeptider blev udviklet fra 1958 og fremefter. Udviklingen af Chlormidasol som en 5% creme i 1958 var gavnlig over en lang række kutane mykoser. I 1960 ‘ erne blev der rapporteret om antifungale og antihelminthiske egenskaber. I 1969 blev det introduceret, som snart blev efterfulgt af econasol i 1974. De allylaminer, der blev opdaget i 1974, er de andre klasser af svampedræbende stoffer, der har en betydelig indvirkning på svampedræbende behandling, især for overfladiske dermatomycoses, herunder Onychomycosis. Den blev udviklet i 1977 og er siden blevet standard blandt de blå. I midten af 1980 ‘ erne blev to bredspektrede, oralt tilgængelige triasoler, Fluconasol (1982) og Itraconasol (1984) opdaget. Intensiv forskning begyndte mellem 1990-1999 for at udvikle nye antisvampemidler og resulterede i introduktion af tre antisvampemidler (2000), micafungin (2005)-Schering-Plough, Ravuconasol (2007) og tre nye echinocandiner (Caspofungin (2002) Anidulafungin (2004), Micafungin (2006) til deresklinisk brug .