| Citric acid | |
|---|---|
|
|
| General | |
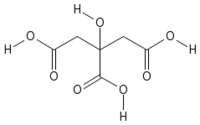
| Systematic name | 2-hydroxypropane- 1,2,3-tricarboxylic acid |
| Empirical formula | C6H8O7 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Molar mass | 192.13 g/mol |
| Appearance | crystalline white solid |
| CAS number | |
| Properties | |
| Density and phase | 1.665 g/cm³ |
| Solubility in water | 133 g/100 ml (20°C) |
| Melting point | 153 °C (307.4F, 426 K) |
| Boiling point | decomposes at 175 °C (448 K) |
| Acidity (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| Hazards | |
| MSDS | External MSDS |
| Main hazards | skin and eye irritant |
| Supplementary data page | |
| Thermodynamic data |
Phase behaviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related compounds | sodium citrate, calcium citrate |
Citric acid is a weak organic acid found en cítricos. Es un conservante natural y también se usa para agregar un sabor ácido (ácido) a los alimentos y refrescos. En bioquímica, es importante como intermediario en el ciclo del ácido cítrico y, por lo tanto, se produce en el metabolismo de casi todos los seres vivos. También sirve como un agente de limpieza benigno para el medio ambiente y actúa como antioxidante.
El ácido cítrico existe en una variedad de frutas y verduras, pero está más concentrado en limones y limas, donde puede abarcar hasta el 8% del peso seco de la fruta.
Propiedades
A temperatura ambiente, el ácido cítrico es un polvo cristalino blanco. Puede existir en forma anhidra (sin agua) o como monohidrato que contiene una molécula de agua por cada molécula de ácido cítrico. La forma anhidra se cristaliza a partir de agua caliente, mientras que el monohidrato se forma cuando el ácido cítrico se cristaliza a partir de agua fría. El monohidrato se puede convertir en forma anhidra calentándolo por encima de 74°C.
Químicamente, el ácido cítrico comparte las propiedades de otros ácidos carboxílicos. Cuando se calienta por encima de 175 ° C, se descompone a través de la pérdida de dióxido de carbono y agua.

Historia
El descubrimiento de ácido cítrico ha sido acreditado para el siglo 8 Islámica alquimista Jabir Ibn Hayyan (Geber). Los eruditos medievales en Europa eran conscientes de la naturaleza ácida de los jugos de limón y lima; tal conocimiento está registrado en la enciclopedia del siglo XIII Speculum Majus (El Gran Espejo), compilada por Vicente de Beauvais. El ácido cítrico fue aislado por primera vez en 1784 por el químico sueco Carl Wilhelm Scheele, quien lo cristalizó a partir de jugo de limón. La producción de ácido cítrico a escala industrial comenzó en 1860, basada en la industria italiana de cítricos.
En 1893, C. Wehmer descubrió que el moho del Penicilio podía producir ácido cítrico a partir del azúcar. Sin embargo, la producción microbiana de ácido cítrico no se volvió industrialmente importante hasta que la Primera Guerra Mundial interrumpió las exportaciones de cítricos italianos. En 1917, el químico estadounidense de alimentos James Currie descubrió que ciertas cepas del moho Aspergillus niger podían ser productores eficientes de ácido cítrico, y Pfizer comenzó la producción a nivel industrial utilizando esta técnica dos años más tarde.
Producción
En esta técnica de producción, que sigue siendo la principal ruta industrial al ácido cítrico utilizada hoy en día, los cultivos de Aspergillus niger se alimentan de sacarosa para producir ácido cítrico. Después de que el molde se filtra de la solución resultante, el ácido cítrico se aísla precipitándolo con cal (hidróxido de calcio) para producir sal de citrato de calcio, a partir de la cual el ácido cítrico se regenera mediante tratamiento con ácido sulfúrico.
Alternativamente, el ácido cítrico a veces se aísla del caldo de fermentación por extracción con una solución de hidrocarburo de la trilaurilamina de base orgánica, seguida de reextracción de la solución orgánica por agua.
Ciclo de Krebs
El ácido cítrico es uno de una serie de compuestos involucrados en la oxidación fisiológica de grasas, proteínas y carbohidratos a dióxido de carbono y agua.
Esta serie de reacciones químicas es fundamental para casi todas las reacciones metabólicas, y es la fuente de dos tercios de la energía derivada de los alimentos en organismos superiores. Fue descubierto por Sir Hans Adolf Krebs. Krebs recibió el Premio Nobel de Fisiología o Medicina en 1953 por el descubrimiento. La serie de reacciones se conoce correctamente como ciclo del ácido tricarboxílico, pero también se conoce como ciclo del ácido cítrico o ciclo de Krebs.
Utiliza
Aditivo alimentario
Como aditivo alimentario, el ácido cítrico se utiliza como aromatizante y conservante en alimentos y bebidas, especialmente refrescos; se indica con el número E330. Las sales de citrato de varios metales se utilizan para entregar esos minerales en una forma biológicamente disponible en muchos suplementos dietéticos. Las propiedades tamponadoras de los citratos se utilizan para controlar el pH en productos de limpieza domésticos y productos farmacéuticos.
Ablandador de agua
La capacidad del ácido cítrico para quelar metales lo hace útil en jabones y detergentes para ropa. Al quelar los metales en el agua dura, permite que estos limpiadores produzcan espuma y funcionen mejor sin necesidad de ablandar el agua. Del mismo modo, el ácido cítrico se utiliza para regenerar los materiales de intercambio iónico utilizados en los ablandadores de agua al eliminar los iones metálicos acumulados como complejos de citrato.
Otros
Se utiliza en la industria biotecnológica y farmacéutica para pasivar tuberías de proceso de alta pureza en lugar de usar ácido nítrico, ya que el ácido nítrico es un problema de eliminación peligroso una vez que se usa para este propósito, mientras que el ácido cítrico no lo es.
También es el ingrediente activo de algunas soluciones de limpieza doméstica para baños y cocinas. Una solución con una concentración de ácido cítrico del 6% eliminará las manchas de agua dura del vidrio sin frotar.
El ácido cítrico se usa comúnmente como tampón para aumentar la solubilidad de la heroína marrón. Los sobres de ácido cítrico de un solo uso se han utilizado como un incentivo para que los consumidores de heroína intercambien sus agujas sucias por agujas limpias en un intento de disminuir la propagación del SIDA y la hepatitis. Otros acidificantes utilizados para la heroína marrón son el ácido ascórbico, el ácido acético y el ácido láctico: en su ausencia, el inyector de drogas a menudo sustituye el jugo de limón o el vinagre.
El ácido cítrico es uno de los productos químicos necesarios para la síntesis de HMTD; un explosivo altamente sensible al calor, la fricción y los golpes similar al peróxido de acetona (también conocido como «Madre de Satanás»). Debido a esto, la compra de grandes cantidades de ácido cítrico puede ser vista por algunos gobiernos como un indicador de una posible actividad terrorista.
El ácido cítrico también se puede agregar al helado para mantener separados los glóbulos grasos. También se puede agregar a las recetas en lugar de jugo de limón fresco. El ácido cítrico se utiliza junto con bicarbonato de sodio en una amplia gama de fórmulas efervescentes, tanto para la ingestión (por ejemplo, polvos y tabletas) como para el cuidado personal (por ejemplo, sales de baño, perlas de baño y un método de limpieza bueno para la grasa).
Cuando se aplica sobre el cabello, el ácido cítrico abre la cutícula. Mientras la cutícula está abierta, permite una penetración más profunda de los agentes de limpieza. Por lo general, no se recomienda si se ha realizado alguna coloración artificial del cabello, a menos que esté tratando de quitarle el color. Se puede usar en champú. También se utiliza en el producto «Sun-In» para blanquear el cabello por la misma razón.
El ácido cítrico también se usa como baño de parada en fotografía. El revelador es normalmente alcalino, por lo que un ácido suave lo neutralizará, aumentando la eficacia del baño de parada en comparación con el agua corriente.
Seguridad
El ácido cítrico es reconocido como seguro para su uso en alimentos por todas las principales agencias reguladoras de alimentos nacionales e internacionales. Está presente de forma natural en casi todas las formas de vida, y el exceso de ácido cítrico se metaboliza y elimina fácilmente del cuerpo.
Curiosamente, a pesar de su ubicuidad en el cuerpo, se sabe que existe intolerancia al ácido cítrico en la dieta. Hay poca información disponible, ya que la afección parece ser rara, pero al igual que otros tipos de intolerancia a los alimentos, a menudo se describe como una reacción «pseudoalérgica».
El contacto con ácido cítrico seco o con soluciones concentradas puede provocar irritación de la piel y los ojos, por lo que se debe usar ropa protectora cuando se manipulen estos materiales.
Reclamaciones de cáncer
Ha habido informes erróneos de que el E330 es una causa importante de cáncer. Se cree que esto ha sido provocado por malentendidos y confusión sobre la palabra Krebs. En este caso, se refiere a Sir Hans Adolf Krebs, descubridor del ciclo de Krebs, y no a la palabra alemana para cáncer.
- Garden, J., Roberts, K., Taylor, A., and Robinson, D. (2003). «Evaluation of the Provision of Single Use Citric Acid Sachets to Injecting Drug Users» (en inglés). Scottish Center for Infection and Environmental Health (en inglés).
- http://www.silverprint.co.uk/chem4.html