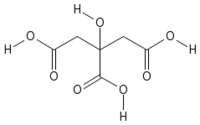
| Citric acid | |
|---|---|
|
|
| General | |
| Systematic name | 2-hydroxypropane- 1,2,3-tricarboxylic acid |
| Empirical formula | C6H8O7 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Molar mass | 192.13 g/mol |
| Appearance | crystalline white solid |
| CAS number | |
| Properties | |
| Density and phase | 1.665 g/cm³ |
| Solubility in water | 133 g/100 ml (20°C) |
| Melting point | 153 °C (307.4F, 426 K) |
| Boiling point | decomposes at 175 °C (448 K) |
| Acidity (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| Hazards | |
| MSDS | External MSDS |
| Main hazards | skin and eye irritant |
| Supplementary data page | |
| Thermodynamic data |
Phase behaviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related compounds | sodium citrate, calcium citrate |
Citric acid is a weak organic acid found citrusfélékben. Természetes tartósítószer, és savas (savanyú) ízt is adnak az ételekhez és üdítőitalokhoz. A biokémiában fontos, hogy közbenső legyen a citromsavciklusban, ezért szinte minden élőlény metabolizmusában fordul elő. Környezetbarát tisztítószerként is szolgál, antioxidánsként működik.
A citromsav sokféle gyümölcsben és zöldségben létezik, de leginkább citromban és limesben koncentrálódik, ahol a gyümölcs száraz tömegének akár 8% – át is kiteheti.
tulajdonságok
szobahőmérsékleten a citromsav fehér kristályos por. Vízmentes (vízmentes) formában vagy monohidrátként létezhet, amely minden citromsav molekulához egy vízmolekulát tartalmaz. A vízmentes forma forró vízből kristályosodik, míg a monohidrát akkor alakul ki, amikor a citromsavat hideg vízből kristályosítják. A monohidrát vízmentes formává alakítható 74°C feletti melegítéssel.
kémiailag a citromsav megosztja más karbonsavak tulajdonságait. 175 ° C fölé hevítve a szén-dioxid és a víz elvesztésével bomlik.

történelem
a citromsav felfedezése a 8.századi Iszlám alkimista Jabir Ibn Hayyan (Geber) tulajdonába került. A középkori tudósok Európában tisztában voltak a citrom-és mészlevek savas természetével; ezt a tudást a Beauvais Vincent által összeállított 13.századi enciklopédia Speculum Majus (a nagy tükör) rögzíti. A citromsavat először 1784-ben izolálta Carl Wilhelm Scheele svéd kémikus, aki citromléből kristályosította. Az ipari méretű citromsavtermelés 1860-ban kezdődött, az olasz citrusfélék iparán alapulva.
1893 – ban C. Wehmer felfedezte, hogy a Penicillium penész citromsavat termelhet a cukorból. A citromsav mikrobiális termelése azonban nem vált iparilag fontossá, amíg az első világháború meg nem zavarta az olasz citrusexportot. 1917-ben James Currie amerikai élelmiszer-kémikus felfedezte, hogy az Aspergillus niger penész bizonyos törzsei hatékony citromsavtermelők lehetnek, a Pfizer pedig két évvel később kezdte meg ipari szintű termelését ezzel a technikával.
termelés
ebben a gyártási technikában, amely még mindig a legfontosabb ipari út a citromsavhoz, amelyet ma használnak, az Aspergillus niger tenyészeteit szacharózban táplálják citromsav előállításához. Miután a penész kiszűri a kapott oldat, citromsav elszigetelt azzal, hogy támogatta a mész (kalcium-hidroxid), hogy a hozam a kalcium-citrát só, ahonnan a citromsav regenerálni a kezelés kénsav.
Vagy, citromsav néha szigetelve a erjedés húsleves extrakcióval a szénhidrogén-megoldás a szerves bázis trilaurylamine, majd újra-extrahálása a szerves megoldás a víz.
Krebs cycle
a citromsav a zsírok, fehérjék és szénhidrátok szén-dioxiddá és vízzé történő fiziológiai oxidációjában részt vevő vegyületek egyikének egyike.
Ez a kémiai reakciósorozat szinte minden metabolikus reakcióban központi szerepet játszik, és a magasabb organizmusokban az élelmiszerből származó energia kétharmadának forrása. Sir Hans Adolf Krebs fedezte fel. Krebs 1953-ban fiziológiai vagy orvosi Nobel-díjat kapott a felfedezésért. A reakciósorozat megfelelően ismert, mint a trikarbonsav ciklus, de az is ismert, mint a citromsav ciklus vagy a Krebs ciklus.
élelmiszer-adalékanyag
élelmiszer-adalékanyagként a citromsavat ízesítőként és tartósítószerként használják élelmiszerekben és italokban, különösen üdítőitalokban;E szám E330. A különböző fémek citrátsóit arra használják, hogy ezeket az ásványi anyagokat biológiailag rendelkezésre álló formában szállítsák számos étrend-kiegészítőben. A citrátok pufferelési tulajdonságait a háztartási tisztítószerek és gyógyszerek pH-értékének szabályozására használják.
vízlágyító
a citromsav Fémek kelátképződésére való képessége hasznos a szappanokban és a mosószerekben. A fémek kemény vízben történő kelátképzésével lehetővé teszi, hogy ezek a tisztítószerek habot termeljenek, és vízlágyítás nélkül jobban működjenek. Hasonlóképpen, a citromsavat a vízlágyítókban használt ioncserélő anyagok regenerálására használják, a felhalmozódott fémionok citrát komplexekként történő eltávolításával.
Egyéb
a biotechnológiában és a gyógyszeriparban a salétromsav használata helyett nagy tisztaságú csővezetékek passziválására használják, mivel a salétromsav veszélyes ártalmatlanítási probléma, ha erre a célra használják, míg a citromsav nem.
Ez is a hatóanyag egyes háztartási tisztítószerek fürdőszobák és konyhák. A 6% – os citromsav-koncentrációjú oldat súrolás nélkül eltávolítja a kemény vízfoltokat az üvegből.
a citromsavat általában pufferként használják a barna heroin oldhatóságának növelésére. Az egyszer használatos citromsav tasakokat arra ösztönözték, hogy a heroinhasználók kicseréljék piszkos tűiket tiszta tűkre, hogy csökkentsék az AIDS és a hepatitis terjedését. A barna heroinhoz használt egyéb savanyítók az aszkorbinsav, az ecetsav és a tejsav: ezek hiányában a gyógyszer injektor gyakran helyettesíti a citromlevet vagy az ecetet.
A citromsav a HMTD szintéziséhez szükséges vegyi anyagok egyike; az aceton-peroxidhoz (más néven “Sátán anyja”) hasonló hő, súrlódás és sokkérzékeny robbanóanyag. Ennek köszönhetően egyes kormányok nagy mennyiségű citromsavat vásárolhatnak a potenciális terrorista tevékenység mutatójaként.
citromsav is hozzáadható a fagylalthoz, hogy a zsírgömbök elkülönüljenek. A friss citromlé helyett a receptekhez is hozzáadható. A citromsavat a nátrium-hidrogén-karbonáttal együtt számos pezsgőfürdő-képletben alkalmazzák, mind lenyelésre (pl. porok és tabletták), mind személyes ápolásra (pl. fürdősók, fürdőgyöngyök, valamint zsírra jó tisztítási módszer).
ha hajra alkalmazzák, a citromsav megnyitja a kutikulát. Amíg a kutikula nyitva van, lehetővé teszi a tisztítószerek mélyebb behatolását. Ez általában nem ajánlott, ha bármilyen mesterséges hajfestés történik, kivéve, ha próbál csík a szín ki. Használható samponban. A “Sun-In” termékben is használják a haj fehérítésére ugyanezen okból.
a citromsavat a fényképezés során megállófürdőként is használják. A fejlesztő általában lúgos, így egy enyhe sav semlegesíti azt, növelve a stop fürdő hatékonyságát a sima vízhez képest.
biztonságosság
a citromsavat minden nagy nemzeti és nemzetközi élelmiszer-szabályozó ügynökség biztonságosnak ismeri el az élelmiszerekben való felhasználás szempontjából. Ez természetesen jelen van szinte minden életformában, és a felesleges citromsav könnyen metabolizálódik, és eliminálódik a szervezetből.
érdekes, hogy annak ellenére, hogy mindenütt jelen van a szervezetben, ismert, hogy az étrendben a citromsav intoleranciája létezik. Kevés információ áll rendelkezésre, mivel az állapot ritkanak tűnik, de más típusú élelmiszer-intoleranciához hasonlóan gyakran “pszeudo-allergiás” reakcióként írják le.
száraz citromsavval vagy koncentrált oldatokkal való érintkezés bőr-és szemirritációt okozhat, ezért védőruházatot kell viselni ezen anyagok kezelésekor.
rákos állítások
téves jelentések voltak arról, hogy az E330 a rák egyik fő oka. Úgy gondolják, hogy ezt a Krebs szó félreértése és félreértése okozta. Ebben az esetben Sir Hans Adolf Krebsre, a Krebs-ciklus felfedezőjére utal, nem pedig a rák német szavára.
- Garden, J., Roberts, K., Taylor, A., and Robinson, D. (2003). “Az egyszer használatos citromsav tasakok intravénás kábítószer-használóknak történő rendelkezésre bocsátásának értékelése” (pdf). Scottish Center for Infection and Environmental Health.
- http://www.silverprint.co.uk/chem4.html