| Citric acid | |
|---|---|
|
|
| General | |
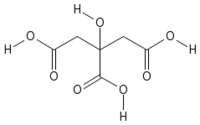
| Systematic name | 2-hydroxypropane- 1,2,3-tricarboxylic acid |
| Empirical formula | C6H8O7 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Molar mass | 192.13 g/mol |
| Appearance | crystalline white solid |
| CAS number | |
| Properties | |
| Density and phase | 1.665 g/cm³ |
| Solubility in water | 133 g/100 ml (20°C) |
| Melting point | 153 °C (307.4F, 426 K) |
| Boiling point | decomposes at 175 °C (448 K) |
| Acidity (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| Hazards | |
| MSDS | External MSDS |
| Main hazards | skin and eye irritant |
| Supplementary data page | |
| Thermodynamic data |
Phase behaviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related compounds | sodium citrate, calcium citrate |
Citric acid is a weak organic acid found in Zitrusfrüchten. Es ist ein natürliches Konservierungsmittel und wird auch verwendet, um Lebensmitteln und alkoholfreien Getränken einen sauren (sauren) Geschmack zu verleihen. In der Biochemie ist es als Zwischenprodukt im Zitronensäurezyklus wichtig und kommt daher im Stoffwechsel fast aller Lebewesen vor. Es dient auch als umweltfreundliches Reinigungsmittel und wirkt als Antioxidans.Zitronensäure kommt in einer Vielzahl von Obst- und Gemüsesorten vor, ist jedoch am stärksten in Zitronen und Limetten konzentriert, wo sie bis zu 8% des Trockengewichts der Früchte ausmachen kann.
Eigenschaften
Bei Raumtemperatur ist Zitronensäure ein weißes kristallines Pulver. Es kann entweder in wasserfreier (wasserfreier) Form oder als Monohydrat vorliegen, das für jedes Molekül Zitronensäure ein Wassermolekül enthält. Die wasserfreie Form kristallisiert aus heißem Wasser, während sich das Monohydrat bildet, wenn Zitronensäure aus kaltem Wasser kristallisiert wird. Das Monohydrat kann durch Erhitzen über 74 °C in die wasserfreie Form überführt werden.
Chemisch teilt Zitronensäure die Eigenschaften anderer Carbonsäuren. Wenn es über 175 Â ° C erhitzt wird, zersetzt es sich durch den Verlust von Kohlendioxid und Wasser.

Geschichte
Die Entdeckung der Zitronensäure wurde dem islamischen Alchemisten Jabir Ibn Hayyan (Geber) aus dem 8. Jahrhundert zugeschrieben. Mittelalterliche Gelehrte in Europa waren sich der sauren Natur von Zitronen- und Limettensäften bewusst; dieses Wissen ist in der Enzyklopädie Speculum Majus (Der Große Spiegel) aus dem 13. Zitronensäure wurde erstmals 1784 vom schwedischen Chemiker Carl Wilhelm Scheele isoliert, der sie aus Zitronensaft kristallisierte. Die Zitronensäureproduktion im industriellen Maßstab begann 1860 auf der Grundlage der italienischen Zitrusfruchtindustrie.
1893 entdeckte C. Wehmer, dass Penicilliumform Zitronensäure aus Zucker herstellen kann. Die mikrobielle Produktion von Zitronensäure wurde jedoch erst industriell wichtig, als der Erste Weltkrieg die italienischen Zitrusexporte störte. Im Jahr 1917 entdeckte der amerikanische Lebensmittelchemiker James Currie, dass bestimmte Stämme des Schimmels Aspergillus niger effiziente Zitronensäureproduzenten sein könnten, und Pfizer begann zwei Jahre später mit der industriellen Produktion mit dieser Technik.
Produktion
Bei dieser Produktionstechnik, die bis heute der wichtigste industrielle Weg zur Zitronensäure ist, werden Kulturen von Aspergillus niger mit Saccharose gefüttert, um Zitronensäure herzustellen. Nach dem Abfiltrieren der Form aus der resultierenden Lösung wird Zitronensäure isoliert, indem man sie mit Kalk (Calciumhydroxid) ausfällt, um Calciumcitratsalz zu erhalten, aus dem Zitronensäure durch Behandlung mit Schwefelsäure regeneriert wird.Alternativ wird Zitronensäure manchmal aus der Fermentationsbrühe durch Extraktion mit einer Kohlenwasserstofflösung der organischen Base Trilaurylamin isoliert, gefolgt von einer erneuten Extraktion aus der organischen Lösung durch Wasser.
Krebszyklus
Zitronensäure gehört zu einer Reihe von Verbindungen, die an der physiologischen Oxidation von Fetten, Proteinen und Kohlenhydraten zu Kohlendioxid und Wasser beteiligt sind.Diese Reihe von chemischen Reaktionen ist von zentraler Bedeutung für fast alle Stoffwechselreaktionen und ist die Quelle von zwei Dritteln der Nahrungsenergie in höheren Organismen. Es wurde von Sir Hans Adolf Krebs entdeckt. Krebs erhielt 1953 den Nobelpreis für Physiologie oder Medizin für die Entdeckung. Die Reihe von Reaktionen ist richtig als Tricarbonsäurezyklus bekannt, aber es ist auch als Zitronensäurezyklus oder Krebszyklus bekannt.
Verwendungen
Lebensmittelzusatzstoff
Als Lebensmittelzusatzstoff wird Zitronensäure als Aroma- und Konservierungsmittel in Lebensmitteln und Getränken, insbesondere alkoholfreien Getränken, verwendet; es wird mit der E-Nummer E330 bezeichnet. Citratsalze verschiedener Metalle werden verwendet, um diese Mineralien in einer biologisch verfügbaren Form in vielen Nahrungsergänzungsmitteln zu liefern. Die puffernden Eigenschaften von Citraten werden zur Kontrolle des pH-Werts in Haushaltsreinigern und Pharmazeutika eingesetzt.
Wasserenthärtung
Die Fähigkeit von Zitronensäure, Metalle zu chelatisieren, macht sie in Seifen und Waschmitteln nützlich. Durch die Chelatisierung der Metalle in hartem Wasser können diese Reiniger Schaum erzeugen und besser arbeiten, ohne dass eine Wasserenthärtung erforderlich ist. In ähnlicher Weise wird Zitronensäure verwendet, um die in Wasserenthärtern verwendeten Ionenaustauschermaterialien zu regenerieren, indem die angesammelten Metallionen als Citratkomplexe abgezogen werden.
Andere
Es wird in der Biotechnologie- und Pharmaindustrie verwendet, um hochreine Prozessleitungen anstelle von Salpetersäure zu passivieren, da Salpetersäure ein gefährliches Entsorgungsproblem darstellt, wenn sie für diesen Zweck verwendet wird, während Zitronensäure dies nicht ist.
Es ist auch der Wirkstoff in einigen Haushaltsreinigungslösungen für Badezimmer und Küchen. Eine Lösung mit einer 6% igen Zitronensäurekonzentration entfernt harte Wasserflecken aus Glas, ohne sie zu schrubben.
Zitronensäure wird üblicherweise als Puffer verwendet, um die Löslichkeit von braunem Heroin zu erhöhen. Einweg-Zitronensäurebeutel wurden als Anreiz verwendet, um Heroinkonsumenten dazu zu bringen, ihre schmutzigen Nadeln gegen saubere Nadeln auszutauschen, um die Ausbreitung von AIDS und Hepatitis zu verringern. Andere für braunes Heroin verwendete Säuerungsmittel sind Ascorbinsäure, Essigsäure und Milchsäure: In ihrer Abwesenheit ersetzt der Arzneimittelinjektor häufig Zitronensaft oder Essig.Zitronensäure ist eine der Chemikalien, die für die Synthese von HMTD benötigt werden; ein sehr hitze-, reibungs- und stoßempfindlicher Sprengstoff ähnlich wie Acetonperoxid (auch bekannt als „Mutter des Satans“). Aus diesem Grund kann der Kauf großer Mengen Zitronensäure von einigen Regierungen als Indikator für potenzielle terroristische Aktivitäten angesehen werden.
Zitronensäure kann auch zu Eiscreme hinzugefügt werden, um Fettkügelchen getrennt zu halten. Es kann auch anstelle von frischem Zitronensaft zu Rezepten hinzugefügt werden. Zitronensäure wird zusammen mit Natriumbicarbonat in einer breiten Palette von Brauseformeln verwendet, sowohl für die Einnahme (z. B. Pulver und Tabletten) als auch für die Körperpflege (z. B. Badesalz, Badekugeln und eine fettarme Reinigungsmethode).
Beim Auftragen auf das Haar öffnet Zitronensäure die Nagelhaut. Während die Nagelhaut offen ist, ermöglicht sie ein tieferes Eindringen der Reinigungsmittel. Es wird im Allgemeinen nicht empfohlen, wenn Sie eine künstliche Haarfärbung durchführen lassen, es sei denn, Sie versuchen, die Farbe zu entfernen. Es kann in Shampoo verwendet werden. Es wird auch in dem Produkt „Sun-In“ verwendet, um Haare aus dem gleichen Grund zu bleichen.
Zitronensäure wird auch als Stoppbad in der Fotografie verwendet. Entwickler ist normalerweise alkalisch, also neutralisiert eine milde Säure es und erhöht die Wirksamkeit des Stoppbades, wenn sie mit normalem Wasser verglichen wird.
Sicherheit
Zitronensäure ist von allen wichtigen nationalen und internationalen Lebensmittelbehörden als sicher für die Verwendung in Lebensmitteln anerkannt. Es ist natürlich in fast allen Lebensformen vorhanden, und überschüssige Zitronensäure wird leicht metabolisiert und aus dem Körper ausgeschieden.
Interessanterweise ist trotz seiner Allgegenwart im Körper eine Intoleranz gegenüber Zitronensäure in der Nahrung bekannt. Es liegen nur wenige Informationen vor, da der Zustand selten zu sein scheint, aber wie andere Arten von Nahrungsmittelunverträglichkeiten wird er oft als „pseudoallergische“ Reaktion beschrieben.
Kontakt mit trockener Zitronensäure oder mit konzentrierten Lösungen kann zu Haut- und Augenreizungen führen, daher sollte beim Umgang mit diesen Materialien Schutzkleidung getragen werden.
Krebsbehauptungen
Es gab fehlerhafte Berichte, dass E330 eine Hauptursache für Krebs ist. Es wird vermutet, dass dies durch Missverständnisse und Verwirrung über das Wort Krebs verursacht wurde. In diesem Fall bezieht es sich auf Sir Hans Adolf Krebs, Entdecker des Krebs-Zyklus, und nicht auf das deutsche Wort für Krebs.
- Garden, J., Roberts, K., Taylor, A. und Robinson, D. (2003). „Bewertung der Bereitstellung von Zitronensäuresäckchen zum einmaligen Gebrauch für injizierende Drogenkonsumenten“ (pdf). Schottisches Zentrum für Infektion und Umweltgesundheit.
- http://www.silverprint.co.uk/chem4.html