| Citric acid | |
|---|---|
|
|
| General | |
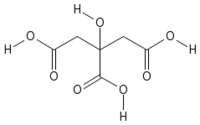
| Systematic name | 2-hydroxypropane- 1,2,3-tricarboxylic acid |
| Empirical formula | C6H8O7 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Molar mass | 192.13 g/mol |
| Appearance | crystalline white solid |
| CAS number | |
| Properties | |
| Density and phase | 1.665 g/cm³ |
| Solubility in water | 133 g/100 ml (20°C) |
| Melting point | 153 °C (307.4F, 426 K) |
| Boiling point | decomposes at 175 °C (448 K) |
| Acidity (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| Hazards | |
| MSDS | External MSDS |
| Main hazards | skin and eye irritant |
| Supplementary data page | |
| Thermodynamic data |
Phase behaviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related compounds | sodium citrate, calcium citrate |
Citric acid is a weak organic acid found i citrusfrugter. Det er et naturligt konserveringsmiddel og bruges også til at tilføje en sur (sur) smag til mad og læskedrikke. I biokemi er det vigtigt som et mellemprodukt i citronsyrecyklussen og forekommer derfor i metabolismen af næsten alle levende ting. Det fungerer også som et miljøvenligt rengøringsmiddel og fungerer som et antioksidant middel.citronsyre findes i en række frugter og grøntsager, men den er mest koncentreret i citroner og limefrugter, hvor den kan udgøre så meget som 8% af frugtens tørvægt.
egenskaber
ved stuetemperatur er citronsyre et hvidt krystallinsk pulver. Det kan eksistere enten i en vandfri (vandfri) form eller som et monohydrat, der indeholder et vandmolekyle for hvert molekyle citronsyre. Den vandfri form krystalliserer fra varmt vand, mens monohydratet dannes, når citronsyre krystalliseres fra koldt vand. Monohydratet kan omdannes til vandfri form ved at opvarme det over 74 liter C.
kemisk deler citronsyre egenskaberne af andre carboksyl syrer. Når det opvarmes over 175 liter C, nedbrydes det gennem tab af kulsyre og vand.

historie
opdagelsen af citronsyre er blevet krediteret det 8.århundrede islamiske alkymist Jabir Ibn Hayyan (Geber). Middelalderlige lærde i Europa var opmærksomme på den sure natur af citron-og limejuice; sådan viden er optaget i det 13.århundrede encyclopedia Speculum Majus (det store spejl), udarbejdet af Vincent af Beauvais. Citronsyre blev først isoleret i 1784 af den svenske kemiker Carl Vilhelm Scheele, der krystalliserede den fra citronsaft. Industriel skala citronsyreproduktion begyndte i 1860, baseret på den italienske citrusfrugtindustri.
i 1893 opdagede C. Vehmer, at Penicillium skimmel kunne producere citronsyre fra sukker. Imidlertid blev mikrobiel produktion af citronsyre ikke industrielt vigtig, før Første Verdenskrig forstyrrede italiensk citruseksport. I 1917 opdagede den amerikanske fødevarekemiker James Currie, at visse stammer af formen Aspergillus niger kunne være effektive citronsyreproducenter.
produktion
i denne produktionsteknik, som stadig er den største industrielle vej til citronsyre, der anvendes i dag, fodres kulturer af Aspergillus niger med saccharose for at producere citronsyre. Efter at formen er filtreret ud af den resulterende opløsning, isoleres citronsyre ved udfældning med kalk (calciumhydroksid) for at give calciumcitratsalt, hvorfra citronsyre regenereres ved behandling med svovlsyre.
alternativt isoleres citronsyre undertiden fra fermenteringsbuljongen ved ekstraktion med en carbonhydridopløsning af den organiske base trilaurylamin efterfulgt af reekstraktion fra den organiske opløsning med vand.
Krebs cyklus
citronsyre er en af en række forbindelser involveret i fysiologisk iltning af fedt, proteiner og kulhydrater til kulsyre og vand.
denne serie af kemiske reaktioner er central for næsten alle metaboliske reaktioner og er kilden til to tredjedele af den fødevareafledte energi i højere organismer. Det blev opdaget af Sir Hans Adolf Krebs. Krebs modtog Nobelprisen i fysiologi eller medicin i 1953 for opdagelsen. Det er også kendt som citronsyrecyklus eller Krebs-cyklus.
bruger
fødevaretilsætningsstof
som fødevaretilsætningsstof anvendes citronsyre som smags-og konserveringsmiddel i fødevarer og drikkevarer, især læskedrikke; det betegnes med E-nummer E330. Citratsalte af forskellige metaller bruges til at levere disse mineraler i en biologisk tilgængelig form i mange kosttilskud. Bufferingsegenskaberne af citrater bruges til at kontrollere pH i husholdningsrengøringsmidler og lægemidler.
vandblødgøring
Citronsyres evne til at chelatere metaller gør det nyttigt i sæber og vaskemidler. Ved at chelatere metallerne i hårdt vand lader det disse rengøringsmidler producere skum og arbejde bedre uden behov for vandblødgøring. Tilsvarende anvendes citronsyre til at regenerere ionbytningsmaterialerne, der anvendes i vandblødgørere ved at fjerne de akkumulerede metalioner som citratkomplekser.
andre
det bruges i bioteknologi og farmaceutisk industri til at passivere procesrør med høj renhed i stedet for at bruge salpetersyre, da salpetersyre er et farligt bortskaffelsesproblem, når det først er brugt til dette formål, mens citronsyre ikke er det.
det er også den aktive ingrediens i nogle husholdningsrengøringsløsninger til badeværelser og køkkener. En opløsning med en 6% koncentration af citronsyre fjerner hårde vandpletter fra glas uden skrubning.
citronsyre anvendes almindeligvis som en buffer for at øge opløseligheden af brun heroin. Engangs citronsyreposer er blevet brugt som en tilskyndelse til at få heroinbrugere til at udveksle deres beskidte nåle med rene nåle i et forsøg på at mindske spredningen af AIDS og hepatitis. Andre forsurere, der anvendes til brun heroin, er ascorbinsyre, eddikesyre og mælkesyre: i deres fravær vil lægemiddelinjektoren ofte erstatte citronsaft eller eddike.
citronsyre er et af de kemikalier, der kræves til syntese af HMTD; et meget varme -, friktions-og stødfølsomt eksplosivstof svarende til Acetonoverilte (også kendt som “Satans Mor”). På grund af dette kan køb af store mængder citronsyre ses af nogle regeringer som en indikator for potentiel terroraktivitet.
citronsyre kan også tilsættes til is for at holde fedtkugler adskilt. Det kan også føjes til opskrifter i stedet for frisk citronsaft. Citronsyre anvendes sammen med natriumbicarbonat i en lang række brusende formler, både til indtagelse (f.eks. pulvere og tabletter) og til personlig pleje (f. eks. badesalte, badperler og en rengøringsmetode, der er god på fedt).
når der påføres hår, åbner citronsyre kutiklen. Mens neglebåndet er åbent, giver det mulighed for dybere penetration af rengøringsmidlerne. Det er generelt ikke anbefales, hvis du har nogen kunstig hår farve gjort, medmindre du forsøger at fratage farven ud. Det kan bruges i shampoo. Det bruges også i produktet “Sun-In” til at blegge hår af samme grund.
citronsyre bruges også som stopbad i fotografering. Udvikler er normalt alkalisk, så en mild syre vil neutralisere det, hvilket øger effektiviteten af stopbadet sammenlignet med almindeligt vand.
sikkerhed
citronsyre er anerkendt som sikkert til brug i fødevarer af alle større nationale og internationale fødevaremyndigheder. Det er naturligt til stede i næsten alle former for liv, og overskydende citronsyre metaboliseres let og elimineres fra kroppen.
interessant, på trods af dets allestedsnærværende i kroppen, er intolerance over for citronsyre i kosten kendt for at eksistere. Lidt information er tilgængelig, da tilstanden ser ud til at være sjælden, men som andre typer fødeintolerance beskrives den ofte som en “pseudo-allergisk” reaktion.
kontakt med tør citronsyre eller med koncentrerede opløsninger kan resultere i hud-og øjenirritation, så beskyttelsesbeklædning skal bæres ved håndtering af disse materialer.
kræftkrav
der har været fejlagtige rapporter om, at E330 er en væsentlig årsag til kræft. Det menes, at dette er forårsaget af misforståelse og forvirring over ordet Krebs. I dette tilfælde henviser det til Sir Hans Adolf Krebs, opdageren af Krebs-cyklussen, og ikke det tyske ord for kræft.
- have, J., Roberts, K., Taylor, A. og Robinson, D. (2003). “Evaluering af levering af Citronsyreposer til engangsbrug til injektion af stofbrugere” (pdf). Scottish Center for infektion og Environmental Health.
- http://www.silverprint.co.uk/chem4.html