| Citric acid | |
|---|---|
|
|
| General | |
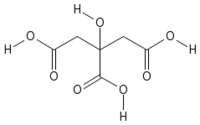
| Systematic name | 2-hydroxypropane- 1,2,3-tricarboxylic acid |
| Empirical formula | C6H8O7 |
| SMILES | C(C(=O)O)C(CC(=O)O)(C(=O)O)O |
| Molar mass | 192.13 g/mol |
| Appearance | crystalline white solid |
| CAS number | |
| Properties | |
| Density and phase | 1.665 g/cm³ |
| Solubility in water | 133 g/100 ml (20°C) |
| Melting point | 153 °C (307.4F, 426 K) |
| Boiling point | decomposes at 175 °C (448 K) |
| Acidity (pKa) | pKa1=3.15 pKa2=4.77 pKa3=6.40 |
| Hazards | |
| MSDS | External MSDS |
| Main hazards | skin and eye irritant |
| Supplementary data page | |
| Thermodynamic data |
Phase behaviour Solid, liquid, gas |
| Spectral data | UV, IR, NMR, MS |
| Related compounds | |
| Related compounds | sodium citrate, calcium citrate |
Citric acid is a weak organic acid found v citrusových plodech. Je to přírodní konzervační látka a používá se také k přidání kyselé (kyselé) chuti do potravin a nealkoholických nápojů. V biochemii je důležitý jako meziprodukt v cyklu kyseliny citronové, a proto se vyskytuje v metabolismu téměř všech živých věcí. Slouží také jako ekologicky šetrný čisticí prostředek a působí jako antioxidant.
kyselina citronová existuje v různých druzích ovoce a zeleniny, ale je nejvíce koncentrovaná v citronech a limetkách, kde může obsahovat až 8% suché hmotnosti ovoce.
vlastnosti
při pokojové teplotě je kyselina citronová bílý krystalický prášek. Může existovat buď v bezvodé (bezvodé) formě, nebo jako monohydrát, který obsahuje jednu molekulu vody pro každou molekulu kyseliny citronové. Bezvodá forma krystalizuje z horké vody, zatímco monohydrát se tvoří, když kyselina citronová krystalizuje ze studené vody. Monohydrát může být přeměněn na bezvodou formu zahřátím nad 74°C.
chemicky sdílí kyselina citronová vlastnosti jiných karboxylových kyselin. Při zahřátí nad 175°C se rozkládá ztrátou oxidu uhličitého a vody.

Historie
objev kyseliny citronové byla připsána do 8. století Islámský alchymista Jabir Ibn Hayyan (Geber). Středověcí učenci v Evropě si byli vědomi kyselé povahy citronové a limetkové šťávy; takové znalosti jsou zaznamenány v encyklopedii Speculum Majus ze 13. století (velké zrcadlo), kterou sestavil Vincent z Beauvais. Kyselina citronová byla poprvé izolována v roce 1784 švédským chemikem Carlem Wilhelmem Scheelem, který ji krystalizoval z citronové šťávy. Výroba kyseliny citronové v průmyslovém měřítku začala v roce 1860 na základě italského průmyslu citrusových plodů.
v roce 1893 C. Wehmer zjistil, že forma Penicillium může produkovat kyselinu citronovou z cukru. Mikrobiální produkce kyseliny citronové se však průmyslově nestala důležitou, dokud první světová válka nenarušila vývoz italských citrusů. V roce 1917, Americký potravinářský chemik James Currie zjistil, že některé kmeny plísní Aspergillus niger může být efektivní výrobců kyseliny citronové, a Pfizer začala průmyslová produkce na úrovni použití této techniky o dva roky později.
Výroba
V této výrobní technika, která je stále hlavní průmyslové trasy, aby se kyselina citronová používá dnes, kultury Aspergillus niger jsou krmena sacharózou, aby produkovat kyselinu citronovou. Po odfiltrování formy z výsledného roztoku se kyselina citronová izoluje vysrážením vápnem (hydroxidem vápenatým) za vzniku soli citrátu vápenatého, ze které se kyselina citronová regeneruje zpracováním kyselinou sírovou.
Případně, kyselina citronová je někdy izolované z kvašení vývar extrakcí s uhlovodíkové řešení ekologické základny trilaurylamine, následuje re-extrakce z organických roztok do vody.
Krebsův cyklus
kyselina citronová je jednou z řady sloučenin podílejících se na fyziologické oxidaci tuků, bílkovin a sacharidů na oxid uhličitý a vodu.
tato řada chemických reakcí je ústředním bodem téměř všech metabolických reakcí a je zdrojem dvou třetin energie získané z potravy ve vyšších organismech. Objevil ji Sir Hans Adolf Krebs. Krebs obdržel za objev roku 1953 Nobelovu cenu za fyziologii nebo medicínu. Série reakcí je správně známá jako cyklus kyseliny trikarboxylové, ale je také známá jako cyklus kyseliny citronové nebo Krebsův cyklus.
používá
potravinářská přídatná látka
jako potravinářská přídatná látka se kyselina citronová používá jako aromatická a konzervační látka v potravinách a nápojích, zejména nealkoholických nápojích; označuje se číslem E E330. Citrátové soli různých kovů se používají k dodávání těchto minerálů v biologicky dostupné formě v mnoha doplňcích stravy. Pufrovací vlastnosti citrátů se používají k regulaci pH v domácích čisticích prostředcích a léčivech.
změkčení vody
schopnost kyseliny citronové chelatovat kovy je užitečná v mýdlech a pracích prostředcích. Chelatací kovů v tvrdé vodě umožňuje těmto čisticím prostředkům vyrábět pěnu a pracovat lépe bez nutnosti změkčování vody. Podobně se kyselina citronová používá k regeneraci iontoměničových materiálů používaných ve změkčovadlech vody odstraňováním nahromaděných kovových iontů jako citrátových komplexů.
Ostatní
používá se v biotechnologii a farmaceutickém průmyslu k pasivaci vysoká čistota procesu potrubí namísto použití kyseliny dusičné, protože kyselina dusičná je nebezpečná likvidaci problém, jakmile je použit pro tento účel, zatímco kyselina citronová není.
je také aktivní složkou v některých domácích čisticích prostředcích pro koupelny a kuchyně. Roztok s 6% koncentrací kyseliny citronové odstraní skvrny tvrdé vody ze skla bez drhnutí.kyselina citronová se běžně používá jako pufr ke zvýšení rozpustnosti hnědého heroinu. Na jedno použití kyseliny citrónové sáčky byly použity jako pobídka, aby si uživatelé heroinu, aby si vyměnili své špinavé jehly za čisté jehly ve snaze snížit šíření AIDS a hepatitidy. Další okyselující používá v případě hnědého heroinu jsou kyselina askorbová, kyselina octová a kyselina mléčná: v jejich nepřítomnosti, lék vstřikovače se často nahradit citronovou šťávou nebo octem.
kyselina citronová je jednou z chemikálií potřebných pro syntézu HMTD; výbušnina citlivá na teplo, tření a šok podobná peroxidu acetonu (také známá jako „matka Satana“). Z tohoto důvodu může být nákup velkého množství kyseliny citronové některými vládami považován za ukazatel potenciální teroristické aktivity.
kyselina citronová může být také přidána do zmrzliny, aby se tukové kuličky oddělily. Může být přidán do receptů místo čerstvé citronové šťávy. Kyselina citronová se používá spolu s hydrogenuhličitan sodný v široké škále šumivé vzorců, a to jak pro požití (např. prášky a tablety) a pro osobní péči (např. koupelové soli, koupelové kuličky a čištění metoda dobrá na tuk).
při aplikaci na vlasy kyselina citronová otevírá kůžičku. Zatímco pokožka je otevřená, umožňuje hlubší pronikání čisticích prostředků. Obecně se nedoporučuje, pokud máte nějaké umělé barvení vlasů, pokud se nesnažíte barvu odstranit. Může být použit v šamponu. Používá se také v produktu „Sun-In“ k bělení vlasů ze stejného důvodu.
kyselina citronová se také používá jako zastavovací lázeň při fotografování. Vývojář je obvykle zásaditý, takže mírná kyselina ji neutralizuje, což zvyšuje účinnost zastavovací lázně ve srovnání s čistou vodou.
bezpečnost
kyselina citronová je uznávána jako bezpečná pro použití v potravinách všemi hlavními národními a mezinárodními regulačními agenturami pro potraviny. Je přirozeně přítomen téměř ve všech formách života a přebytečná kyselina citronová se snadno metabolizuje a vylučuje z těla.
je zajímavé, že navzdory své všudypřítomnosti v těle je známo, že existuje nesnášenlivost kyseliny citronové ve stravě. Málo informací je k dispozici jako podmínka se zdá být vzácné, ale podobně jako jiné typy potravinové intolerance je často popisován jako „pseudo-alergické“ reakce.
kontakt se suchou kyselinou citronovou nebo s koncentrovanými roztoky může vést k podráždění kůže a očí, proto je třeba při manipulaci s těmito materiály nosit ochranný oděv.
tvrzení o rakovině
byly chybné zprávy, že E330 je hlavní příčinou rakoviny. Předpokládá se, že to bylo způsobeno nedorozuměním a zmatkem nad slovem Krebs. V tomto případě se odkazuje na sira Hanse Adolfa Krebse, objevitele Krebsova cyklu, a nikoli na německé slovo pro rakovinu.
- Garden, J., Roberts, k., Taylor, A., and Robinson, D. (2003). „Hodnocení poskytování sáčků s kyselinou citronovou na jedno použití injekčním uživatelům drog „(pdf). Skotské Centrum pro infekce a zdraví životního prostředí.
- http://www.silverprint.co.uk/chem4.html