nume Generic: fluocinonida
forma de dozare: unguent
Medical revizuite de Drugs.com. Ultima actualizare pe 22 decembrie 2020.
- Prezentare generală
- efecte secundare
- dozare
- Professional
- interacțiuni
- mai mult
numai Rx
numele mărcii Lidex a fost întrerupt în SUA dacă versiunile generice ale acestui produs au fost aprobate de FDA, pot exista echivalente generice disponibile.
Lidex descriere
Lidex (fluocinonidă) unguent 0,05% este destinat administrării topice. Componenta activă este fluocinonida corticosteroidă, care este esterul 21-acetat al acetonidei de fluocinolonă și are denumirea chimică pregna-1,4-dien-3,20-dionă,21-(acetiloxi)-6,9-difluoro-11-hidroxi-16,17–,(6. Are următoarea structură chimică:
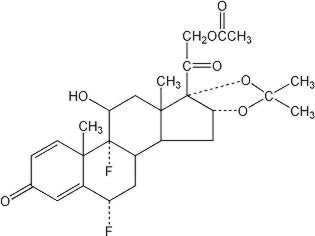
Lidex unguent conține fluocinonidă 0.5 mg / g într-o bază de unguent special formulată constând din monostearat de gliceril, petrolatum alb, carbonat de propilen, propilen glicol și ceară albă. Oferă efectele ocluzive și emoliente dorite într-un unguent.
în această formulare, ingredientul activ este în totalitate în soluție.
Lidex – Farmacologie Clinică
corticosteroizii topici au acțiuni antiinflamatorii, anti-pruritice și vasoconstrictive.mecanismul activității antiinflamatorii a corticosteroizilor topici este neclar. Diferite metode de laborator, inclusiv testele vasoconstrictoare, sunt utilizate pentru a compara și prezice potențele și/sau eficacitatea clinică a corticosteroizilor topici. Există unele dovezi care sugerează că există o corelație recunoscută între potența vasoconstrictorului și eficacitatea terapeutică la om.
farmacocinetica
gradul de absorbție percutanată a corticosteroizilor topici este determinat de mulți factori, inclusiv vehiculul, integritatea barierei epidermice și utilizarea pansamentelor ocluzive.
corticosteroizii topici pot fi absorbiți de pe pielea intactă normală. Inflamația și / sau alte procese de boală la nivelul pielii cresc absorbția percutanată. Pansamentele ocluzive cresc substanțial absorbția percutanată a corticosteroizilor topici. Astfel, pansamentele ocluzive pot fi un adjuvant terapeutic valoros pentru tratamentul dermatozelor rezistente (vezi dozare și administrare).
odată absorbiți prin piele, corticosteroizii topici sunt manipulați prin căi farmacocinetice similare corticosteroizilor administrați sistemic. Corticosteroizii sunt legați de proteinele plasmatice în grade diferite. Corticosteroizii sunt metabolizați în principal în ficat și sunt apoi excretați de rinichi. Unii dintre corticosteroizii topici și metaboliții lor sunt, de asemenea, excretați în bilă.
indicații și utilizare pentru Lidex
unguentul Lidex este indicat pentru ameliorarea manifestărilor inflamatorii și pruriginoase ale dermatozelor receptive la corticosteroizi.
contraindicații
corticosteroizii topici sunt contraindicați la acei pacienți cu antecedente de hipersensibilitate la oricare dintre componentele preparatului.
Precauții
General
absorbția sistemică a corticosteroizilor topici a produs suprimarea reversibilă a axei hipotalamo-hipofizo-suprarenale (HPA), manifestări ale sindromului Cushing, hiperglicemie și glucozurie la unii pacienți.
condițiile care sporesc absorbția sistemică includ aplicarea steroizilor mai puternici, utilizarea pe suprafețe mari, utilizarea prelungită și adăugarea de pansamente ocluzive.
prin urmare, pacienții cărora li se administrează o doză mare de steroid topic puternic aplicat pe o suprafață mare sau sub un pansament ocluziv trebuie evaluați periodic pentru evidențierea suprimării axei HPA prin utilizarea testelor de cortizol liber urinar și de stimulare a ACTH. Dacă se observă suprimarea axei HPA, trebuie făcută o încercare de a retrage medicamentul, de a reduce frecvența aplicării sau de a înlocui un steroid mai puțin puternic.
recuperarea funcției axei HPA este în general promptă și completă la întreruperea medicamentului. Rareori, pot apărea semne și simptome de retragere a steroizilor, necesitând corticosteroizi sistemici suplimentari.
copiii pot absorbi cantități proporțional mai mari de corticosteroizi topici și astfel pot fi mai susceptibili la toxicitate sistemică (vezi precauții – utilizare pediatrică). Dacă apare iritație, corticosteroizii topici trebuie întrerupți și trebuie instituit un tratament adecvat.
ca în cazul oricărui produs corticosteroid topic, utilizarea prelungită poate produce atrofie a pielii și a țesuturilor subcutanate. Atunci când este utilizat pe zone intertriginoase sau Flexoare sau pe față, acest lucru poate apărea chiar și în cazul utilizării pe termen scurt.
în prezența infecțiilor dermatologice, trebuie instituită utilizarea unui agent antifungic sau antibacterian adecvat. Dacă un răspuns favorabil nu apare prompt, corticosteroidul trebuie întrerupt până când infecția a fost controlată în mod adecvat.
informații pentru pacient
pacienții care utilizează corticosteroizi topici trebuie să primească următoarele informații și instrucțiuni:
- acest medicament trebuie utilizat conform indicațiilor medicului. Este doar pentru uz extern. Evitați contactul cu ochii.
- pacienții trebuie sfătuiți să nu utilizeze acest medicament pentru alte afecțiuni decât cea pentru care a fost prescris.
- zona tratată a pielii nu trebuie bandajată sau acoperită sau învelită în alt mod pentru a fi ocluzivă, cu excepția cazului în care medicul recomandă acest lucru.
- pacienții trebuie să raporteze orice semne de reacții adverse locale, în special sub pansament ocluziv.
- părinții pacienților pediatrici trebuie sfătuiți să nu folosească scutece sau pantaloni de plastic pe un copil tratat în zona scutecului, deoarece aceste articole de îmbrăcăminte pot constitui pansamente ocluzive.
teste de laborator
următoarele teste pot fi utile în evaluarea suprimării axei HPA:
testul cortizolului liber urinar
testul de stimulare a ACTH
carcinogeneza, mutageneza și afectarea fertilității
nu s-au efectuat studii pe termen lung la animale pentru a evalua potențialul carcinogen sau efectul corticosteroizilor topici asupra fertilității.
studiile pentru determinarea mutagenității cu prednisolon și hidrocortizon au evidențiat rezultate negative.
sarcina categoria C
corticosteroizii sunt în general teratogeni la animalele de laborator atunci când sunt administrați sistemic la doze relativ mici. Corticosteroizii mai puternici s-au dovedit a fi teratogeni după aplicarea cutanată la animalele de laborator. Nu există studii adecvate și bine controlate la femeile gravide privind efectele teratogene ale corticosteroizilor aplicați local. Prin urmare, corticosteroizii topici trebuie utilizați în timpul sarcinii numai dacă beneficiul potențial justifică riscul potențial pentru făt. Medicamentele din această clasă nu trebuie utilizate pe scară largă la pacienții gravide, în cantități mari sau pentru perioade prelungite de timp.
mamele care alăptează
nu se cunoaște dacă administrarea topică de corticosteroizi poate avea ca rezultat o absorbție sistemică suficientă pentru a produce cantități detectabile în laptele matern. Corticosteroizii administrați sistemic sunt secretați în laptele matern în cantități care nu pot avea un efect dăunător asupra sugarului. Cu toate acestea, se recomandă prudență atunci când corticosteroizii topici sunt administrați unei femei care alăptează.
utilizare pediatrică
pacienții pediatrici pot demonstra o susceptibilitate mai mare la supresia axei hipotalmic-hipofizo-suprarenale (HPA) indusă de corticosteroizi topici și sindromul Cushing decât pacienții maturi din cauza unui raport mai mare al suprafeței pielii la greutatea corporală.
suprimarea axei HPA, sindromul Cushing și hipertensiunea intracraniană au fost raportate la copiii cărora li s-au administrat corticosteroizi topici. Manifestările supresiei suprarenale la copii includ întârzierea creșterii liniare, creșterea în greutate întârziată, nivelurile scăzute de cortizol plasmatic și absența răspunsului la stimularea ACTH. Manifestările hipertensiunii intracraniene includ fontanele bombate, durerile de cap și papilema bilaterală.
administrarea corticosteroizilor topici la copii trebuie limitată la cea mai mică cantitate compatibilă cu un regim terapeutic eficient. Terapia cronică cu corticosteroizi poate interfera cu creșterea și dezvoltarea copiilor.
reacții Adverse
următoarele reacții adverse locale sunt raportate rar la corticosteroizi topici, dar pot apărea mai frecvent la utilizarea pansamentelor ocluzive. Aceste reacții sunt enumerate într-o ordine descrescătoare aproximativă de apariție:
| Burning | Perioral dermatitis |
| Itching | Allergic contact dermatitis |
| Irritation | Maceration of the skin |
| Dryness | Secondary infection |
| Folliculitis | Skin atrophy |
| Hypertrichosis | Striae |
| Acneiform eruptions | Miliaria |
| Hypopigmentation |
Overdosage
Topically applied corticosteroids can be absorbed in sufficient amounts to produce systemic effects (see PRECAUTIONS).
dozare și Administrare Lidex
unguentul Lidex se aplică în general pe zona afectată sub formă de film subțire de două până la patru ori pe zi, în funcție de gravitatea afecțiunii.
pansamentele ocluzive pot fi utilizate pentru gestionarea psoriazisului sau a afecțiunilor recalcitrante.
dacă apare o infecție, utilizarea pansamentelor ocluzive trebuie întreruptă și trebuie instituită o terapie antimicrobiană adecvată.
cum se administrează Lidex
Lidex (fluocinonidă) unguent 0.05% este furnizat în
15 g tub –NDC 99207-514-13
30 g tub –NDC 99207-514-14
60 g tub –NDC 99207-514-17
120 g tub –NDC 99207-514-22
A se păstra la temperatura camerei. Se va evita temperatura peste 30 de grade C (86 de grade F).
U. s. Patent No 4,017,615
Fabricat pentru:
MEDICIS, La Dermatologie Compania®
Scottsdale, AZ 85258
de: Patheon, Inc.
Mississauga, Ontario
Canada L5N 7K9
IN-5070/S
| Lidex fluocinonide ointment |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Labeler – MEDICIS
Frequently asked questions
- Is it used for hair loss?
- What is a substitute for fluocinonide cream?
- Is fluocinonide an antifungal cream?
- How long should you use fluocinonide for?
- What is fluocinonide cream good for?
- fluocinonida poate fi utilizată pentru a trata o erupție de iederă otrăvitoare?
- este un steroid?
- este un antibiotic?
mai multe despre Lidex (fluocinonidă topică)
- efecte secundare
- în timpul sarcinii sau alăptării
- informații privind dozajul
- interacțiuni medicamentoase
- 8 recenzii
- disponibilitate generică
- clasa de medicamente: steroizi topici
resurse pentru consumatori
- citire avansată
- Lidex ușoară (citire avansată)
- Lidex Regular (citire avansată)
resurse profesionale
- informații de prescriere
- soluție topică Lidex (FDA)
- Gel Lidex (FDA)
Alte mărci Vanos, lidex-e
ghiduri de tratament înrudite
- dermatită atopică
- eczemă
- dermatită
- psoriazis
Disclaimer medical