adăugarea hidrogenului la o dublă legătură carbon-carbon se numește hidrogenare. Efectul general al unei astfel de adăugiri este eliminarea reductivă a grupului funcțional cu dublă legătură. Regioselectivitatea nu este o problemă, deoarece același grup (un atom de hidrogen) este legat de fiecare dintre carbonii cu dublă legătură. Cea mai simplă sursă de doi atomi de hidrogen este hidrogenul molecular (H2), dar amestecarea alchenelor cu hidrogenul nu are ca rezultat nicio reacție perceptibilă. Deși reacția generală de hidrogenare este exotermă, o energie de activare ridicată o împiedică să aibă loc în condiții normale. Această restricție poate fi eludată prin utilizarea unui catalizator, după cum se arată în diagrama următoare.
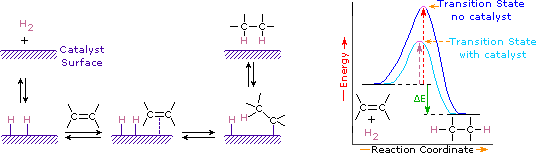
catalizatorii sunt substanțe care modifică viteza (viteza) unei reacții chimice fără a fi consumate sau care apar ca parte a produsului. Catalizatorii acționează prin scăderea energiei de activare a reacțiilor, dar nu modifică energia potențială relativă a reactanților și a produselor. Metalele fin divizate, cum ar fi platina, paladiul și nichelul, sunt printre cei mai utilizați catalizatori de hidrogenare. Hidrogenarea catalitică are loc în cel puțin două etape, așa cum este descris în diagramă. În primul rând, alchena trebuie adsorbită pe suprafața catalizatorului împreună cu o parte din hidrogen. Apoi, doi hidrogeni se deplasează de la suprafața metalică la carbonii dublei legături, iar hidrocarbura saturată rezultată, care este mai slab adsorbită, părăsește suprafața catalizatorului. Natura exactă și calendarul ultimelor evenimente nu sunt bine înțelese.
după cum se arată în diagrama energetică, hidrogenarea alchenelor este exotermă, iar căldura este eliberată corespunzător cu OQUSTE (verde colorat) din diagramă. Această căldură de reacție poate fi utilizată pentru a evalua stabilitatea termodinamică a alchenelor având un număr diferit de substituenți alchilici pe dubla legătură. De exemplu, următorul tabel listează căldurile de hidrogenare pentru trei alchene C5H10 care dau același produs alcanic (2-metilbutan). Deoarece o căldură mare de reacție indică un reactant cu energie ridicată, aceste călduri sunt invers proporționale cu stabilitatea izomerilor alchenei. Pentru o aproximare aproximativă, vedem că fiecare substituent alchil pe o legătură dublă stabilizează această grupă funcțională cu puțin mai mult de 1 kcal/mol.
| izomer alchenă | (CH3)2CHCH=CH2 3-metil-1-butenă |
CH2=C(CH3)ch2ch3 2-metil-1-butenă |
(CH3)2C=chch3 2-metil-2-butenă |
|---|---|---|---|
| căldură de reacție ( inkth inkt ) |
-30,3 kcal/mol | -28,5 kcal/mol | -26,9 kcal/mol |
din mecanismul prezentat aici ne-am aștepta ca adăugarea de hidrogen să aibă loc cu syn-STEREOSELECTIVITATE. Acest lucru este adesea adevărat, dar catalizatorii de hidrogenare pot provoca, de asemenea, izomerizarea dublei legături înainte de adăugarea de hidrogen, caz în care stereoselectivitatea poate fi incertă.formarea complexelor metalice de tranziție cu alchene a fost demonstrată convingător prin izolarea complexelor stabile de platină, cum ar fi sarea lui Zeise, K. H2O și etilenebis(trifenilfosfină)platină, 2pt(H2C=CH2). În acesta din urmă, platina este cu trei coordonate și zero-valent, în timp ce sarea lui Zeise este un derivat al platinei(II). Un model al sării lui Zeise și o discuție despre legătura neobișnuită în astfel de complexe pot fi vizualizate făcând clic aici. Complexe similare au fost raportate pentru nichel și paladiu, metale care funcționează și ca catalizatori pentru hidrogenarea alchenei.
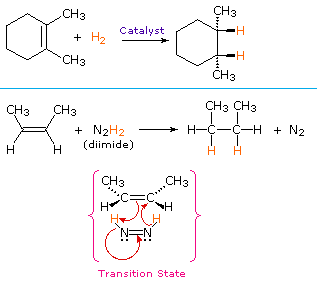
o procedură necatalitică pentru adăugarea de hidrogen face uz de diimida compusului instabil, N2H2. Acest reactiv trebuie să fie proaspăt generat în sistemul de reacție, de obicei prin oxidarea hidrazinei, iar reacția puternic exotermă este favorizată de eliminarea azotului gazos (un compus foarte stabil). Diimida poate exista ca izomeri cis-trans; numai izomerul cis servește ca agent reducător. Exemple de reduceri ale alchenei prin ambele proceduri sunt prezentate mai jos.
Contributors
- William Reusch, Profesor Emerit (Michigan State U.), manual Virtual de Chimie Organică