proprietățile compușilor covalenți
când am vorbit despre compușii ionici solizi din compușii ionici, am constatat că proprietățile lor derivă adesea din atracția puternică a sarcinilor electrice opuse. Nu ar trebui să fie o surpriză să constatăm că proprietățile compușilor covalenți se datorează în mare parte naturii legăturilor covalente.
unul dintre cele mai importante lucruri de reținut despre compușii covalenți este că nu sunt ionici. Acest lucru pare evident, dar diferența este de fapt mai subtilă decât vă puteți imagina. Pentru a ilustra acest concept, aruncați o privire la următoarea figură:
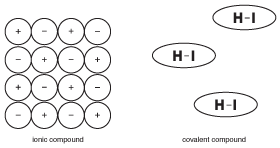
figura 9.5 proprietățile compușilor ionici solizi se bazează pe faptul că mulți ioni sunt ținuți rigid în poziție cu forțe electrice. Cu toate acestea, moleculele din compușii covalenți funcționează cu relativă independență față de moleculele vecine.
spre deosebire de compușii ionici, unde toți ionii dintr-un cristal mare ajută la menținerea reciprocă, moleculele dintr-un compus covalent sunt ținute împreună de forțe numite „forțe intermoleculare”, care sunt mult mai slabe decât legăturile chimice (mai multe despre forțele intermoleculare din solide). Ca urmare, moleculele dintr-un compus covalent nu sunt atrase una de cealaltă la fel de mult ca ionii din compușii ionici. Această diferență de structură este importantă în înțelegerea proprietăților compușilor covalenți.
compușii covalenți au puncte de topire și fierbere scăzute
după cum se menționează în compușii ionici, este necesară o cantitate mare de energie pentru a topi un compus ionic din cauza interacțiunilor puternice dintre cationi și anioni într-un cristal ionic. Cu toate acestea, în compușii covalenți, toate moleculele sunt legate doar slab de moleculele vecine; prin urmare, este nevoie de foarte puțină energie pentru a separa moleculele covalente una de cealaltă.
mulți studenți începători la chimie cred în mod fals că atunci când o moleculă covalentă se topește, legăturile covalente sunt rupte. Acest lucru este fals. Când compușii ionici se topesc, atracția Ionică eșuează. Când compușii covalenți se topesc, moleculele se îndepărtează pur și simplu unul de celălalt, lăsând legăturile intacte.
compușii covalenți sunt conductori slabi
compușii ionici sunt mari conductori de electricitate atunci când sunt dizolvați sau topiți. Așa cum s-a menționat în compușii ionici, acest lucru se datorează faptului că compușii ionici au ioni mobili care sunt capabili să transfere sarcina electrică dintr-un loc în altul. De asemenea, conduc căldura foarte bine, deoarece ionii sunt în regulă unul lângă celălalt, făcând posibilă transferul eficient al energiei dintr-un loc în altul.
compușii covalenți, pe de altă parte, sunt aproape întotdeauna izolatori buni atât pentru electricitate, cât și pentru căldură. Electricitatea nu este capabilă să conducă eficient prin compuși covalenți, deoarece nu există ioni care să deplaseze sarcina electrică. Un exemplu excelent în acest sens este în propria casă, unde metalul din cablurile prelungitoare este acoperit cu plastic pentru a evita electrocutarea pisicii. De asemenea, căldura nu călătorește bine prin compuși covalenți, deoarece moleculele nu sunt la fel de strâns legate între ele ca ionii dintr-un compus ionic, făcând transferul de căldură mai puțin eficient. Acesta este motivul pentru care folosiți mănuși de cuptor pentru a scoate cookie-urile din cuptor, mai degrabă decât să vă acoperiți mâinile cu sare.
compușii covalenți ard uneori
compușii organici sunt compuși covalenți care conțin carbon. De obicei conțin și hidrogen. și poate conține cantități mai mici de alte elemente, cum ar fi azot, sulf, fosfor, oxigen sau oricare dintre halogeni.
mulți compuși covalenți sunt inflamabili și ard ușor cu adăugarea de căldură. Grupul principal de compuși covalenți care sunt inflamabili se numesc compuși organici. Compușii organici ard deoarece conțin carbon și hidrogen, ambele combinându-se Frumos cu oxigenul la temperaturi ridicate.
este important să rețineți că nu toți compușii covalenți ard?de exemplu, apa este un compus covalent și veți avea un timp foarte greu de a începe un foc cu ea. Cu toate acestea, mulți compuși covalenți decât ionici sunt inflamabili.
inflamabilitatea este o proprietate generală a compușilor covalenți, deoarece o mare majoritate a compușilor covalenți cunoscuți sunt organici. Deoarece majoritatea compușilor organici ard, putem enumera în siguranță acest lucru ca o proprietate a compușilor covalenți, chiar dacă există mulți compuși covalenți care nu ard.
extras din Ghidul Idiotului complet pentru Chimie 2003 de Ian Guch. Toate drepturile rezervate, inclusiv dreptul de reproducere, integral sau parțial, sub orice formă. Folosit de aranjament cu Alpha Books, un membru al Penguin Group (SUA) Inc.
pentru a comanda această carte direct de la editor, vizitați site-ul Penguin USA sau sunați la 1-800-253-6476. De asemenea, puteți achiziționa această carte de la Amazon.com și Barnes & nobil.