nome genérico: fluocinonida Drugs.com. última atualização em 22 de Dezembro de 2020.
- Descrição
- Efeitos Colaterais
- Dosagem
- Profissional
- Medicamentosas
- Mais
Somente Rx
O Lidex marca foi descontinuado nos EUA Se versões genéricas deste produto foi aprovado pelo FDA, pode ser equivalentes genéricos disponíveis.
Lidex Descrição
Lidex® (fluocinonida) pomada 0, 05% destina-se a administração tópica. O componente ativo é o corticosteróide fluocinonide, que é o 21-éster acetato de fluocinolona acetonide e tem o nome químico pregna-1,4-dieno-3,20-diona,21-(acetiloxi)-6,9-difluoro-11-hidroxi-16,17–,(6α,11β,16α)-. Ele tem a seguinte estrutura química:
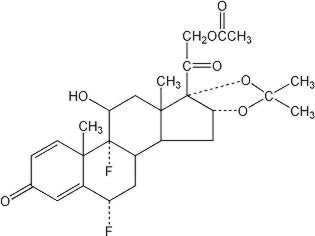
Lidex Pomada contém fluocinonide 0.5 mg / g numa base de pomada especialmente formulada, constituída por monoestearato de glicerilo, petrolato branco, carbonato de propileno, propilenoglicol e cera branca. Fornece os efeitos oclusivos e emolientes desejáveis numa pomada.nesta formulação, a substância activa está totalmente em solução.
Lidex-Farmacologia Clínica
os corticosteróides tópicos partilham acções anti-inflamatórias, anti-pruríticas e vasoconstritivas.o mecanismo da actividade anti-inflamatória dos corticosteróides tópicos não é claro. Vários métodos laboratoriais, incluindo testes vasoconstritores, são utilizados para comparar e prever as potências e/ou as efficacias clínicas dos corticosteróides tópicos. Existem algumas evidências que sugerem que existe uma correlação reconhecível entre a potência vasoconstritora e a eficácia terapêutica no homem.farmacocinética
farmacocinética
a extensão da absorção percutânea de corticosteróides tópicos é determinada por muitos factores, incluindo o veículo, a integridade da barreira epidérmica e a utilização de pensos oclusivos.os corticosteróides tópicos podem ser absorvidos a partir da pele intacta normal. A inflamação e / ou outros processos de doença na pele aumentam a absorção percutânea. Pensos oclusivos aumentam substancialmente a absorção percutânea de corticosteróides tópicos. Assim, os pensos oclusivos podem ser um valioso adjuvante terapêutico para o tratamento de dermatoses resistentes (ver dosagem e administração).uma vez absorvidos através da pele, os corticosteróides tópicos são manuseados através de vias farmacocinéticas semelhantes às dos corticosteróides administrados por via sistémica. Os corticosteróides estão ligados às proteínas plasmáticas em vários graus. Os corticosteróides são metabolizados principalmente no fígado e são depois excretados pelo rim. Alguns dos corticosteróides tópicos e seus metabolitos também são excretados na bílis.
indicações e utilização de Lidex
Lidex pomada está indicado para o alívio das manifestações inflamatórias e pruríticas das dermatoses que respondem aos corticosteróides.
contra-indicações
corticosteróides tópicos estão contra-indicados em doentes com história de hipersensibilidade a qualquer um dos componentes da preparação.
precauções
geral
absorção sistémica de corticosteróides tópicos produziu supressão reversível do eixo hipotalâmico-pituitária-adrenal (HPA), manifestações da síndrome de Cushing, hiperglicemia e glucosúria em alguns doentes.as condições que aumentam a absorção sistémica incluem a aplicação de esteróides mais potentes, a utilização em grandes áreas de superfície, o uso prolongado e a adição de pensos oclusivos.assim, os doentes a receber uma grande dose de um potente esteróide tópico aplicado numa grande área de superfície ou sob um penso oclusivo devem ser avaliados periodicamente quanto à evidência de supressão do eixo HPA utilizando os testes urinários de estimulação do cortisol livre e ACTH. Se a supressão do eixo HPA é notado, uma tentativa deve ser feita para retirar a droga, para reduzir a frequência de aplicação, ou para substituir um esteróide menos potente.a recuperação da função do eixo HPA é geralmente rápida e completa após a descontinuação do fármaco. Raramente, podem ocorrer sinais e sintomas de privação de esteróides, exigindo corticosteróides sistémicos suplementares.
As crianças podem absorver quantidades proporcionalmente maiores de corticosteróides tópicos e, assim, ser mais sensíveis à toxicidade sistémica (ver precauções – Utilização Pediátrica). Se se desenvolver irritação, os corticosteróides tópicos devem ser descontinuados e instituída terapêutica apropriada.tal como com qualquer corticosteróide tópico, a utilização prolongada pode produzir atrofia da pele e dos tecidos subcutâneos. Quando usado em áreas intertriginosas ou flexoras, ou na face, isso pode ocorrer mesmo com uso de curto prazo.na presença de infecções dermatológicas, deve ser instituído o uso de um agente antifúngico ou antibacteriano apropriado. Se não ocorrer prontamente uma resposta favorável, o corticosteróide deve ser interrompido até que a infecção tenha sido adequadamente controlada.
informação para o doente
os doentes que utilizam corticosteróides tópicos devem receber a seguinte informação e instruções:
- Este medicamento deve ser utilizado de acordo com as instruções do médico. É apenas para uso externo. Evitar o contacto com os olhos.
- Os doentes devem ser aconselhados a não utilizar este medicamento para qualquer doença para além da para a qual foi prescrito.a área da pele tratada não deve ser tratada com ligaduras ou de outra forma coberta ou embrulhada como sendo oclusiva, a menos que indicado pelo médico.os doentes devem comunicar quaisquer sinais de reacções adversas locais, especialmente sob tratamento oclusivo.os pais de doentes pediátricos devem ser aconselhados a não usar fraldas apertadas ou calças de plástico numa criança a ser tratada na área das fraldas, uma vez que estas roupas podem constituir pensos oclusivos.os seguintes testes podem ser úteis na avaliação da supressão do eixo HPA:não foram realizados estudos em animais a longo prazo para avaliar o potencial carcinogénico ou o efeito na fertilidade de corticosteróides tópicos.os estudos para determinar a Mutagenicidade com prednisolona e hidrocortisona revelaram resultados negativos.os corticosteróides são geralmente teratogénicos em animais de laboratório quando administrados sistemicamente a níveis posológicos relativamente baixos. Os corticosteróides mais potentes demonstraram ser teratogénicos após aplicação dérmica em animais de laboratório. Não existem estudos adequados e bem controlados em mulheres grávidas sobre efeitos teratogénicos de corticosteróides topicamente aplicados. Assim, os corticosteróides tópicos só devem ser utilizados durante a gravidez se o potencial benefício justificar o potencial risco para o feto. Os medicamentos desta classe não devem ser utilizados extensivamente em doentes grávidas, em grandes quantidades ou durante períodos prolongados de tempo.não se sabe se a administração tópica de corticosteróides pode resultar numa absorção sistémica suficiente para produzir quantidades detectáveis no leite materno. Os corticosteróides administrados por via sistémica são secretados no leite materno em quantidades que não são susceptíveis de ter um efeito deletério no lactente. No entanto, deve ter-se precaução quando os corticosteróides tópicos são administrados a uma mulher amamentadora.
Utilização Pediátrica
os doentes pediátricos podem demonstrar uma maior susceptibilidade à supressão do eixo hipotálmico-pituitária-adrenal (HPA) induzida por corticosteróides tópicos e à síndrome de Cushing do que os doentes adultos, devido a uma maior relação entre a superfície da pele e o peso corporal.foram notificados casos de supressão do eixo HPA, síndrome de Cushing e hipertensão intracraniana em crianças tratadas com corticosteróides tópicos. As manifestações de supressão supra-renal em crianças incluem atraso no crescimento linear, aumento de peso retardado, níveis plasmáticos baixos de cortisol e ausência de resposta à estimulação da ACTH. Manifestações de hipertensão intracraniana incluem Fontanelas inchadas, dores de cabeça e papiledema bilateral.a administração de corticosteróides tópicos a crianças deve ser limitada ao mínimo compatível com um regime terapêutico eficaz. A terapêutica crónica com corticosteróides pode interferir com o crescimento e desenvolvimento de crianças.
reacções adversas
as seguintes reacções adversas locais são notificadas pouco frequentemente com corticosteróides tópicos, mas podem ocorrer mais frequentemente com o uso de pensos oclusivos. Estas reacções estão listadas numa ordem decrescente aproximada de ocorrência:
Burning Perioral dermatitis Itching Allergic contact dermatitis Irritation Maceration of the skin Dryness Secondary infection Folliculitis Skin atrophy Hypertrichosis Striae Acneiform eruptions Miliaria Hypopigmentation Overdosage
Topically applied corticosteroids can be absorbed in sufficient amounts to produce systemic effects (see PRECAUTIONS).a dose e a administração de Lidex da pomada de Lidex são geralmente aplicadas na área afectada, sob a forma de uma película fina, de duas a quatro vezes por dia, dependendo da gravidade da situação.podem ser utilizadas pensos oclusivos para o tratamento da psoríase ou de situações recalcitrantes.se se desenvolver uma infecção, deve interromper-se a utilização de pensos oclusivos e instituir-se uma terapêutica antimicrobiana adequada.
como é fornecido Lidex
Lidex® (fluocinonida) pomada 0.05% é fornecido em
15 g do Tubo –NDC 99207-514-13
30 g do Tubo –NDC 99207-514-14
de 60 g do Tubo –NDC 99207-514-17
120 g de Tubo –NDC 99207-514-22
Armazenar em temperatura ambiente. Evitar temperaturas superiores a 30 ° C (86°F).
Patente No. 4017,615
fabricado para:
MEDICIS, the Dermatology Company®
Scottsdale, AZ 85258
Por: Patheon, Inc.
Mississauga, Ontario
Canada L5N 7K9
IN-5070/S
Lidex
fluocinonide ointmentProduct Information Product Type HUMAN PRESCRIPTION DRUG LABEL Item Code (Source) NDC:99207-514 Route of Administration TOPICAL DEA Schedule Active Ingredient/Active Moiety Ingredient Name Basis of Strength Strength fluocinonide (fluocinonide) fluocinonide 0.5 mg in 1 g Inactive Ingredients Ingredient Name Strength glyceryl monostearate white petrolatum propylene carbonate propylene glycol white wax Packaging # Item Code Package Description 1 NDC:99207-514-13 15 g (15 GRAM) in 1 TUBE 2 NDC:99207-514-14 30 g (30 GRAM) in 1 TUBE 3 NDC:99207-514-17 60 g (60 GRAM) in 1 TUBE 4 NDC:99207-514-22 120 g (120 GRAM) in 1 TUBE Labeler – MEDICIS
MEDICISFrequently asked questions
- Is it used for hair loss?
- What is a substitute for fluocinonide cream?
- Is fluocinonide an antifungal cream?
- How long should you use fluocinonide for?
- What is fluocinonide cream good for?o fluocinonida pode ser utilizado para tratar uma erupção cutânea da hera venenosa?é um esteróide?isto é um antibiótico?
Mais sobre Lidex (fluocinonide tópica)
- Efeitos Colaterais
- Durante a Gravidez ou a Amamentação
- Informação sobre a Dosagem
- Interações Medicamentosas
- 8 Comentários
- Disponibilidade Genérico
- classe de Drogas: os esteróides tópicos
recursos para o Consumidor
- Avançado de Leitura
- Lidex Leve (Leitura Avançada)
- Lidex Regular (Leitura Avançada)
recursos
- Informação de Prescrição
- Lidex Solução Tópica (FDA)
- Lidex Gel (FDA)
Outras marcas Vanos, Lidex-E
Relacionados guias de tratamento
- Dermatite Atópica
- Eczema
- Dermatite
- Psoríase
Medical Disclaimer