Antiaromatische verbindingen zijn ongewoon instabiel
Wat zijn de belangrijkste factoren die bepalen of een molecuul antiaromatisch is?
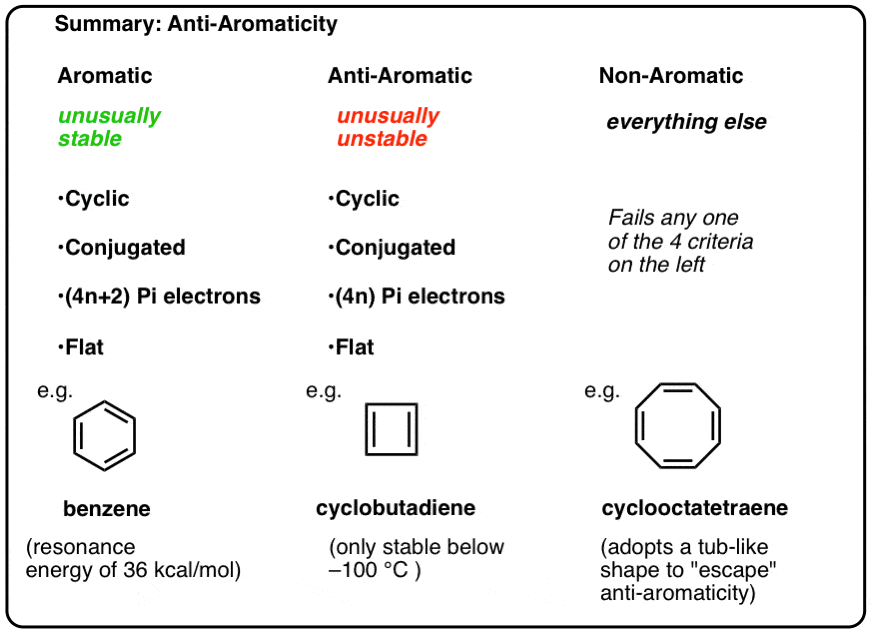
In onze vorige berichten in onze serie over aromaticiteit zagen we dat aromatische moleculen ongewoon stabiel zijn. Zij hebben bijzonder grote resonantie-energieën, ondergaan eerder substitutie dan additie reacties, en hebben delokaliseerde pi-elektronen (alle C-C Bindingslengten in benzeen zijn bijvoorbeeld gelijk).
om aromatisch te zijn, moet een molecuul de volgende vier structurele kenmerken hebben:
- cyclisch
- rondom de ring geconjugeerd
- pi-elektronen
- plat (vlak)
indien aan deze vier voorwaarden wordt voldaan, is het molecuul aromatisch.
als het ook maar één vraag in de test zakt, is het niet-aromatisch.
dat lijkt vrij duidelijk. Of toch wel?
je zou kunnen raden aan de manier waarop ik deze vraag framing dat het antwoord is “niet helemaal”. : – )
Inhoudsopgave
- Sommige Moleculen Zijn Zo Spectaculair En Buitengewoon Instabiel En Moeilijk Te Isoleren Dat Ze Verdienen Hun Eigen Categorie:Antiaromatic
- Cyclopentadienyl Kation: De “Resonantie Gestabiliseerd” Carbocation Die niet Stabiel
- Antiaromatic Drie-Ledige Ringen: Oxirene, 1H-Azirene, Thiirene
- Cyclobutadiene Is Antiaromatic
- Een 8 Pi-Elektron Voorbeeld van een Samengestelde Antiaromatic: Pentaleen
- Wat maakt een molecuul Anti-aromatisch?
- Cyclooctatetraeen “ontsnapt” aan Anti-aromaticiteit door uit vlakheid te draaien
- conclusie: Antiaromatische verbindingen
- noten
- Geavanceerd: referenties en verdere lezing
1. Spectaculair onstabiele moleculen die een categorie op zichzelf vormen: “Anti-aromatisch”
Het zit zo. Er is een klein aantal moleculen dat zakt voor de aromaticiteitstest die niet alleen niet aromatisch zijn: ze hebben de eigenschap zo spectaculair en ongewoon onstabiel te zijn en moeilijk te isoleren dat ze een andere naam verdienen.
we noemen deze moleculen “anti-aromatisch”.wat interessant is, is dat in veel gevallen de moleculen zelf niet bijzonder onstabiel lijken ten opzichte van de eerste principes, in tegenstelling tot bijvoorbeeld Cubaan. Grappig genoeg kun je Cubaan (min of meer) van Aldrich kopen, maar de meeste anti-aromatische moleculen die we hieronder bespreken zijn alleen stabiel bij extreem lage temperaturen – als ze al geïsoleerd kunnen worden!
2. Cyclopentadienylkation: De” resonantie-gestabiliseerde ” carbocatie die niet stabiel is
laten we onze reis door het konijnenhol beginnen met een eenvoudig voorbeeld dat bekend zou moeten lijken uit de organische chemie van het eerste semester.
herinnert u zich de SN1-reactie? De kat die als eerste de comfortabele stoel verlaat?
snelle beoordeling: begin met een alkylhalide. Het verlaten van de groep verlaat, de vorming van een carbocatie. Nucleofiele aanvallen. Het heet de SN1 omdat de snelheidsbepalende stap (carbocatievorming) unimoleculair is. Bottom line: hoe stabieler de carbocatie, hoe sneller de reactie verloopt. Daarom is de reactiesnelheid voor alkylhalogeniden tertiair > secundair > primair, en de carbocatie krijgt speciale bonuspunten als het door resonantie wordt gestabiliseerd.
Kijk naar deze twee SN1-reacties. Welke zou volgens u sneller gebeuren – de SN1-reactie die door een secundaire carbocatie gaat (A), of de SN1-reactie die door een secundaire carbocatie gaat en meerdere resonantievormen kan vormen (B)?
van alles wat je tot nu toe hebt geleerd, zou je verwachten dat het antwoord B) is.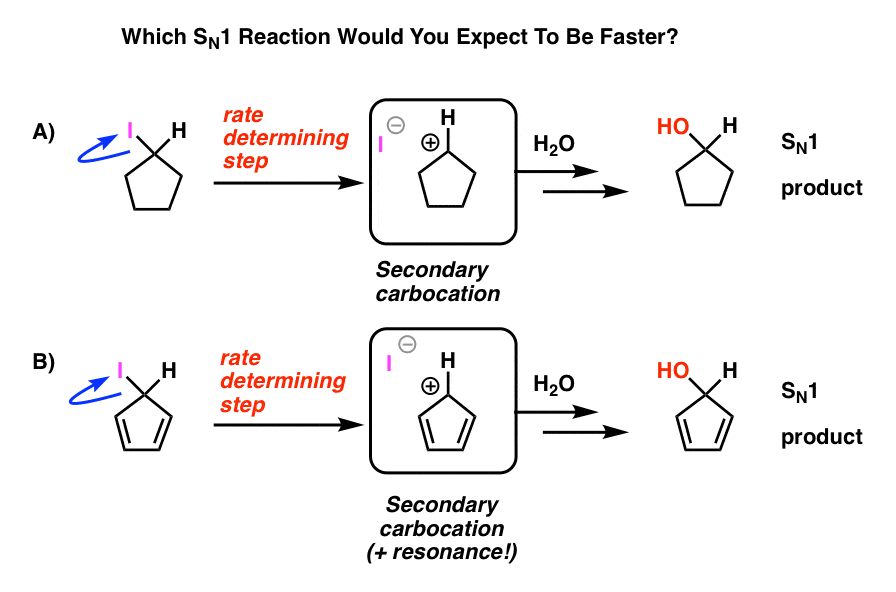
Het is niet.
het antwoord is dat reactie A) sneller gebeurt. Reactie B komt helemaal niet voor.
Dit zou je heel vreemd moeten vinden.
Het is!
Hoe komt het dat deze zogenaamde resonantie-gestabiliseerde carbocatie minder stabiel is dan een secundaire carbocatie?
immers, hoe vaak wordt het geboord in je hoofd dat resonantie stabiliseert moleculen, vooral carbokaties?
maar hier lijkt het destabiliserend. Het is … het is …

maar onstabiel is het! Het cyclopentadienylkation is ongelooflijk onstabiel en moeilijk te maken – en het is niet bij gebrek aan proberen. Er is iets heel vreemds aan de structuur van het cyclopentadienylkation dat het ongewone instabiliteit geeft.

cyclisch, geconjugeerd, plat…. en heeft 4 pi-elektronen. Interessant!
3. Antiaromatische drievoudige ringen: Oxirene, 1h-Azireen, Thiirene
een andere klasse van “ongrijpbare” moleculen is een familie van drievoudige ringen. U herinnert zich misschien uit Org 1 dat het gemakkelijk is om epoxiden te maken van alkenen met behulp van een oxidant zoals m-CPBA.heb je je ooit afgevraagd waarom we nooit dezelfde reactie voor alkynen hebben behandeld?
nou, het is niet bij gebrek aan proberen. Chemici hebben allerlei methoden geprobeerd om alkynen te epoxideren, en weet je wat? De reactie werkt gewoon niet.
bijvoorbeeld, epoxidatie van acetyleen zou het molecuul hieronder geven (oxirene).
Oxirene zelf is nooit waargenomen, hoewel er prikkelende sporen zijn van zijn vluchtige bestaan. En trouwens, noch het stikstof-analoog, 1H-azireen, of het thiirene.
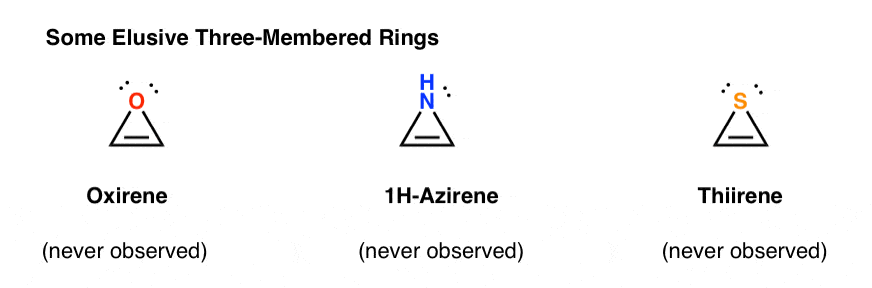
waarom niet? Wat is er speciaal aan elk van deze zaken?
je zou kunnen opmerken dat, net als het cyclopentadienylkation, deze moleculen cyclisch, geconjugeerd, vlak zijn en 4 pi-elektronen hebben (twee in de pi-binding, en twee uit een enkel paar).
OK. Wat kan er nog meer cyclisch, geconjugeerd, plat zijn en 4 pi-elektronen hebben?
4. Cyclobutadieen is Antiaromatisch
Cyclobutadieen lijkt een eenvoudig genoeg molecuul, maar werd pas in 1965 gesynthetiseerd. En zelfs toen bleek dat het niet stabiel was bij temperaturen boven 35 Kelvin.
de vraag is, waarom?

zeker, het is een vier-ledige ring, en ja, het heeft veel ringstam, maar er zijn meer gespannen moleculen gemaakt die eigenlijk stabiel zijn bij kamertemperatuur.
u kunt ook opmerken dat, net als de bovenstaande voorbeelden, cyclobutadieen een ander voorbeeld is van een molecuul dat cyclisch is, geconjugeerd, 4 pi-elektronen heeft en plat is.
wat nog interessanter is, is wat geleerd werd over de geometrie van cyclobutadieen. In plaats van een molecuul met identieke bindingslengtes (zoals benzeen), bleek cyclobutadieen een rechthoekige vorm te hebben, wat erop wijst dat de elektronen niet gedelokaliseerd waren.
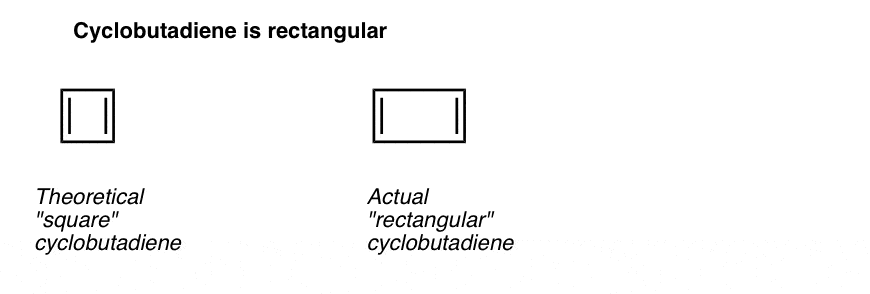
wat dit ons vertelt is dat zelfs wanneer een molecuul aan alle voorwaarden voldoet (cyclische, geconjugeerde, platte, 4 pi-elektronen), de symmetrische geometrie bijzonder onstabiel is. . Heel interessant!
een 8 Pi-elektron voorbeeld van een Antiaromatische verbinding: Pentaleen
tot nu toe hadden alle voorbeelden die we tot nu toe hebben gezien 4 pi-elektronen. Je vraagt je misschien af: zijn er voorbeelden van anti-aromatische moleculen die meer dan 4 pi elektronen hebben? Waarom, Ja.
het molecuul hieronder wordt “Pentaleen”genoemd. Het is samengesteld, maar is slechts Stabiel onder -100 °C. boven deze temperatuur combineert het met een ander molecuul van zichzelf (referentie). Nog een voorbeeld van spectaculaire instabiliteit.

Pentaleen heeft 8 pi-elektronen. Dit kan een aantal alarmbellen van herkenning doen afgaan. Herinner hoe het aantal pi-elektronen in aromatische moleculen de opeenvolging volgden (2, 6, 10, 14….) ?
dit voorbeeld suggereert dat het aantal pi-elektronen in anti-aromatische moleculen de sequentie volgt (4, 8, 12…)
wat maakt een molecuul Anti-aromatisch?
dus wat hebben al deze moleculen in deze galerij gemeen?
elk van hen is cyclisch, geconjugeerd en plat – en als je het aantal pi-elektronen meetelt, is het veelvouden van 4. Dus terwijl aromatische moleculen (4n+2) pi-elektronen hebben, is de” regel ” voor anti-aromatische moleculen (4n). (een andere manier om het te bekijken: het aantal pi-elektronen zal tweemaal een even getal zijn).
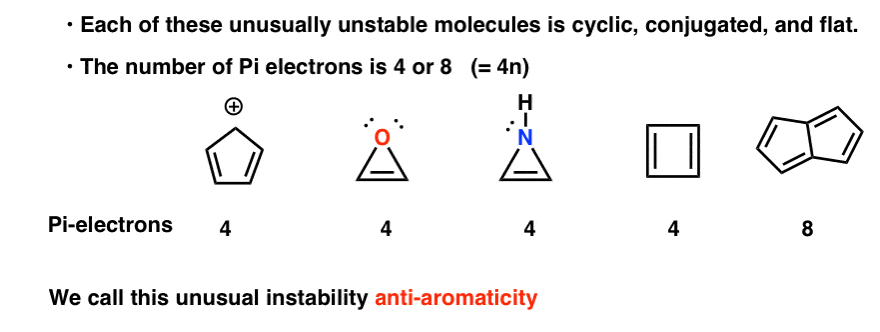
deze ongewone instabiliteit wordt”anti-aromaticiteit” genoemd.
Dit betekent dat we nu drie categorieën voor moleculen kunnen opstellen volgens de volgende criteria:
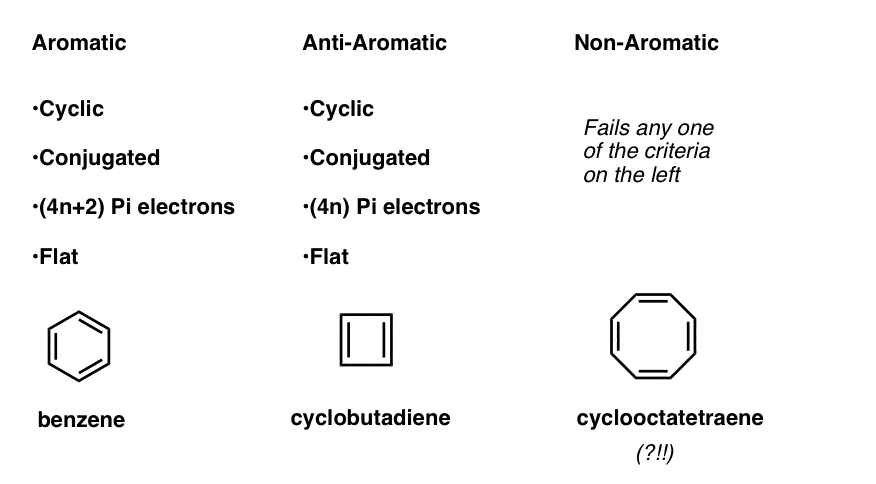
- aromatische moleculen zijn cyclisch, geconjugeerd, hebben (4n+2) pi-elektronen en zijn plat.
- Anti-aromatische moleculen zijn cyclisch, geconjugeerd, hebben (4N) pi-elektronen en zijn plat.
- niet-aromatische moleculen zijn elk ander molecuul dat niet voldoet aan een van deze voorwaarden.
wacht even – je zou je kunnen afvragen waarom cyclooctatetraeen geclassificeerd is als”niet-aromatisch”. Met 8 pi-elektronen (tweemaal een even getal) zou het niet “anti-aromatisch”moeten zijn?
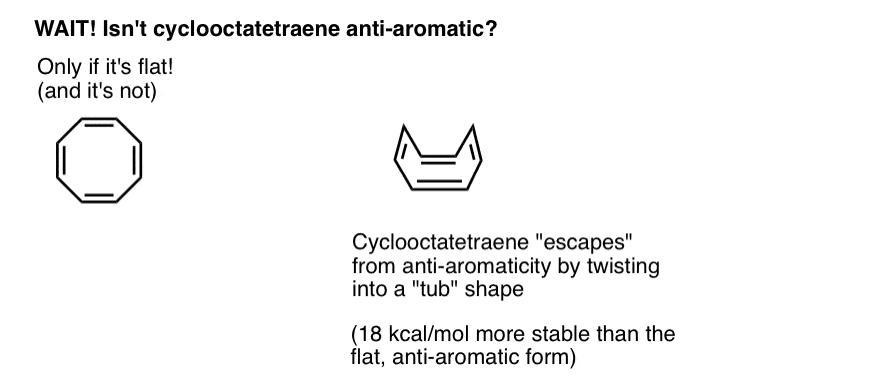
Cyclo-Octatetraeen “ontsnapt” aan Anti-aromaticiteit door uit vlakheid te draaien
zie het voldoen aan de voorwaarden voor “anti-aromaticiteit” als een beetje als het in aanmerking komen voor een zeer zware inkomstenbelasting. Als je de kans krijgt om een maas in de wet te vinden om onder de belasting te komen, zou je dat dan doen? Waarschijnlijk.
Cyclooctatetraeen is alleen anti-aromatisch als het plat is. De relatief “floppy” structuur van cyclooctatetraeen zorgt echter voor enige flexibiliteit. De bindingen kunnen van vlakheid zo roteren dat het molecuul een “tub-achtige” vorm aanneemt, waardoor de “antiaromaticiteitsbelasting” van 18 12 kcal / mol wordt vermeden die zou worden betaald als alle p-orbitalen op het molecuul met elkaar werden vervoegd.
Het blijkt dat Cyclo-octatetraeen is gesynthetiseerd, stabiel is (je kunt het hier bijvoorbeeld kopen) en zich gedraagt als een “normaal” alkeen, additie reacties ondergaat, hydrogenering, enzovoort.
Pentaleen (boven), dat ook 8 pi-elektronen heeft, heeft een zeer stijve bicyclische structuur die binding-rotatie weg van vlakheid voorkomt. Daarom zit het vast in zijn anti-aromatische constructie.
Anti-aromaticiteit voor moleculen met meer dan 8 pi-elektronen is bekend, maar zeer ongebruikelijk. (Hier is een leuk voorbeeld van een andere “ontsnapping” uit de aromaticiteit voor een molecuul met 18 pi-elektronen.)
conclusie: Antiaromatische verbindingen
tot nu toe is onze behandeling van aromaticiteit en anti-aromaticiteit zuiver beschrijvend en empirisch geweest. We hebben veel voorbeelden laten zien, en veel regels gegeven, maar ontbreekt in de discussie is een diepe verklaring van “waarom”geweest.
Wat is er zo speciaal aan de benzeenring dat deze zo stabiel is? Waarom is het stabiel?
Wat is er zo speciaal aan het cyclobutadieenstelsel dat het zo onstabiel maakt? Waarom is het onstabiel?
om deze diepere vragen te beantwoorden, moeten we een stap terug doen en de moleculaire orbitalen van deze twee moleculen onderzoeken, en dan tot een dieper begrip komen van aromaticiteit en anti-aromaticiteit.
dat is wat we gaan doen in ons volgende bericht.
Met dank aan Matthew Knowe voor hulp bij het voorbereiden van dit bericht.
opmerkingen
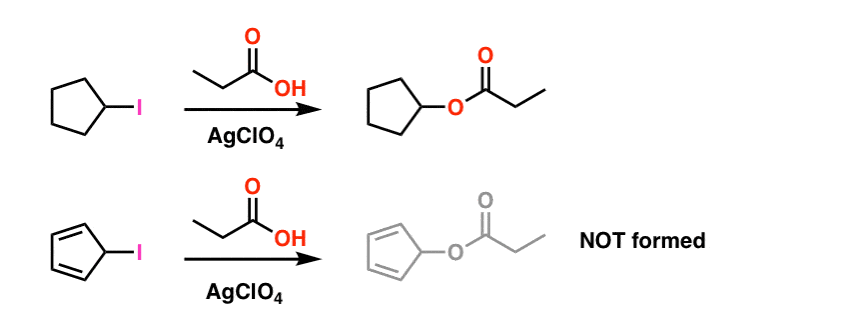
voetnoot 1. Voor de eenvoud, de afbeelding in het hoofdartikel fudges op de werkelijke reactie voorwaarden. De werkelijke experimentele omstandigheden worden hieronder weergegeven. Het oplosmiddel is propionzuur, en het Lewis-zuur zilverperchloraat wordt toegevoegd om te helpen bij het uittrekken van het jodium. .
zelfs onder deze omstandigheden wordt de cyclopentadienylcarbocatie niet gevormd, wat een bewijs is van zijn extreme instabiliteit.
voetnoot 2. Epoxidatie op etheen (aka ethyleen) wordt gedaan op de melodie van 15 miljoen ton, jaarlijks. Epoxidatie van acetyleen tot oxirene is niet bekend.
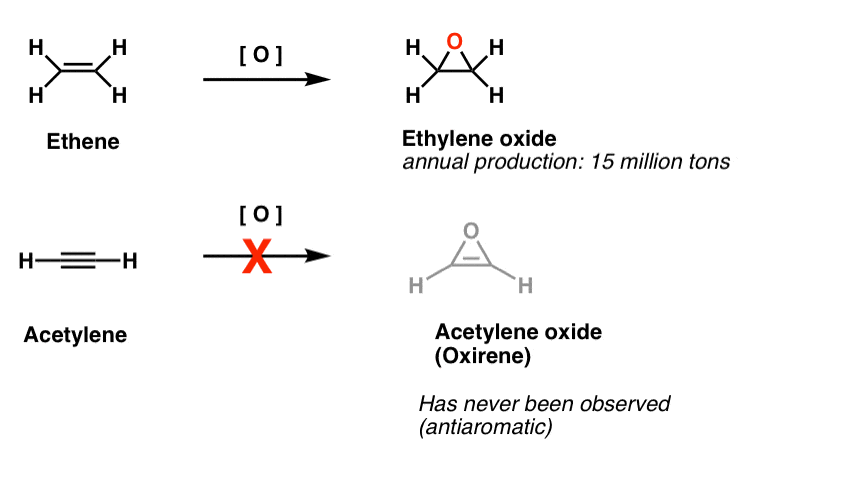
Vluchtig bewijs van het bestaan van oxirenen is gevonden. Er zijn goede aanwijzingen uit isotopenetiketteringsstudies dat oxirenen vluchtige tussenproducten zijn in bepaalde Wolff-herschikkingen. Er zijn ook twee voorbeelden van oxirenen die zijn gevangen bij extreem lage temperatuur, maar ontbonden boven 35 Kelvin.
het vluchtige bestaan van een 1h-azirine is gepostuleerd in de toevoeging van een nitreen aan een acetyleen, dat snel herschikt tot een (stabiel) 2H-azireen (hieronder).
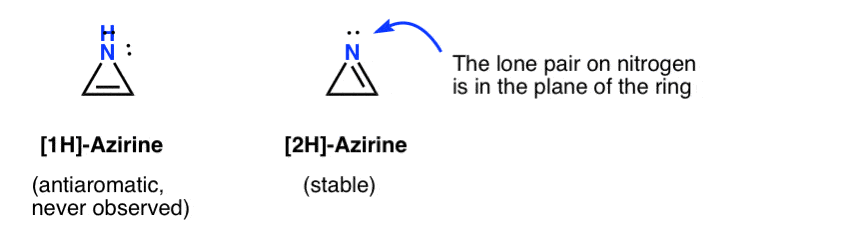
merk op dat in 2H-azireen het eenzame paar op de stikstof loodrecht staat op het pi-systeem, dus dit systeem is niet-aromatisch in tegenstelling tot anti-aromatisch.
voor meer discussie, zie March ‘ s Advanced Organic Chemistry. Ik heb gewerkt aan de 5e editie, pagina ‘ s 62-63.
. Voetnoot 3. Een zeer slim experiment stelde vast dat 1,2-dideutero cyclobutadieen twee isomeren heeft, niet één (zie hieronder). Dit wijst erop dat de dubbele bindingen in cyclobutadieen niet worden gedelokaliseerd zoals in benzeen, maar eerder dubbele bindingen zijn in een conventioneel dieen.
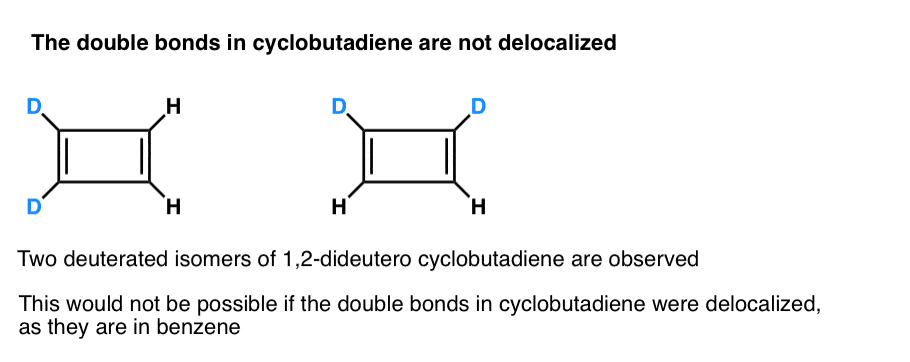
Cyclobutadieen reageert met zichzelf bij 35 K om een “dimeer” te vormen, in een voorbeeld van een Diels-Elsreactie.
voetnoot 4. Ja, Het is waar dat het eenzame paar in azireen in een sp3 hybride orbitaal kan worden geplaatst (hieronder). Dit vermindert waarschijnlijk de anti-aromatische “straf” enigszins, maar het molecuul is nog steeds ongelooflijk onstabiel. Anti-aromaticiteit is de eenvoudigste manier om dit te verklaren.

voetnoot 5. De rechthoekige geometrie is te wijten aan een effect dat bekend staat als het Jahn-Teller effect. Herinner je je het Pauli uitsluitingsprincipe, waar elektronen niet hetzelfde kwantumgetal kunnen hebben? Nou, zoals we zullen zien als we kijken naar het moleculaire orbitale diagram van cyclobutadieen, “vierkant” cyclobutadieen heeft twee “gedegenereerde” elektronen, dat wil zeggen ze hebben dezelfde energieën en kwantumgetallen. Dit leidt tot een fenomeen dat bekend staat als “Pauli repulsion”, waar verlenging van de bindingen plaatsvindt totdat de energieniveaus van de twee elektronen zijn gedifferentieerd. Zeker een geavanceerd onderwerp.
(Advanced) References and Further Reading
- Transition-State Spectroscopy of Cyclooctatetraene
Paul G. Wenthold, David A. Hrovat, Weston T. Borden, W. C. Lineberger.Science, 1996, 272, 1456-1459.DOI: 10.1126 / science.Deze studie vormt de basis voor de stelling dat de niet-aromatische grondtoestand van cyclo-octatetraeen 12 kcal/mol onder de “anti-aromatische” bevleesdheid ligt.The Taming of Cyclobutadieen Donald J. Cram, Martin E. Tanner, Robert Thomas Chem. Int. Ed. 1991, 30 (8), 1024-1027
DOI: 10.1002/anie.Dit artikel van Nobelprijswinnaar Prof.Donald J. Cram (UCLA) beschrijft de eerste spectroscopische karakterisering van cyclobutadieen. Dit wordt bereikt door de precursor te omsluiten in een hemicarcerand (kooicomplex), en het vervolgens te bestralen met UV-licht, waardoor cyclobutadieen ontstaat, dat niet in staat is om iets te doen omdat het gevangen is.Cyclobutadieen Thomas Bally, Satoru Masamune Tetrahedron 1980, 36 (3), 343-370 DOI: 1016/0040-4020(80) 87003-7 dit artikel uit 1980 geeft een overzicht van de tot dan toe verrichte werkzaamheden aan cyclobutadieen. Dit is verdeeld in 2 delen – experimentele synthetische inspanningen en theoretische berekeningen. - Tetrahedraan en Cyclobutadieen
Günther Maier
Chem. Int. Ed. 1988, 27 (3), 309-332 DOI: 10.1002/anie.198803093 dit artikel geeft een overzicht van de synthetische inspanningen voor tetrahedraan en cyclobutadieen – beide moleculen hebben een formule van C4H4. Alleen gesubstitueerde (tetra t-butyl en tetra trimethylsilyl) tetrahedranen zijn tot op heden met succes gesynthetiseerd en geïsoleerd. - Cyclobutadieen – and Benzocyclobutadieen-Iron Tricarbonyl Complexes
F. Emerson, L. Watts,and R. Pettit
Journal of the American Chemical Society 1965, 87 (1), 131-133
DOI: 10.1021/ja01079a032 - Cyclobutadieeneiron Tricarbonyl. Een nieuw aromatisch systeem
D. Fitzpatrick, L. Watts, G. F. Emerson,and R. Pettit Journal of the American Chemical Society 1965, 87 (14), 3254-3255
DOI: 10.1021/ja01092a050
a bonus topic: cyclobutadieen can be stabilised with metals – the organometallic complex cyclobutadieen iron tricarbonyl is a stable, crystalline solid. Zoals de auteurs vermelden, is het onwaarschijnlijk dat vrij cyclobutadieen wordt gegenereerd in de synthese. - https://www.asu.edu/courses/chm233/notes/aromatic/aromaticRL1/antiaromatic.html
het antipsychoticum olanzapine heeft een” vlindervorm ” om antiaromatische effecten te vermijden, vergelijkbaar met cyclooctatetraeen. Dit is blijkbaar van cruciaal belang voor zijn functie.Ronald Breslow Accounts of Chemical Research 1973, 6 (12), 393-398 * DOI: 1021/ar50072a001 * Doi: 1021 / Ar50072a001 * Doi: 1021 / Ar50072a001 * Doi: 1021 / Ar50072a001 * Doi: 1021 / Ar50072a001 Hij citeert ook ander werk van Prof. M. J. S. Dewar en anderen waar de antiaromatische destabilisatie van cyclobutadieen wordt berekend tussen 18-33 kcal/mol ten opzichte van lineair butadieen.Experimental Determination of the Antiaromaticity of Cyclobutadieen Ashok A. Deniz, Kevin S. Peters, Gary J. Snyder Science 1999, 286 (5442), 1119-1122 DOI: 1126/science.Dit is een zeer rigoureus artikel dat gebruik maakt van nieuwe spectroscopische technieken om antiaromatische destabilisatie van cyclobutadieen te bepalen. Ten opzichte van een hypothetische stamloze, geconjugeerde dieenreferentie wordt cyclobutadieen gedestabiliseerd met in totaal 87 kcal/mol, waarvan 32 kcal/mol kan worden toegeschreven aan ringstam en 55 kcal/mol aan antiaromaticiteit (vergeleken met 21 kcal/mol voor de aromatische stabilisatie van benzeen).Unsubstituated cyclopentadienyl cation,a ground-state triplet Saunders, R. Berger, A. Jaffe, J. M. McBride, J. O ‘ Neill, R. Breslow, J. M. Hoffmann, C. Perchonock, E. Wasserman, R. S. Hutton, V. J. Kuck Journal of the American Chemical Society 1973, 95 (9), 3017-3018 DOI: 10.1021 / ja00790a049
Het cyclopentadienylkation kan alleen met moeite worden bereid, zoals in dit artikel wordt beschreven. Zodra het is gevormd, heeft het een drievoudige elektronische grondtoestand (met 2 ongepaarde elektronen), en kan door EPR (elektron paramagnetische resonantie) spectroscopie worden gekenmerkt. - Oxirenes
Errol G. Lewars
Chemical Reviews 1983, 83 (5), 519-534
DOI: 10.1021 / cr00057a002