Ziprasidon versus Olanzapin i vektøkningen forbundet med behandling av schizofreni: en seks måneders dobbeltblind randomisert parallellgruppestudie
Enric Álvarez*; Miguel Bernardo**; José Ramón Gutié Casares***; Á L. Montejo****
* institutt for psykiatri. Hospital De La Santa Creu I Sant Pau. Cibersam, Universitat Aut@noma De Barcelona, IBSantpau Barcelona. Spania
** Institutt For Psykiatri, Hospital Clinic De Barcelona, CIBERSAM, Universitetet I Barcelona, IDIBAPS, Barcelona. Spania
* * * Universitetssykehus Kompleks Av Badajoz. Extremadura Helsetjeneste, Badajoz. Spania
**** Universitetssykehuset I Salamanca. Universitetet I Salamanca, Salamanca. Spania
denne studien ble finansiert Av Pfizer.
Korrespondanse
ABSTRAKT
Bakgrunn Og Mål: Tidligere data fra sikkerhetsanalyser indikerer at olanzapin kan gi betydelig vektøkning, mens ingen endring er observert med ziprasidon. Fedme kan være en trussel mot helse og føre til at personer slutter å ta antipsykotiske medisiner. For ytterligere å vurdere de differensielle effektene av ziprasidon og olanzapin på vektøkning, ble det utført en studie med kroppsvekt som det primære effektendepunktet.
Metoder: En seks måneders randomisert, dobbeltblind, parallellstudie ble utført med mannlige og kvinnelige forsøkspersoner i alderen 18-70 år med primærdiagnose schizofreni (DSM-IV-TR) og en klinisk tilstand som krevde oppstart av behandling med et nytt antipsykotikum, ziprasidon eller olanzapin 1:1, for å vurdere behandlingsrelaterte vektendringer. Femti pasienter ble inkludert. Effektresultatene ble vurdert ved baseline og ved uke 1, 4, 12, 18 og 24. Det primære effektendepunktet var prosentvis endring fra baseline i kroppsvekt ved uke 24. Sikkerheten ble også vurdert.
Resultater: Ved uke 24 var det en signifikant større økning i kroppsvekt (7,5%, p <0,0001) hos pasienter behandlet med olanzapin enn hos pasienter behandlet med ziprasidon, og antall personer som hadde vektøkning > 7% var signifikant høyere i olanzapin sammenlignet med ziprasidongruppen (n = 11 ) vs n = 3 ; eller = 6,246, p-verdi = 0,0150). PANNS-N betydelig redusert i begge grupper. De fleste Ae var moderate eller milde i begge grupper. Konklusjoner: Olanzapin øker kroppsvekten betydelig over ziprasidon ved uke 24. Behandling med enten ziprasidon eller olanzapin bedret PANSS positive, negative og generelle psykopatologiske skår og ble godt tolerert.
Nøkkelord: Antipsykotiske midler; Vektøkning; Ziprasidon; Olanzapin; Fedme.
Innledning
Schizofrene pasienter viser en høyere pre-valens av fedme, glukoseintoleranse og type 2 diabetes mellitus, med en genetisk kobling til enzymer involvert i glykolyse1, 2 og en høyere forekomst av kardiovaskulære hendelser3. Videre er mange andre generasjons antipsykotika forbundet med høyere risiko for vektøkning2, 4, insulinresistens, hyperglykemi og dyslipidemi5. Kombinasjonen av disse ulike faktorene, genetisk følsomhet, stillesittende livsstil og dårlig kosthold og de negative bivirkningene av antipsykotisk behandling, utgjør en viktig risikofaktor for kardiovaskulær sykdom hos pasienter behandlet med atypiske antipsykotika6. Ikke bare er fedme en trussel mot helse og lang levetid, men det kan også føre til at forsøkspersoner avslutter sin antipsykotiske medisinering7.
både ziprasidon og olanzapin er effektive atypiske antipsykotika som ofte brukes ved behandling av schizofreni og schizoide lidelser. Atypiske antipsykotika viser bedre effekt og mindre negative bivirkninger enn typiske antipsykotika8,9. Imidlertid er de fortsatt tilbøyelige til å forårsake uønskede effekter, inkludert hypostatisk hypotensjon10, somnolens11, vektøkning1, 2, dyslipidemi12, hyperglykemi og diabetes mellitus5 og hyperprolaktinemi, som kan generere fertilitetsproblemer, seksuell dysfunksjon og redusert benmineraltetthet13,14.
Tidligere studier har ikke vist noen endringer i vekt eller metabolisme hos personer behandlet med ziprasidon1,2, 15, Ziprasidon viser lav tilbøyelighet til å forårsake ekstrapyramidale bivirkninger (EPS) eller laboratorieavvik8,16,17, og påvirker ikke den seksuelle funksjonen til schizofrene pasienter18 negativt. Ziprasidon har blitt rapportert å forårsake vekttap og reduksjon i serum lipid nivåer 19, 20.Olanzapin Er et av de mest foreskrevne antipsykotiske legemidlene, med påvist effekt for schizofrenisymptomer21-23. Olanzapin er imidlertid blant de atypiske antipsykotiske legemidlene som induserer vektøkning24, 25, og er også forbundet med betydelige økninger i totalt kolesterol, triglyserider, LDL og fastende insulin20,26,27. I tidligere studier som sammenlignet ziprasidon vs. olanzapin, utelukkende eller kombinert med annen behandling, viste olanzapin signifikant større økning i vekt og BMI og en høyere sannsynlighet for rask vektøkning enn noen annen behandling7,20,26,27. Alle disse studiene hadde imidlertid en effektvariabel som primærvariabel, ettersom vektvurdering bare var en del av sikkerhetsstudien.
Antipsykotiske behandlinger er ofte langsiktige, og det er nødvendig å vurdere økt risiko for metabolske endringer i pasientbehandlingen. Derfor ble denne randomiserte, dobbeltblinde studien designet for å spesifikt ta opp spørsmålet om vektøkning på lang sikt (6 måneder), dette er den primære variabelen. Også, med tanke på at andre faktorer er relatert til pasientens disposisjon og overholdelse av behandlingen, vurderte denne studien livskvalitet, generell funksjon, preferanser og holdning til behandling, for å gi mer informasjon om problemer som skal behandles i disse langsiktige behandlingene og for å diskutere deres forhold til hovedformålet.En seks måneders randomisert, multisenter, parallell, dobbeltblind studie ble utført fra April 2003 til februar 2007 for å estimere og sammenligne effekten av ziprasidon versus olanzapin på kroppsvekt ved behandling av personer med schizofreni.
studien ble utført på 11 sentre Over Hele Spania. Mannlige eller kvinnelige forsøkspersoner i alderen 18-70 år med en primærdiagnose av schizofreni, I HENHOLD TIL DSM-IV-TR28, og en klinisk tilstand som krever oppstart av behandling med et nytt antipsykotisk legemiddel ble inkludert. Pasienter, eller deres juridiske representant, ga sitt informerte samtykke. Eksklusjonskriterier: anamnese med klinisk signifikant fysisk sykdom eller ekg-abnormaliteter (F. eks. QTc> 500 ms), klinisk signifikante unormale laboratorieverdier, epilepsi, krampeanfall, psykokirurgi, manglende respons eller tidligere intoleranse overfor olanzapin eller ziprasidon; graviditet eller amming; serologiske tegn PÅ HIV eller hepatitt; behandling med begge legemidlene innen 6 måneder før screening; pasient som ikke er i stand til eller har vanskeligheter med å overholde studieprotokollen.; umiddelbar risiko for å begå skade på seg selv eller andre; samtidig behandling med antipsykotiske midler etter randomisering; depot antipsykotisk medisinering innen en måned etter innreise; behandling med antidepressiva eller stemningsstabilisatorer innen to uker etter randomisering; rusmisbruk innen tidligere 3 måneder; organisk psykisk sykdom; behandling med kliniske legemidler innen 30 dager før randomisering.studien ble utviklet i samsvar Med Helsinki29-erklæringen, og studieprotokollen ble godkjent av De Etiske Komiteene som svarer til de involverte sentrene og Av Legemiddel Til Human Bruk Avdeling for Medisin og Helseprodukter spansk Byrå (aemps).
Forsøkspersoner ble inkludert i studien 12 timer etter forrige antipsykotiske dose, med unntak av forsøkspersoner behandlet med depot antipsykotiske (se ovenfor), og ble tilfeldig fordelt i forholdet 1:1.
behandlingsdose og besøksplan
Dosering var fleksibel innen 3 nivåer: Lav (ziprasidon 40 mg TO GANGER ELLER olanzapin 5 mg TO GANGER), Medium (ziprasidon 60 mg TO GANGER ELLER olanzapin 15 mg DAGLIG) Og Høy (ziprasidon 80 mg TO GANGER ELLER olanzapin 10 mg TO GANGER DAGLIG). Behandlingen ble initiert med lav dose i dag 1-7, og fra dag 3 og utover kunne dosen justeres.behandlingsfasen (6 måneder) inkluderte 6 besøk: Dag 1 (Uke 0), Uke 1, Uke 4, Uke 12, Uke 18 og Uke 24. Oppfølgingsbesøk (Uke 48) utføres seks måneder etter avsluttet behandling. Studiemedisin ble rapportert fra besøk 1 til 6. Pasienter som viste utilstrekkelig respons på noe tidspunkt i løpet av studien, som indikert av Et Klinisk Globalt Inntrykk Av Forbedring (CGI-I) score på ≥ 6, ble trukket tilbake.
Effekt-og sikkerhetsvurderinger
de målte effektresultatene var vekt, BMI og midjeomkrets (WC); blodtrykk og puls; positive and negative syndrome scale (PANSS)30; Clinical Global Impression (CGI) scale31 og en annen for forbedring (CGI-I); pasientens fysiske aktivitet; patient preference scale (PPS) , for å måle pasientens tilfredshet med medisinering; den spanske versjonen Av Health Utilities Index-Mark 3 (HUI-3) 32,22. Appetitt ble målt ved en visuell analog skala( VAS), en subjektiv kvantifiseringsmetode. Pasienten markerer sin appetitt nivå siden siste besøk på en horisontal linje merket 0 (ingen appetitt) venstre og 10 (ekstremt sulten) til høyre. Avstanden fra 0 måles deretter i cm og appetittnivå kvantifiseres.
alle effektresultater ble vurdert ved visit 1 (baseline-verdier) og i tillegg: CGI-S, CGI-I og PANSS fra visit 2 til 7, appetitt og pasientens fysiske aktivitet fra visit 3 til 6, PPS og HUI-3 ved visit 4 og 6
sikkerhetsevalueringer inkluderte klinisk monitorering, elektrokardiogram, vitale tegn, bivirkninger (aes) og sikkerhetslaboratorietester. Sikkerhetsvurderinger ble rapportert i Henhold Til Worldwide Safety Standards (Wss) Versjon 3 krav.
Statistisk analyse
alle analyser ble utført på intent-to-treat (itt) – populasjonen ved BRUK AV SAS® versjon 8.2 eller høyere. Statistiske tester var 2 tailed og p-verdier på 0.05 eller mindre ble vurdert som statistisk signifikante. Behandlingen ble montert som en kategorisk. 95% konfidensintervall (KI) ble konstruert rundt alle estimerte behandlingsforskjeller. Alle endringer ble analysert ved analyse av kovarians (ANCOVA), inkludert effekter for behandlingsgruppen og baseline verdi (hvis aktuelt). Beskrivende statistikk ble brukt for å oppsummere alle sikkerhetsvurderinger. Bivirkninger ble kodet i Henhold Til Medical Dictionary for Regulatory Activities (Meddra). Ingen formell statistisk testing ble utført på sikkerhetsparametere.
Resultater
individuell disposisjon og legemiddeldose
selv om studien opprinnelig var ment for 112 pasienter, ble bare 58 pasienter screenet i studieperioden. Til slutt ble 50 itt-pasienter inkludert: 27 til ziprasidon og 23 til olanzapin. I løpet av studieperioden avsluttet totalt 29 pasienter behandlingen (19 i ziprasidongruppen og 10 i olanzapin). Selv om de fleste seponeringer ikke var relatert til studielegemidlet, skyldtes 2 (ett i hver gruppe) manglende effekt og 7 (5 i ziprasidon og 2 i olanzapin) legemiddelrelaterte bivirkninger. Median behandlingsvarighet var lavere for ziprasidon (52,5 dager ) enn for olanzapin-gruppen (164 dager; 32% av pasientene i ziprasidon-gruppen og 58% i olanzapin fullførte studien.
i behandlingsfasen fikk pasienter på ziprasidon en gjennomsnittlig dose på 107,4 ± 27,3 mg / dag, og pasienter på olanzapin fikk en gjennomsnittlig dose på 15 ± 3,3 mg / dag.
baseline karakteristika
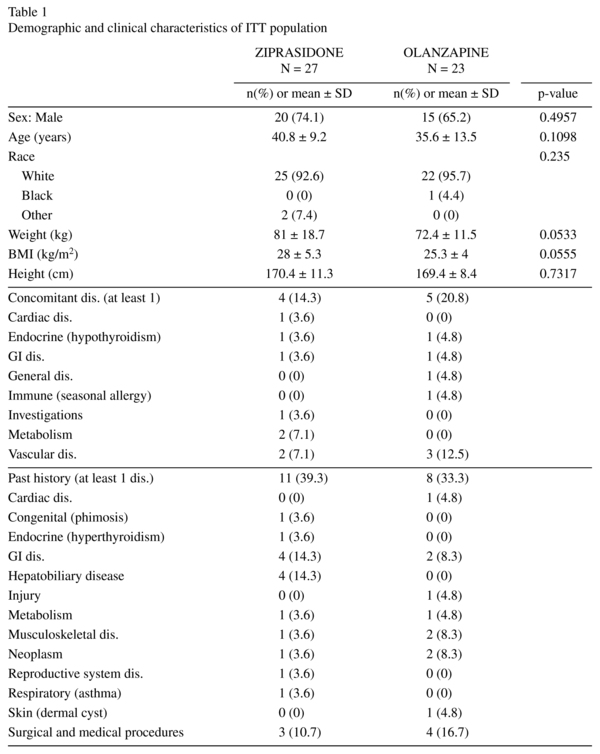
Demografiske karakteristika var homogene mellom begge gruppene og viste ingen signifikante forskjeller. Itt-pasientene var i alderen 19-63 år, de fleste mellom 18-44 år. Detaljerte demografiske data er gitt i tabell 1. Tilsvarende antall forsøkspersoner i begge behandlingsgruppene fikk samtidig legemiddelbehandling i løpet av studien (26 i ziprasidon og 21 i olanzapingruppen). De hyppigst brukte (av ≥ 5 personer i begge behandlingsgruppene) i begge behandlingsgruppene var lorazepam, lormeta-zepam og risperidon.
Effekter på Vektøkning
Kroppsvekten var stabil ved uke 24 i ziprasidongruppen, og viste ingen signifikant forskjell med basal vekt (-0,1% prosent reduksjon; n.s.) mens det var en statistisk signifikant økning fra baseline i olanzapingruppen (7,4% prosent økning i kroppsvekt fra baseline, p < 0,0001) (Tabell 2). Forskjellen mellom behandlingsgruppene i endring i kroppsvekt fra baseline var statistisk signifikant på alle tidspunkter, og olanzapinbehandlede pasienter viste signifikant vektøkning fra baseline ved alle besøk (Tabell 2). Antall forsøkspersoner som hadde 7% vektøkning ved uke 24 var signifikant lavere i ziprasidon (n = 3 ) enn i olanzapingruppen (n = 11) (OR = 6,246; p = 0.0150). Forskjellen mellom behandlingsgruppene var også tydelig ved uke 12 (p = 0,0266) og 18 (p = 0,0261) (data ikke vist).

de sekundære endepunktene ved uke 24 er oppsummert i Tabell 3. Ziprasidonbehandlede pasienter opplevde ingen signifikant endring I WC og BMI ved 24 uker, mens olanzapinbehandlede pasienter fikk en signifikant økning i begge parametrene, noe som resulterte i en signifikant forskjell i 24-ukers LSM (least square means) av begge verdier mellom gruppene.

Effektresultater
Ziprasidonbehandling resulterte i en signifikant reduksjon (dvs. forbedring) AV PANNS-n og olanzapin i en signifikant reduksjon av ALLE PANNS-delskalaer. Alle reduksjoner var signifikant større i olanzapin enn i ziprasidongruppen. Det var imidlertid ingen signifikant forskjell i antall pasienter som opplevde bedring av schizofrenisymptomer mellom gruppene, vurdert med PANNS (7) ziprasidon vs. 11 olanzapin; p = 0,1385). PÅ cgi-s-skalaen var 19 pasienter i ziprasidongruppen og 16 i olanzapin moderat til markert syke ved baseline; ved 24 uker var det henholdsvis 19 og 12 pasienter (data ikke vist). PÅ cgi-i-skalaen var 5 pasienter i ziprasidongruppen og 4 i olanzapin «mye bedre» og 1 i ziprasidon og 4 i olanzapin «veldig mye bedre» etter 24 uker (data ikke vist). Pasienter behandlet med olanzapin hadde bedre karakterer for symptomforverring (CGI-S) (OR: 3,321, p = 0,0286) og forbedring (CGI-I) (OR: 3,512, p = 0.0307) ved uke 24 enn de som ble behandlet med ziprasidon. Det var imidlertid ingen signifikante forskjeller i antall pasienter som viste forbedring I CGI-S (4 på ziprasidon vs. 7 på olanzapin; p = 0,2379) og CGI-I (6 på ziprasidon vs. 8 på olanzapin; p = 0,2823) mellom gruppene. Bedre tilfredshet med medisinering, målt i PPS, ble observert i ziprasidongruppen enn i olanzapingruppen (p = 0,0161). Som vist i Tabell 4, reduserte appetitten også signifikant hos pasienter behandlet med ziprasidon, mens den økte noe i olanzapingruppen. Selv om appetittøkning i sistnevnte ikke nådde statistisk signifikans, var endringen statistisk forskjellig mellom behandlingsgruppene. Det var ingen signifikante forskjeller mellom behandlingsgruppenes blodtrykk og hjertefrekvens.

Sikkerhetsresultater
Ingen dødsfall ble rapportert i denne studien. Bivirkninger under denne studien og laboratorietester er oppsummert i Tabell 5. Halvparten AV BIVIRKNINGENE i hver gruppe var behandlingsrelaterte (ziprasidon: sedasjon, angst, rastløshet, schizofreni og hypersomni; olanzapin: schizofreni, rastløshet). Tjueen behandlingsrelaterte Bivirkninger ble opplevd av 15 pasienter (53,6%) i ziprasidongruppen og 11 av 8 pasienter (33,3%) i olanzapingruppen.

Diskusjon
I henhold til studieprotokollen bør 78 pasienter (39 i hver gruppe) ha blitt evaluert for en statistisk effekt på 80% for å oppdage en forskjell på 5 kg, estimere EN SD = 7,7. Den endelige itt-populasjonen inkludert var imidlertid 50 pasienter. Selv om dette kunne ha representert en begrensning, var forskjellen i kroppsvekt mellom grupper ved 24 uker 7,5% (SD = 4,5). Kraften var 99% og resultatet var bedre enn opprinnelig planlagt.
i samsvar med tidligere studier var kroppsvekten stabil i ziprasidongruppen, mens det var en statistisk signifikant økning fra baseline i olanzapin-gruppen ved hvert tidspunkt6,7. Følgelig opplevde ziprasidonbehandlede pasienter ingen signifikant endring I WC og BMI, mens olanzapinbehandlede pasienter fikk en signifikant økning i både parametere og vekt. I en tidligere studie34 var prosentandelen av olanzapinbehandlede pasienter med ≥ 7% vektøkning enda høyere: 60% av pasientene ved 3 måneder som økte til 80% etter 1 års olanzapinbehandling. Olanzapindosen i den nevnte studien var lik eller lavere enn i vår studie. Dette er ikke overraskende, siden dosen ikke har vært relatert til olanzapin vektøkning, men relatert til terapeutisk respons25. Pasienter med maksimal effekt av olanzapin på symptomer er også de med høyest risiko for signifikant vektøkning.
Variasjoner i matinntak har blitt foreslått som en mulig årsak til disse effektene på vekt. I denne studien ble appetitten signifikant redusert hos pasienter behandlet med ziprasidon, mens ingen signifikant endring i olanzapin ble rapportert. Appetittstimulering er sterkt korrelert med antipsykotisk legemiddelaffinitet for h1-og alfa1-adrenerge reseptorer35, og appetittreduksjon hos pasienter behandlet med ziprasidon er sannsynligvis forbundet med stoffets lave affinitet For H1-reseptor. De olanzapinbehandlede pasientene viste ingen signifikant økning i appetitt, men viste likevel en signifikant økning i kroppsvekt, noe som tyder på at andre mekanismer kan være involvert i olanzapinindusert vektøkning. Tschoner et al. det ble funnet høyere fastende glukose og økt skår i en insulinresistensmodell hos pasienter behandlet med olanzapin, mens denne effekten ikke kunne observeres hos pasienter behandlet med ziprasidon, noe som indikerer at denne effekten var involvert i olanzapinindusert vektøkning6. Dyrestudier har vist at olanzapin, men ikke ziprasidon, stimulerer forbruket av fat36 og at kronisk behandling med olanzapin svekker lipolyse av adipocytter37. Tidligere studier har også funnet at kolesterol, triglyserider og LDL-kolesterol øker hos olanzapinbehandlede pasienter, og ikke hos ziprasidonbehandlede individer6, 38. Fysisk aktivitet er signifikant redusert hos olanzapinbehandlede pasienter39, 40, MEN OR av fysisk trening i denne studien favoriserer olanzapin betydelig fremfor ziprasidonbehandlede pasienter og forklarer derfor ikke forskjellen i vektøkning.
olanzapinbehandlede pasienter viste signifikant bedre resultater i PANNS-delskalaer enn de som ble behandlet med ziprasidon, noe som bekreftet resultater fra en tidligere studie20. Deltakerne i den studien hadde avsluttet en tidligere behandling på grunn av intoleranse, noe som vanskeliggjorde sammenligningen med vår nåværende studie. Dosen av ziprasidon var lik, men olanzapindosen var høyere. Olanzapin viser økende dose-responskurver for schizofrenisymptomer 21, 41, noe som kan forklare den større forbedringen AV PANNS sammenlignet med ziprasidon i studien med høyere olanzapindose. Olanzapindoser høyere enn 20 mg / dag er imidlertid beskrevet for å gi større risiko for viktige bivirkninger 42, 43.
i kontrast fant to andre studier ingen forskjell i effekt mellom behandlingene. Studien utført Av Lieberman et al.7 viste ingen signifikante forskjeller i PANNS totalskårendring fra baseline eller mellom olanzapin og ziprasidon. På samme måte, studien Av Simpson et al. viste ingen forskjeller i PANNS score forbedring mellom grupper26, 27. Disse studiene brukte lignende fleksible doser som de vi brukte, fant samme effekt med enten olanzapin-eller ziprasidonbehandling. En plausibel forklaring kan være at selv om ziprasidon er indisert for behandling av schizofreni i et doseområde på 40-160 mg / dag, er den optimale dosen nærmere 120 mg / dag44, og gjennomsnittsdosen i studien vår, litt lavere enn gjennomsnittsdosene i de to andre studiene, kanskje ikke har vært optimal. Videre kan den biotilgjengelige dosen ha vært enda lavere. Selv om ziprasidon plasmanivå viser en signifikant positiv korrelasjon med reseptorbelastning, forutsier ikke dosen plasmanivå44, siden mat kan forstyrre ziprasidonabsorpsjon45, påvirker kan avhenge av medisinering timing.
det var 1,6 ganger flere behandlingsavbrudd i ziprasidon enn i olanzapin-gruppen, noe som viste en høyere foldeforskjell mellom begge behandlingene enn i andre studier7,20. De fleste Bivirkningene var milde eller moderate i begge gruppene og inkluderte bivirkninger som vanligvis ble observert med disse legemidlene 20, 34. PPS-skala indikerer at pasienter foretrakk ziprasidon fremfor olanzapin.
denne studien viser en signifikant større økning i kroppsvekt ved uke 24 hos pasienter behandlet med olanzapin sammenlignet med pasienter behandlet med ziprasidon. Den rapporterte progressive appetittreduksjonen kan ha bidratt til en svak reduksjon i kroppsvekt observert hos pasienter behandlet med ziprasidon. På den annen side indikerte pasienter på olanzapin en viss økning i appetitten, men endringer i denne gruppen var ikke signifikante og viste ikke den progressive økningen i variasjon som ziprasidon-pasienter rapporterte. Den visuelle analoge skalaen er en subjektiv metode for å måle appetitt, og selv om forskjeller i appetitt var signifikante og resultatene syntes bestatt under studien, synes noe økt appetitt eller mangel på mosjon ikke ansvarlig for vektøkningen opplevd av olanzapinbehandlede pasienter, noe som tyder på andre mekanismer. Fettmatpreferanse og metabolsk dysregulering kan spille en rolle i den underliggende årsaken. Både ziprasidon-og olanzapingruppene ble godt tolerert og VISTE en reduksjon I PANSS-score ved uke 24. Selv om reduksjonen var signifikant større for alle skår i olanzapin-gruppen, kan muligheten for redusert biotilgjengelighet av ziprasidon ikke utelukkes.
hos pasienter hvor vektøkning under behandling av schizofreni kan være et problem, bør behandling med ziprasidon forsøkes på grunn av sin gode sikkerhetsprofil på dette feltet.Medisinsk skriftlig støtte ble gitt Av Medical Statistics Consulting og ble finansiert Av Pfizer.
1. Allison DB, Fontaine KR, Heo M, Mentore JL, Cappelleri JC, Chandler LP, et al. Fordelingen av kroppsmasseindeks blant personer med og uten schizofreni. J Clin Psykiatri 1999; 60 (4): 215-220.
2. Baptista T, De Mendoza S, Beaulieu S, Bermudez A, Martinez M. metabolsk syndrom under atypisk antipsykotisk behandling: mekanismer og ledelse. Metab Syndr Relatert Disord 2004; 2 (4): 290-307.
3. Enger C, Weatherby L, Reynolds RF, Glasser DB, Walker AM. Alvorlige kardiovaskulære hendelser og dødelighet blant pasienter med schizofreni. J Nerv Ment Dis 2004; 192(1): 19-27.
4. Allison DB, Mentore JL, Heo M, Chandler LP, Cappelleri JC, Infante MC, Et al. Antipsykotisk indusert vektøkning: en omfattende forskningssyntese. Am J Psykiatri 1999; 156 (11): 1686-1696.
5. Kane JM, Barrett EJ, Casey DE, Correll CU, Gelenberg AJ, Klein S, Et al. Metabolske effekter av behandling med atypiske antipsykotika. J Clin Psykiatri 2004; 65 (11): 1447-1455.
6. Tschoner A, Engl J, Rettenbacher M, Edlinger M, Kaser S, Tatarczyk T, et al. Effekter av seks andre generasjons antipsykotika på kroppsvekt og metabolisme – risikovurdering og resultater fra en prospektiv studie. Farmakopsykiatri 2009; 42 (1): 29-34.
7. Lieberman JA, Stroup TS, McEvoy JP, Swartz MS, Rosenheck RA, Perkins DO, et al. Effekt av antipsykotiske legemidler hos pasienter med kronisk schizofreni. N Engl J Med 2005; 353 (12): 1209-1223.
8. King DJ. Narkotikabehandling av de negative symptomene på schizofreni. Eur Neuropsykofarmakol 1998; 8(1): 33-42.
9. Weiden P, Aquila R, Standard J. Atypiske antipsykotiske legemidler og langsiktig utfall i schizofreni. J Clin Psykiatri 1996; 57 (Suppl 11): 53-60.
10. Drici MD, Priori S. Kardiovaskulær risiko ved atypisk antipsykotisk behandling. Pharmacoepidemiol Narkotika Saf 2007; 16 (8): 882-890.
11. Gao K, Ganocy SJ, Gajwani P, Muzina DJ, Kemp DE, Calabrese JR. en gjennomgang av følsomhet og toleranse for antipsykotika hos pasienter med bipolar lidelse eller skizofreni: fokus på somnolens. J Clin Psykiatri 2008; 69 (2): 302-309.
12. Nasrallah HA. Atypiske antipsykotiske induserte metabolske bivirkninger: innsikt fra reseptorbindende profiler. Mol Psykiatri 2008; 13(1): 27-35.
13. Baldwin D, Mayers A. Seksuelle bivirkninger av antidepressiva og antipsykotiske legemidler. Adv Psychiatr Behandle 2003; 9(3): 202-210.
14. Montejo AL. Prolactin bevissthet: en viktig faktor for fysisk helse i schizofreni. Eur Nevropsykofarmakol 2008; 18 (Suppl 2): S108-114.
15. Keck PE, Jr., Mcelroy SL, Arnold LM. Ziprasidon: et nytt atypisk antipsykotisk middel. Ekspert Opin Pharmacother 2001; 2 (6): 1033-1042.
16. Kane JM, Khanna S, Rajadhyaksha S, Giller E. effekt og toleranse av ziprasidon hos pasienter med behandlingsresistent schizofreni. Int Clin Psychopharmacol 2006; 21(1): 21-28.
17. Keck P, Jr., Buffenstein A, Ferguson J, Feighner J, Jaffe W, Harrigan EP, et al. Ziprasidon 40 og 120 mg / dag ved akutt forverring av schizofreni og schizoaffektiv lidelse: en 4-ukers placebokontrollert studie. Psykofarmakologi (Berl)) 1998; 140(2): 173-184.
18. Montejo AL, Rico-Villademoros F. Endringer i seksuell funksjon hos polikliniske pasienter med schizofreni eller andre psykotiske lidelser behandlet med ziprasidon i klinisk praksis: en 3-måneders prospektiv observasjonsstudie. J Clin Psychopharmacol 2008; 28 (5): 568-570.
19. St. Hanshaugen, J. M., St. Hanshaugen D., Zada J., Simpson GM. De tilsynelatende effektene av ziprasidon på plasmalipider og glukose. J Clin Psykiatri 2001; 62 (5): 347-349.
20. Ragnhild RAGNAR et al. Effekt av olanzapin, kvetiapin, risperidon og ziprasidon hos pasienter med kronisk schizofreni etter seponering av et tidligere atypisk antipsykotikum. Er J Psykiatri 2006; 163 (4): 611-622.
21. Beasley CM, Jr., Tollefson G, Tran P, Satterlee W, Sanger T, Hamilton S. Olanzapin versus placebo og haloperidol: akuttfaseresultater fra den nordamerikanske dobbeltblinde olanzapinstudien. Neuropsykofarmakologi 1996; 14 (2): 111-123.
22. Conley RR, Mahmoud R. En randomisert dobbeltblind studie av risperidon og olanzapin ved behandling av schizofreni eller schizoaffektiv lidelse. Er J Psykiatri 2001; 158 (5): 765-774.
23. Gomez JC, Crawford AM. Overlegen effekt av olanzapin over haloperidol: analyse av pasienter med schizofreni fra en internasjonal multisenterstudie. J Clin Psykiatri 2001; 62 (Suppl 2): 6-11.
24. Bobes J, Rejas J, Garcia-Garcia M, Rico-Villademoros F, Garcia-Portilla MP, Fernandez I, et al. Vektøkning hos pasienter med schizofreni behandlet med risperidon, olanzapin, kvetiapin eller haloperidol: resultater FRA EIRE-studien. Schizophr Res 2003; 62 (1-2): 77-88.
25. Kinon BJ, Kaiser CJ, Ahmed S, Rotelli MD, Kollack-Walker S. Sammenheng mellom tidlig og rask vektøkning og endring i vekt over ett år med olanzapinbehandling hos pasienter med schizofreni og relaterte lidelser. J Clin Psychopharmacol 2005; 25 (3): 255-258.
26. Simpson GM, Glick ID, Weiden PJ, Romano SJ, Siu CO. Randomisert, kontrollert, dobbeltblind multisenter-sammenligning av effekt og toleranse av ziprasidon og olanzapin hos akutt syke pasienter med schizofreni eller schizoaffektiv lidelse. Am J Psykiatri 2004; 161 (10): 1837-1847.
27. Simpson GM, Weiden P, Pigott T, Murray S, Siu CO, Romano SJ. Seks måneders, blindet, multisenter fortsettelsesstudie av ziprasidon versus olanzapin ved schizofreni. Er J Psykiatri 2005; 162 (8): 1535-1538.
28. American Psychiatric Association (Engelsk). American Psychiatric Association (Engelsk). Task Force på DSM-IV. Diagnostisk og statistisk håndbok for psykiske lidelser: DSM-IV-TR. 4.utg. Washington, DC: American Psychiatric Association; 2000.
29. WMA. Helsinkideklarasjonen: etiske prinsipper for medisinsk forskning som involverer mennesker. J Postgrad Med. 2002; 48(3): 206-208.
30. Kay SR, Fiszbein A, Opler LA. POSITIV og negativ syndrom skala (PANSS) for schizofreni. Schizophr Bull 1987; 13(2): 261-276.
31. Guy W, Nasjonalt Institutt For Mental Helse (USA). Psychopharmacology Research Branch (Engelsk). Tidlig Klinisk Legemiddelevalueringsprogram. ECDEU assessment manual for psykofarmakologi. Pastor ed. Rockville, Md.: U. S. Dept. Av Helse, Utdanning og Velferd, Offentlig Helsetjeneste, Alkohol, Narkotikamisbruk Og Psykisk Helseadministrasjon, Nasjonalt Institutt For Mental Helse, Psykofarmakologisk Forskningsavdeling, Divisjon For Ekstramural Forskningsprogrammer; 1976.
32. Feeny D, Furlong W, Boyle M, Torrance GW. Multi-attributt helsestatus klassifiseringssystemer. Health Utilities Index (Engelsk). Farmakoøkonomi 1995; 7 (6): 490-502.
33. Ruiz M, Rejas J, Soto J, Pardo A, Rebollo I. Tilpasning og validering Av Health Utilities Index Mark 3 til spansk og korreksjonsnormer for spansk befolkning. Med Clin (Barc)) 2003; 120(3): 89-96.
34. McEvoy JP, Lieberman JA, Perkins DO, Hamer RM, Gu H, Lazarus A, et al. Effekt og toleranse av olanzapin, kvetiapin og risperidon ved behandling av tidlig psykose: en randomisert, dobbeltblind 52-ukers sammenligning. Am J Psykiatri 2007; 164 (7): 1050-1060.
35. Baptista T, Zarate J, Joober R, Colasante C, Beaulieu S, Paez X, et al. Drug indusert vektøkning, et hinder for vellykket farmakoterapi: fokus på antipsykotika. Curr Narkotika Mål 2004; 5 (3): 279-299.
36. Hartfield AW, Moore NA, Clifton PG. Effekter av atypiske antipsykotiske legemidler på intralipidinntak og kokainindusert hyperaktivitet hos rotter. Neuropsykofarmakologi 2006; 31 (9): 1938-1945.
37. Minet-Ringuet J, Selv PC, Betjent P, Carpene C, Visentin V, Prevot D, et al. Endringer i lipidmetabolisme og genuttrykk i rotteadipocytter ved kronisk olanzapinbehandling. Mol Psykiatri 2007; 12(6): 562-571.
38. Jørgensen, Jørgensen C, Jørgensen A, Jørgensen G, Jørgensen m, Et al. Tidlige endringer av plasmalipider under behandling med atypiske antipsykotika. Int Clin Psychopharmacol 2006; 21 (6): 369-372.
39. Mj, Anjum N, Dickinson K, Marshall KM, Peltola LM, Vickers S, et al. De distinkte effektene av subkronisk antipsykotisk legemiddelbehandling på makronæringsstoffvalg, kroppsvekt, fedme og metabolisme hos hunnrotter. Psykofarmakologi (Berl)) 2007; 194(2): 221-231.
40. C, Heiser P, Hennighausen K, Herpertz-Dahlmann B, Holtkamp K, Mehler-Wex C, Et al. Klinisk legemiddelovervåking i barne-og ungdomspsykiatri: bivirkninger av atypiske nevroleptika. J Barn Adolesc Psychopharmacol 2006; 16(3): 308-316.
41. Fanous A, Lindenmayer JP. Schizofreni og schizoaffektiv lidelse behandlet med høye doser olanzapin. J Clin Psychopharmacol 1999; 19 (3): 275-276.
42. Farah A. Atypicality av atypiske antipsykotika. Prim Care Folgesvenn J Clin Psykiatri 2005; 7 (6): 268-274.
43. Reich J. bruk av høydose olanzapin ved refraktær psykose. Er J Psykiatri 1999; 156 (4): 661.
44. Mamo D, Kapur S, Shammi CM, Papatheodorou G, Mann S, Therrien F, et al. EN PET-studie av dopamin D2 og serotonin 5-HT2-reseptorbelastning hos pasienter med schizofreni behandlet med terapeutiske doser ziprasidon. Er J Psykiatri 2004; 161 (5): 818-825.
45. Hamelin BA, Allard S, Laplante L, Miceli J, Wilner KD, Tremblay J, et al. Effekten av timing av et standardmåltid på farmakokinetikken og farmakodynamikken til det nye atypiske antipsykotiske stoffet ziprasidon. Farmakoterapi 1998; 18 (1): 9-15.