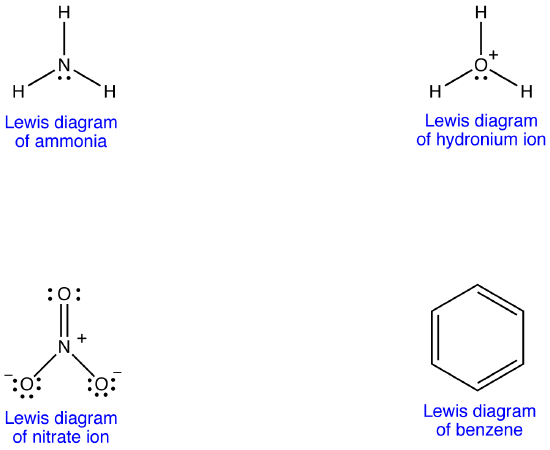
Le diagramme de Lewis de plusieurs molécules n’est cependant pas compatible avec les propriétés observées de la molécule.
Exemple 1: Ion nitrate
L’ion nitrate, selon son diagramme de Lewis, a deux types de liaisons azote-oxygène, une double liaison et deux liaisons simples, ce qui suggère qu’une liaison azote-oxygène dans l’ion nitrate est plus courte et plus forte que chacune des deux autres. De plus, la structure de Lewis implique, en ce qui concerne la charge formelle, qu’il existe deux types d’atomes d’oxygène dans l’ion nitrate, l’un formellement neutre et chacun des deux autres portant une charge formelle de -1. Expérimentalement, cependant, les trois liaisons azote-oxygène dans l’ion nitrate ont la même longueur de liaison et la même énergie de liaison, et les trois atomes d’oxygène sont indiscernables. Le diagramme de Lewis ne permet pas d’expliquer de manière satisfaisante la structure et la liaison de l’ion nitrate.
Deux diagrammes de Lewis supplémentaires peuvent être dessinés pour l’ion nitrate.
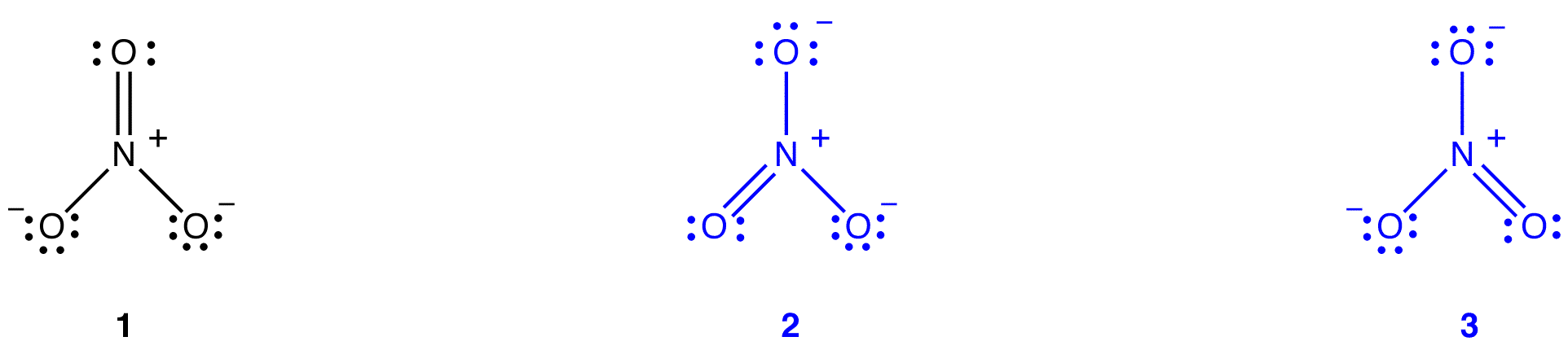
Cependant, aucun d’entre eux n’est compatible avec les propriétés observées de l’ion nitrate et, par conséquent, ne représente pas correctement l’ion nitrate.
Exemple 2: Benzène
Le benzène, selon son diagramme de Lewis, a deux types de liaisons carbone-carbone, trois doubles liaisons et trois liaisons simples, ce qui suggère que chacune des trois liaisons carbone-carbone dans le benzène est plus courte et plus forte que chacune des trois autres. Expérimentalement, cependant, les six liaisons carbone-carbone dans le benzène ont la même longueur de liaison et la même énergie de liaison. Le diagramme de Lewis ne permet pas d’expliquer de manière satisfaisante la structure et la liaison du benzène.
Un attribut des molécules dont le diagramme de Lewis classique n’est pas cohérent avec les propriétés observées est que d’autres diagrammes de Lewis valides peuvent être générés pour elles. Un diagramme de Lewis supplémentaire peut être dessiné pour le benzène.

Cependant, aucun d’entre eux ne correspond aux propriétés observées du benzène et, par conséquent, ne représente pas correctement le benzène.
La théorie de la résonance est une tentative d’expliquer la structure d’une espèce, comme l’ion nitrate ou le benzène, dont aucun diagramme de Lewis n’est compatible avec les propriétés observées de l’espèce. L’avantage majeur de la théorie de la résonance est que, bien que basée sur une analyse mathématique rigoureuse, la théorie de la résonance peut être appliquée avec succès en invoquant peu ou pas de mathématiques. La théorie de la résonance est expliquée ci-dessous en utilisant l’ion nitrate comme exemple.
Selon la théorie de la résonance, la structure de l’ion nitrate n’est pas 1, ni 2, ni 3, mais la moyenne des trois, pondérée par la stabilité. Les diagrammes de Lewis 1, 2 et 3 sont appelés formes de résonance, structures de résonance ou contributeurs de résonance de l’ion nitrate. La structure de l’ion nitrate est dite hybride de résonance ou, simplement, hybride des formes de résonance 1, 2 et 3. Chaque fois qu’il est nécessaire de montrer la structure de l’ion nitrate, les formes de résonance 1, 2 et 3 sont dessinées, reliées par une flèche à double tête.
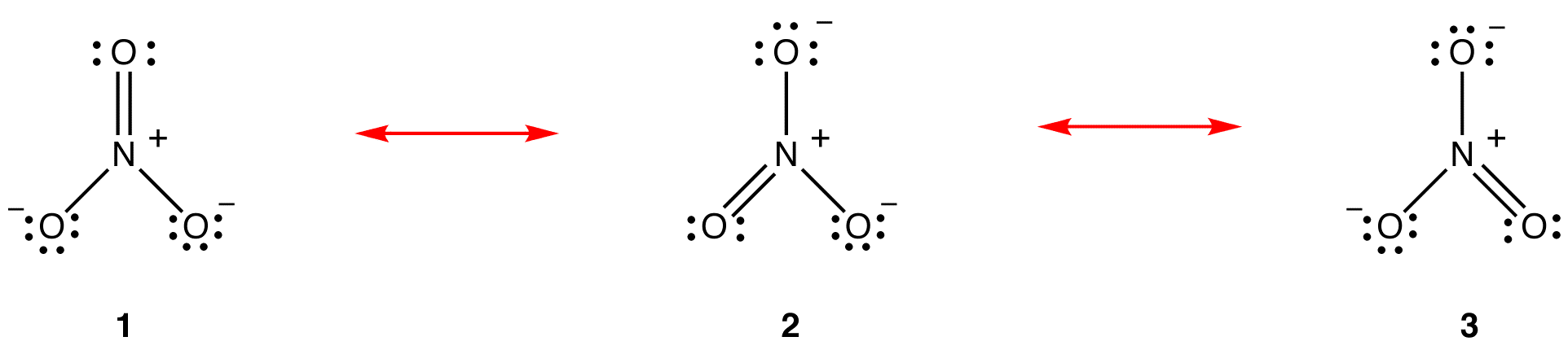
Les trois formes de résonance de l’ion nitrate, 1, 2 et 3, sont identiques, elles ont donc la même stabilité et, par conséquent, contribuent également à l’hybride. Étant donné que la mesure exacte dans laquelle chaque forme de résonance de l’ion nitrate contribue à l’hybride est connue, l’ordre de liaison de chaque liaison azote-oxygène ainsi que la charge formelle sur chaque atome d’oxygène dans l’hybride peuvent être facilement déterminés:
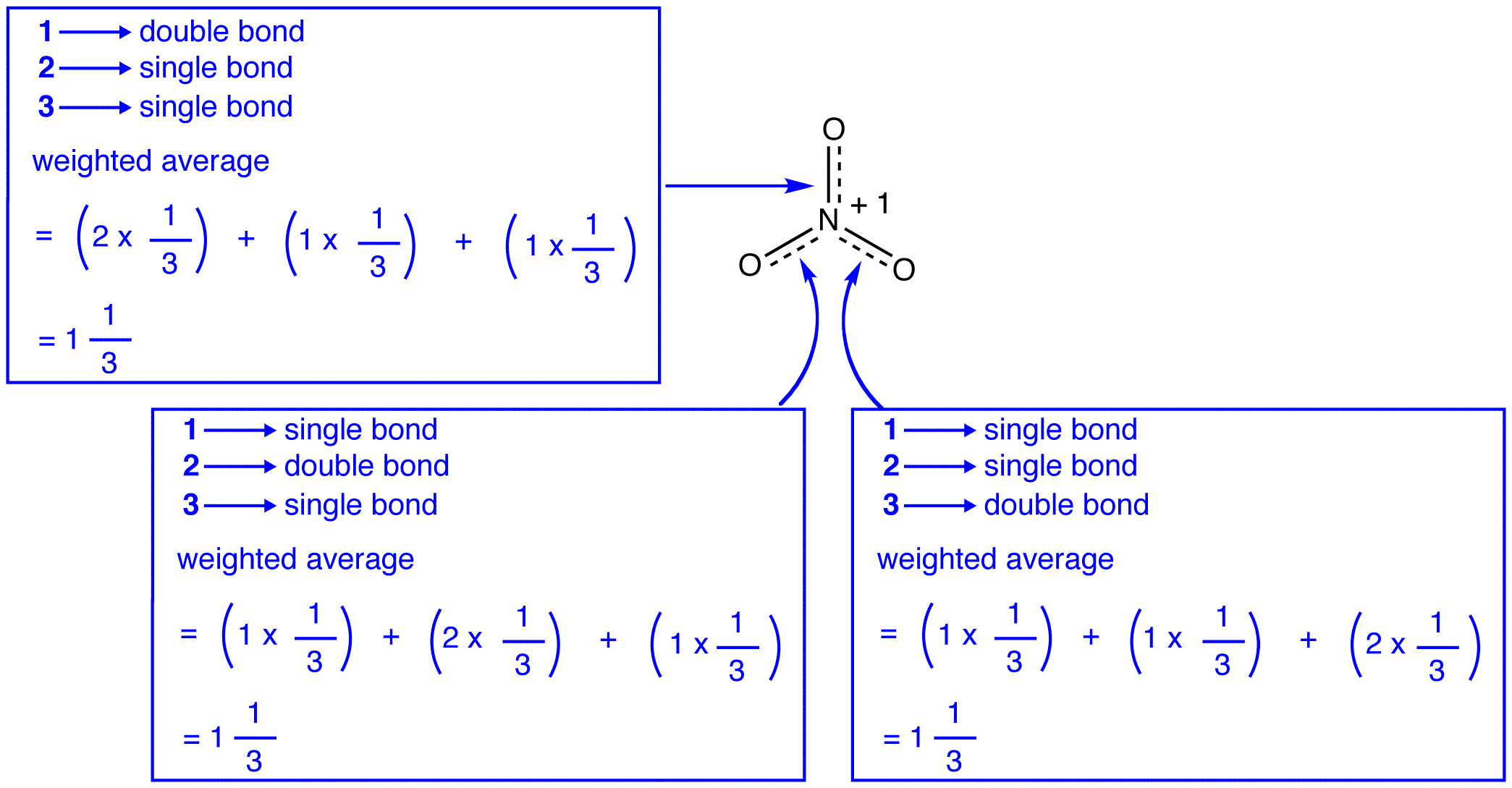
Selon la théorie de la résonance, chaque liaison dans l’ion nitrate est un et un tiers d’une liaison, ce qui est cohérent avec l’observation que les trois liaisons dans l’ion nitrate ont la même longueur de liaison et la même énergie de liaison.
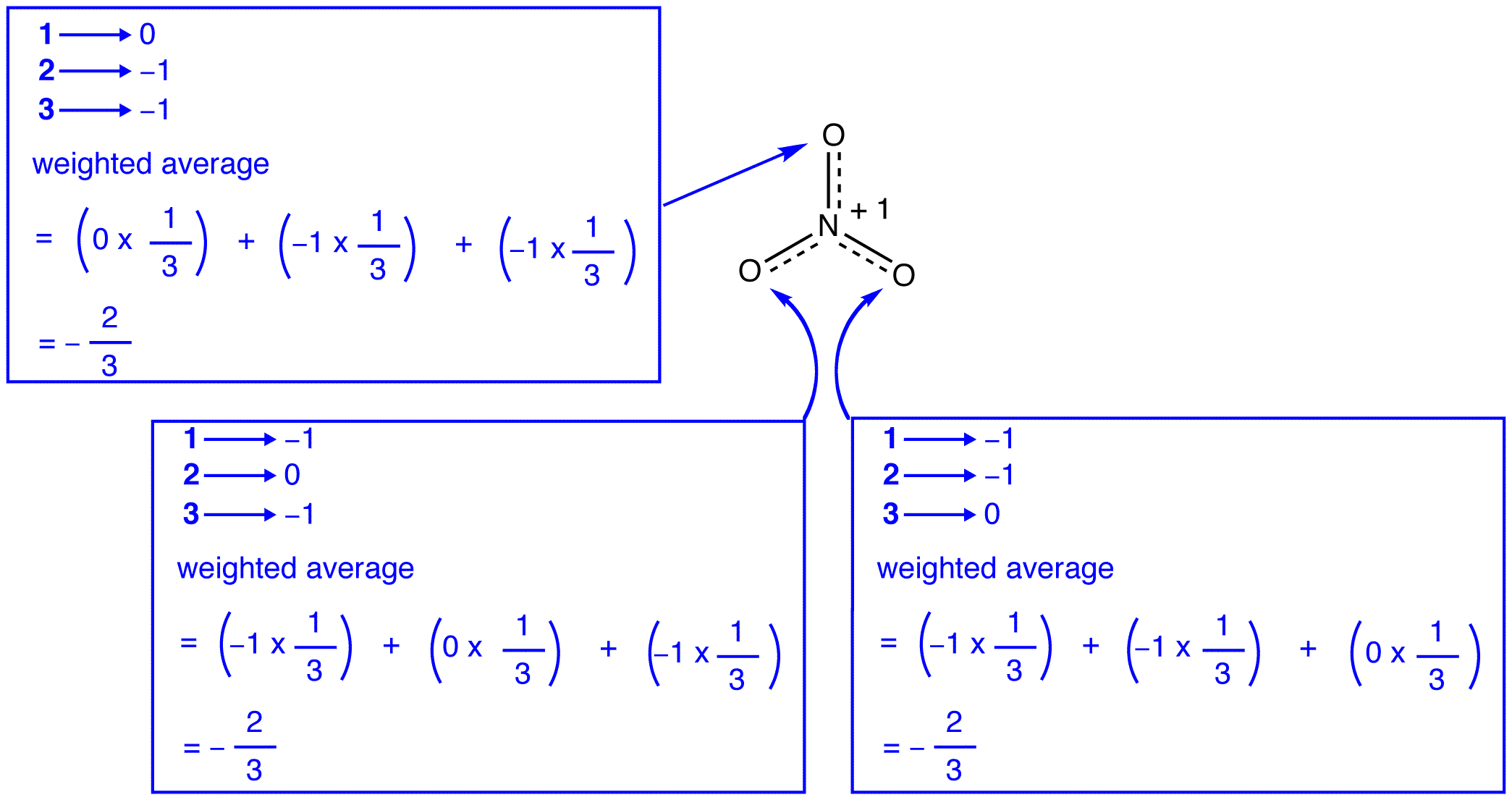
Selon la théorie de la résonance, chaque atome d’oxygène dans l’ion nitrate a une charge formelle de -2 /3, ce qui, en conjonction avec le fait que les trois liaisons azote-oxygène sont identiques, est cohérent avec l’observation que les trois atomes d’oxygène dans l’ion nitrate sont indiscernables.
Dans chaque forme de résonance de l’ion nitrate, il y a deux électrons pi, et ils ne sont partagés que par deux atomes. Un électron partagé seulement par deux atomes est dit localisé. Ainsi, les deux électrons pi dans chaque forme de résonance de l’ion nitrate sont localisés. L’ion nitrate, tel que représenté par l’hybride, a deux électrons pi :
# électrons dans une liaison pi = 2
# électrons dans un tiers d’une liaison pi = 2/3
# électrons dans trois d’entre eux = 3 x ( 2/3) = 2
Les deux électrons pi dans l’ion nitrate sont partagés par un total de quatre atomes, un atome d’azote et trois atomes d’oxygène. Un électron partagé par plus de deux atomes est dit délocalisé. Ainsi, les deux électrons pi dans l’ion nitrate sont délocalisés. La délocalisation des électrons pi dans l’ion nitrate nécessite que les quatre atomes soient sur le même plan, ce qui permet un chevauchement latéral des orbitales p sur eux.
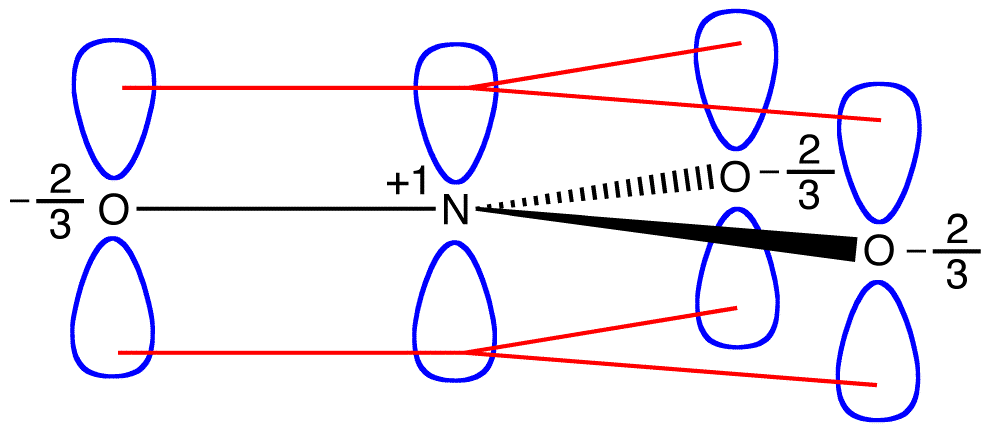
Si l’énergie de l’ion nitrate était la moyenne pondérée des énergies de ses trois formes de résonance, tout comme la structure de l’ion nitrate est la moyenne pondérée des structures de ses trois formes de résonance, elle devrait être égale à l’énergie de l’une des trois formes de résonance identiques:
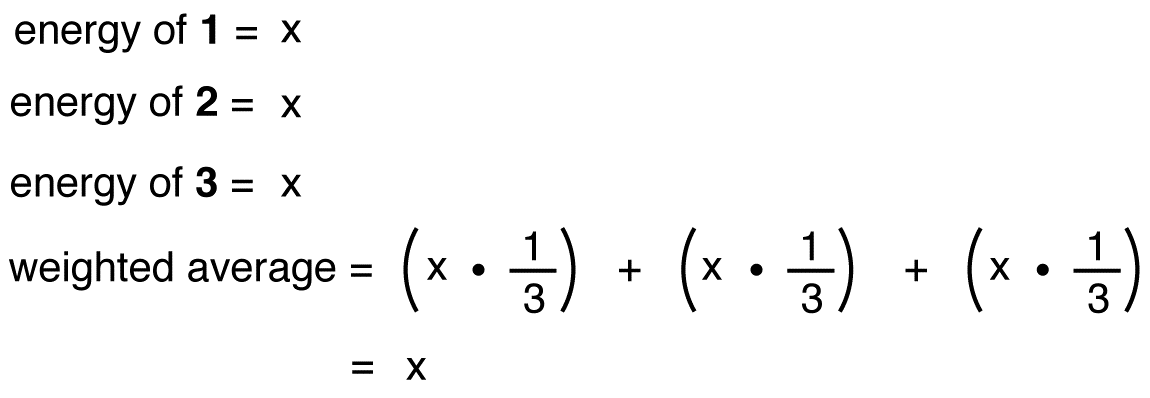
Si l’énergie de l’hybride était égale à celle d’une forme de résonance, étant donné que toutes les entités chimiques (particules élémentaires, atomes, molécules, etc.) ont naturellement tendance à être dans l’état d’énergie le plus bas possible, il n’y aurait aucun avantage pour l’ion nitrate d’exister en tant qu’hybride; il pourrait simplement exister en tant que forme de résonance. Puisque l’ion nitrate existe en tant qu’hybride et non en tant que forme de résonance, on peut en déduire que l’énergie de l’hybride est inférieure à celle de l’une des formes de résonance.
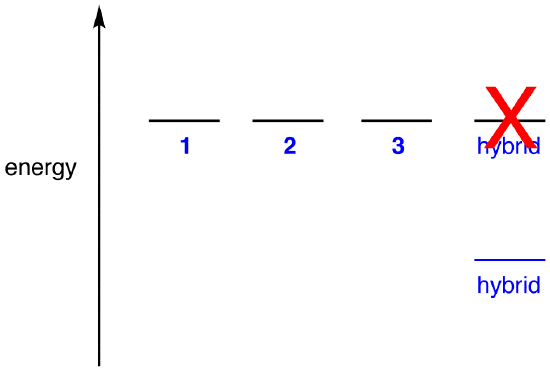
Selon la théorie de la résonance alors, l’énergie d’une molécule est inférieure à celle de la forme de résonance de plus basse énergie. Puisque l’ion nitrate a une énergie plus faible et, par conséquent, est plus stable que n’importe laquelle de ses formes de résonance, l’ion nitrate est dit stabilisé par résonance.
Il existe deux idées fausses sur la théorie de la résonance chez les étudiants débutants, probablement en raison de l’interprétation littérale du mot résonance. Ils sont décrits ci-après en prenant comme exemple l’ion nitrate.
Idée fausse 1: L’ion nitrate existe sous forme de résonance 1 pendant un moment, puis passe soit à la forme de résonance 2, soit à la forme de résonance 3, qui s’interconverse, ou revient à 1.
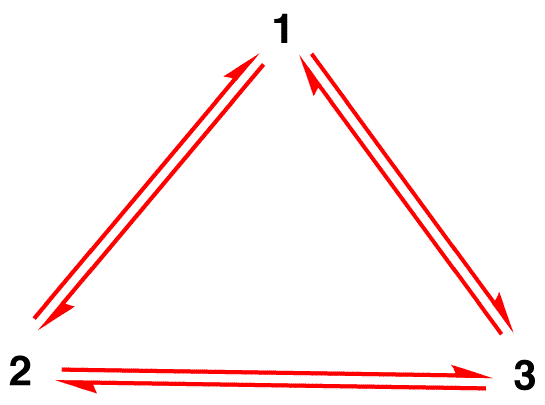
La structure de l’ion nitrate n’est pas 1, ni 2, ni 3 mais l’hybride et ne change pas avec le temps à moins de subir une réaction.
Idée fausse 2: Dans un échantillon d’ions nitrate, à un moment donné, un tiers des ions existe sous forme de résonance 1, un autre tiers sous forme de résonance 2 et le tiers restant sous forme de résonance 3.
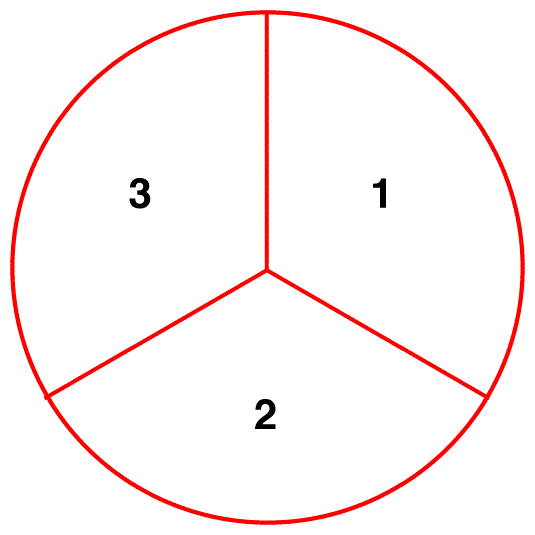
Dans un échantillon d’ions nitrate, à un moment donné, tous les ions ont la même structure, qui est l’hybride.
L’analogie classique utilisée pour clarifier ces deux idées fausses est la mule (Morrison, R. T.; Boyd, R. N. Organic Chemistry, cinquième édition; Allyn et Bacon: Boston, 1987, p. 373). Biologiquement, une mule est un hybride d’un cheval et d’un âne. Cela ne signifie pas qu’une mule ressemble un instant à un cheval puis change pour ressembler à un âne. L’apparence d’une mule est une combinaison de celle d’un cheval et de celle d’un âne et ne change pas avec le temps. Cela ne signifie pas non plus que, dans un troupeau, certaines mules ressemblent à un cheval et les autres à un âne. Dans un troupeau, toutes les mules ont la même apparence, qui est une combinaison d’un cheval et d’un âne. La faiblesse de cette analogie est que les chevaux et les ânes existent, alors que les formes de résonance sont strictement hypothétiques. Une meilleure analogie, citée dans Morrison et Boyd, est le rhinocéros. En voyant un rhinocéros, on pourrait le décrire comme l’hybride d’un dragon et d’une licorne, deux créatures qui n’existent pas.
Règles pour Dessiner des Formes de résonance
1. Les formes de résonance sont des diagrammes de Lewis, qui sont basés sur la théorie des liaisons de valence.Ils doivent donc obéir aux règles de base de la théorie des liaisons de valence. Ainsi, l’hydrogène ne peut pas avoir plus de deux électrons de valence; Période – deux éléments ne peuvent pas avoir plus de huit électrons de valence; les éléments de la période trois et inférieure peuvent avoir plus de huit électrons de valence. par exemple: Dans chaque forme de résonance de l’ion nitrate, il y a deux éléments, l’azote et l’oxygène, qui sont deux éléments de période. Dans aucune des formes de résonance de l’ion nitrate, il n’y a plus de huit électrons de valence sur l’un des atomes.
2. Toutes les formes de résonance doivent avoir le même cadre de liaison sigma, ne différant que par les emplacements des électrons pi et des électrons de valence non liés. par exemple: Les trois formes de résonance de l’ion nitrate ont le même cadre de liaison sigma:
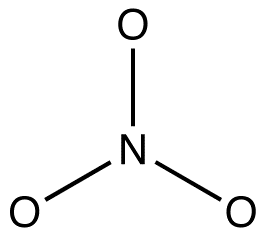
Elles ne diffèrent les unes des autres que par l’emplacement des électrons pi et des paires solitaires.
Les chimistes organiques violent de plus en plus cette règle afin d’expliquer les structures des intermédiaires réactifs en tant qu’espèces stabilisées par résonance. eg : oxymercuration
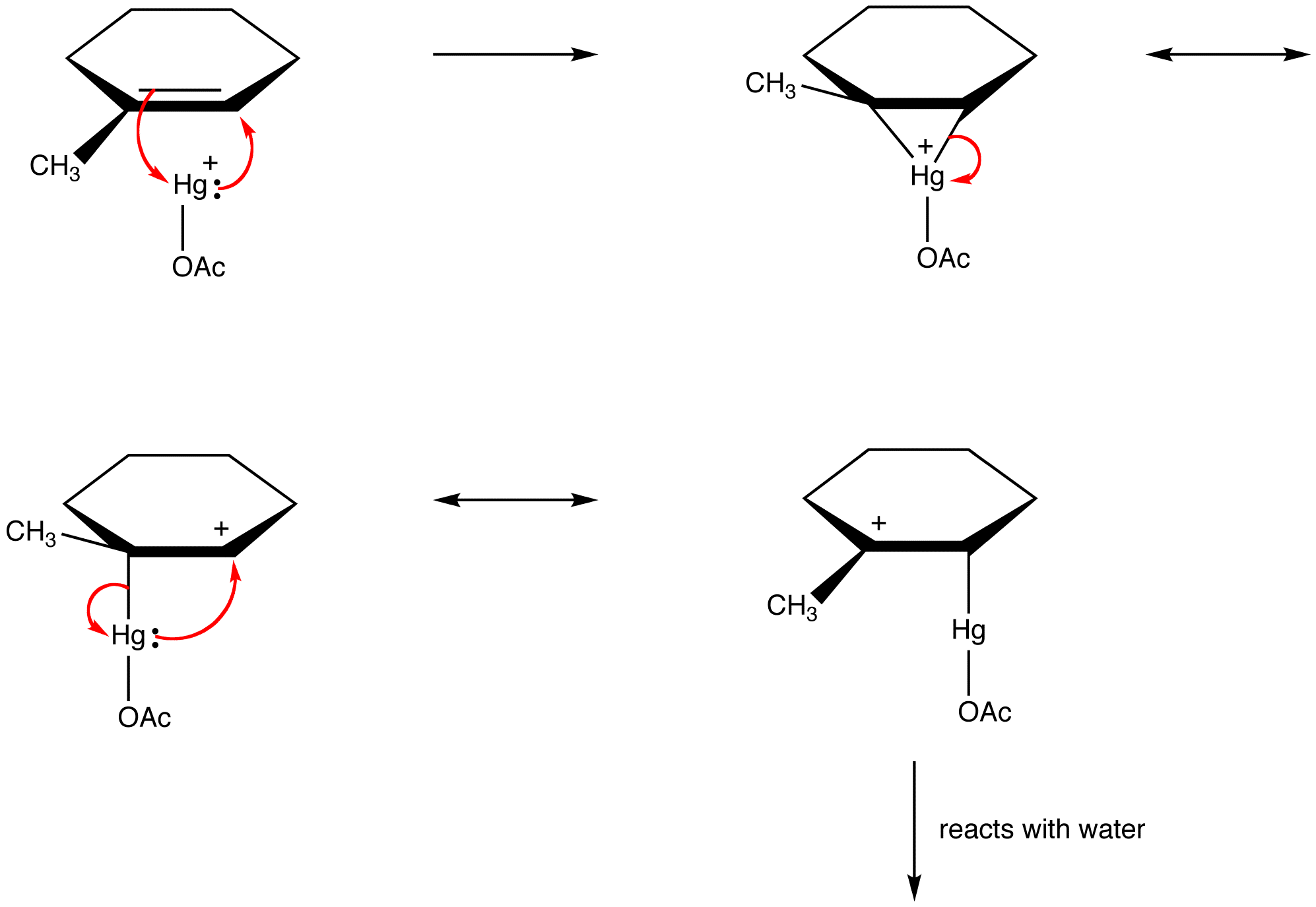
Détermination de la Contribution Relative des Formes de Résonance à l’Hybride
Les trois formes de l’ion nitrate sont identiques et ont donc la même stabilité. Par conséquent, ils contribuent également à l’hybride. Les formes de résonance de la plupart des molécules stabilisées par résonance sont différentes les unes des autres, elles ne contribuent donc pas également à l’hybride. Plus la forme de résonance est stable, plus elle contribue à l’hybride. Ainsi, la détermination des formes de contribution relative ou de résonance à l’hybride nécessite la détermination de leur stabilité relative. Utilisez les règles suivantes pour déterminer la stabilité relative des formes de résonance.
Règle 1 :
Une forme de résonance dans laquelle tous les atomes ont un octet d’électrons de valence est plus stable qu’une forme dans laquelle au moins un atome n’en a pas. par exemple:
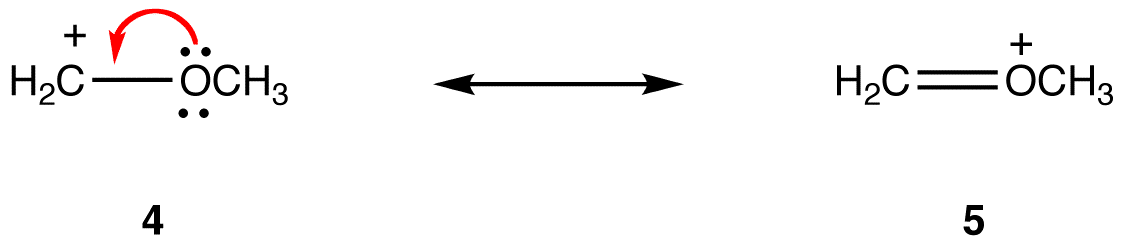
Sous la forme de résonance 5, tous les atomes ont un octet d’électrons de valence; en 4, un atome, l’atome de carbone portant la charge formelle de +1, ne le fait pas. Ainsi, la forme de résonance 5 est plus stable que la forme de résonance 4.
Règle 2:
Toutes choses étant égales par ailleurs, une forme de résonance qui a une charge négative formelle sur un atome plus électronégatif est plus stable qu’une forme qui a une charge négative formelle sur un atome moins électronégatif. par exemple:
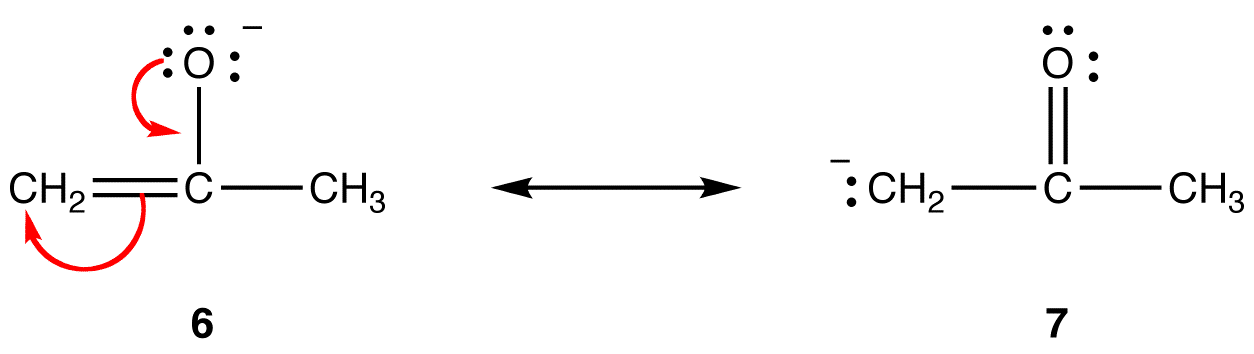
Sous la forme de résonance 6, la charge négative formelle est sur un atome d’oxygène; en 7, elle est sur un atome de carbone. L’oxygène est plus électronégatif que le carbone. Ainsi, la forme de résonance 6 est plus stable que la forme de résonance 7.
La tendance est inverse en ce qui concerne les charges positives formelles. Toutes choses étant égales par ailleurs, une forme de résonance qui a une charge positive formelle sur un atome moins électronégatif est plus stable qu’une forme qui a une charge positive formelle sur un atome plus électronégatif. par exemple:
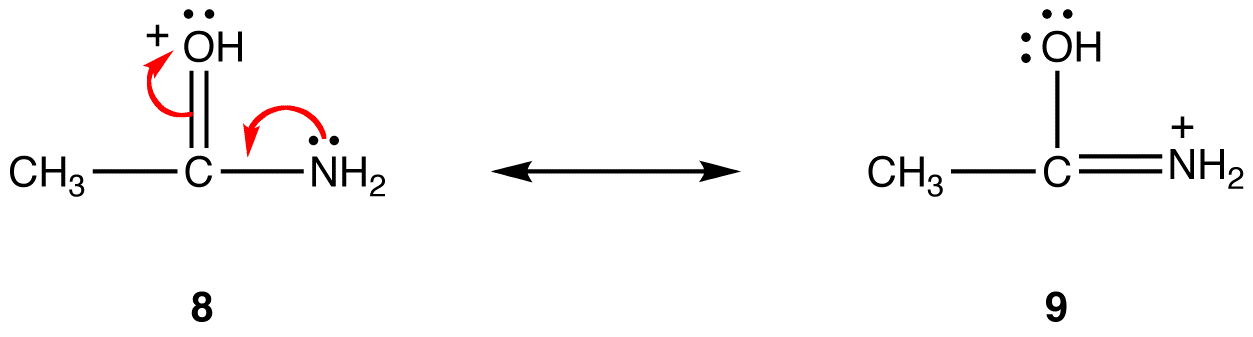
Sous la forme de résonance 8, la charge positive formelle est sur un atome d’oxygène ; en 9, elle est sur un atome d’azote. L’azote est moins électronégatif que l’oxygène, Ainsi, la forme de résonance 9 est plus stable que la forme de résonance 8.
Règle 3 :
Toutes choses étant égales par ailleurs, une forme de résonance qui n’a pas de séparation de charge, appelée forme de résonance dipolaire, est plus stable que celle qui le fait. par exemple:
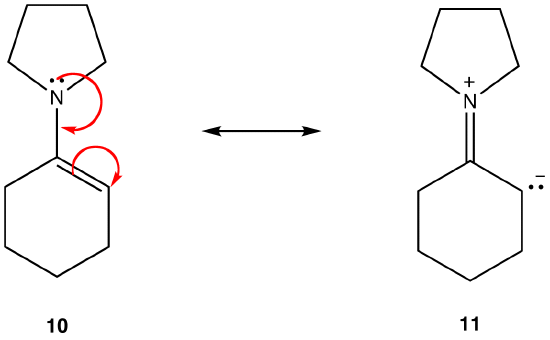
La forme de résonance 11 est une forme de résonance dipolaire; 10 ne l’est pas. Ainsi, 10 est plus stable que 11. Cette règle est une conséquence de la forme vectorielle de la loi de Coloumb, selon laquelle les charges opposées s’attirent. Le corollaire est que, pour séparer les charges opposées, de l’énergie est nécessaire, ce qui signifie que 11 a une énergie supérieure à 10, donc 10 est plus stable que 11.
Règle 4 :
Dans les formes de résonance dipolaire, toutes choses étant égales par ailleurs, plus la distance entre les charges séparées est grande, plus la forme de résonance est stable. par exemple:
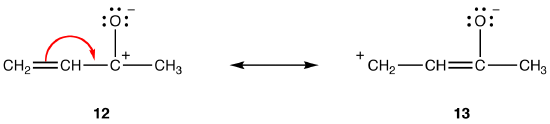
Les deux formes de résonance 12 et 13 sont des formes de résonance dipolaire. La distance entre les charges séparées est plus grande dans 13 (trois liaisons) que dans 12 (une liaison), donc 13 est plus stable que 12. Cette règle est une conséquence de la forme scalaire de la loi de Coloumb, qui stipule que la force d’attraction entre les charges opposées est inversement proportionnelle au carré de la distance qui les sépare. Ainsi, l’énergie nécessaire pour maintenir les charges opposées séparées en 12 est supérieure à celle en 13, ce qui signifie que 12 a une énergie supérieure à 13, donc 13 est plus stable que 12.
Les règles ci-dessus peuvent ne pas s’appliquer à la résonance impliquant des éléments de période trois et inférieure, en raison de leur capacité à accueillir plus de huit électrons dans la coque de valence. par exemple :
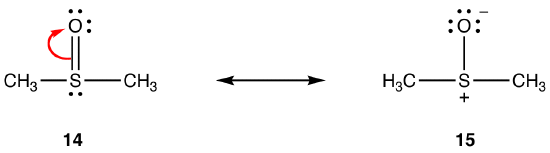
La double liaison en 14 est constituée d’une liaison sigma et d’une liaison formée par le chevauchement d’une orbitale 2p, portant deux électrons, dans l’atome d’oxygène et d’une orbitale 3d vide dans l’atome de soufre. Ces deux orbitales ont des énergies, des tailles et des formes très différentes, de sorte que le chevauchement entre elles, connu sous le nom d’interaction pn–dn, est faible. Par conséquent, il y a peu de caractère de double liaison dans la liaison soufre-oxygène dans l’hybride, c’est-à-dire que 15 est la forme de résonance principale.
Contributeurs et attributions
- Gamini Gunawardena du site OChemPal (Université de la vallée de l’Utah)