Un varón de 49 años con antecedentes de abuso de alcohol presenta al Departamento de Emergencias quejas de dolor abdominal generalizado y vómitos durante las últimas 36 horas. El paciente es bien conocido por el departamento de visitas relacionadas con el alcohol y continúa bebiendo a diario. A su llegada, tiene taquicardia y taquipnea, y los hallazgos del examen físico incluyen membranas mucosas secas, disminución de la turgencia sakin, sensibilidad epigástrica y temblor en ambas manos. Los estudios de laboratorio muestran un bicarbonato sérico de 10 mEq/L, una brecha aniónica de 30, una glucosa sérica de 95 mg / dL, una acidosis láctica con pH 7,2, hipofosfatemia y cetonuria traza. La tomografía computarizada abdominal es normal. Niega tener antecedentes de diabetes mellitus, ingestión de alcoholes tóxicos o enfermedad reciente.
Este paciente podría tener cualquiera de los muchos diagnósticos, pero su presentación y hallazgos de laboratorio son más consistentes con cetoacidosis alcohólica (AKA). AKA puede ser un diagnóstico común de disfunción eréctil y típicamente ocurre en bebedores crónicos de alcohol que tienen un cese abrupto en su consumo de alcohol junto con una disminución de la ingesta glucémica y una depleción del volumen intravascular.1
En la mayoría de los casos, un evento precipitante como pancreatitis, gastritis o neumonía por aspiración conduce a una disminución abrupta de la ingesta oral. Alrededor de 24 a 72 horas después del cese de la ingesta de PO, AKA, puede desarrollarse.2 Estos pacientes suelen tener una concentración de alcohol sérico baja o ausente y pueden presentar diversos grados de abstinencia alcohólica. Sin embargo, un sensorio claro es un sello distintivo de esta condición. La presencia de una alteración en la conciencia sugiere fuertemente que otro proceso está presente.3
Aunque la fisiopatología subyacente es compleja, una comprensión adecuada ayuda en gran medida en el diagnóstico y manejo de esta afección.
Hay tres conceptos generales que impulsan AKA:
- La ingestión de alcohol, combinada con una disminución de la ingesta calórica y la deshidratación, favorece un estado cetótico.La cetoacidosis es causada por una combinación de factores, que incluyen hipoinsulinemia inducida por inanición, oxidación del alcohol a sus diversos metabolitos cetónicos, lipólisis con liberación de ácidos grasos libres (AFF) y contracción del volumen intravascular. El estado de inanición relativo en AKA conduce a una secreción excesiva de glucagón y concentraciones reducidas de insulina periférica, lo que juega un papel clave en el desarrollo de cetoacidosis. El metabolismo de las grasas a través de la lipólisis produce beta-hidroxibutirato (BHB) y actilo-acetato (ACA). Estas cetonas se utilizan para la respiración celular para proporcionar energía a través de la producción de trifosfato de adenosina (ATP), pero se suman a la acidosis de la brecha aniónica observada en AKA.
- Durante el metabolismo del etanol, se generan altas cantidades de NADH (la forma reducida de dinucleótido de nicotinamida-adenina).4
NAD + es una coenzima utilizada para transportar electrones en reacciones redox intracelulares. La reducción de NAD+ y la consiguiente acumulación y desequilibrio de NADH en el metabolismo del etanol tiene varias consecuencias importantes. La generación de BHB predomina sobre la producción de ACA en esta alta relación NADH / NAD+. Esta proporción anormal conduce a una inhibición del ciclo del ácido cítrico y la gluconeogénesis hepática, lo que explica en parte por qué la hiperglucemia es rara en estos pacientes.Casi contraintuitivamente, hay un fallo en la regeneración de los niveles normales de NAD+ y ACA en AKA. La reoxidación de NADH a NAD+ parece estar limitada por una combinación de factores, incluyendo hipofosfatemia y un bloqueo funcional dentro de las mitocondrias.2La acidosis láctica observada en AKA se debe a un estado redox anormal. El piruvato es un sustrato utilizado en numerosas vías productoras de energía, pero en la cetoacidosis alcohólica, se desplaza de sus vías metabólicas normales a otras que aumentan la producción de lactato. Además, la regeneración del piruvato a partir del ácido láctico se ve afectada.
- Un estado adrenérgico elevado y el agotamiento del volumen empeoran la cetosis e inhiben la gluconeogénesis, creando un estado que favorece la creación y el mantenimiento de un entorno cetótico.El cuerpo responde al hambre, la deshidratación y la hipoglucemia con la liberación de hormonas contrarreguladoras. Estas hormonas aumentan el tono simpático, disminuyen la liberación de insulina y aumentan la concentración de cetonas a través de la liberación de AGF y la disminución del metabolismo de cetonas periféricas. Todos estos cambios perpetúan el estado cetótico hasta que la glucosa se reintroduce en el sistema. La deshidratación significativa debida a los vómitos y la disminución de la ingesta oral provocan un deterioro del aclaramiento de cetonas renales, lo que agrava aún más la situación.2El diagnóstico diferencial para AKA debe incluir cetosis por inanición y cetoacidosis diabética (CAD). Aunque una historia clínica completa puede ayudar a reducir el diferencial, un panel metabólico es esencial para confirmar el diagnóstico. Se pueden ver huecos de aniones de 30 mEq/L o más en AKA, aunque el hueco puede estar oscurecido por una alcalosis metabólica primaria concomitante debido a vómitos. De hecho, hay informes de casos de pacientes con AKA que tienen un pH sérico alcalémico debido a vómitos excesivos.La brecha aniónica en la cetosis por inanición es típicamente mucho menor, con niveles de bicarbonato raramente por debajo de 18 mEq/L, y pH sérico típicamente por encima de 7,30.2 En CAD, por el contrario, la brecha aniónica puede ser bastante alta, con niveles de bicarbonato que frecuentemente alcanzan los dígitos individuales. La hiperglucemia con glucosuria, típicamente observada en cetoacidosis diabética (CAD), es rara con AKA.4 La desnutrición crónica conduce a bajas reservas de glucógeno, y el tono adrenérgico elevado conduce a la inhibición de la gluconeogénesis hepática. La cetonuria, presente en estas tres condiciones, puede confundir la gravedad de AKA.La cetonuria se mide mediante la prueba de nitroprusiato, en la que un cambio de color indica la concentración relativa de acetona y ACA en la orina. La presencia de BHB, la cetona más prominente presente en AKA, no se refleja en la prueba de nitroprusiato. Esto explica por qué los pacientes con AKA pueden mostrar ninguna o solo una ligera cetonuria en la presentación inicial, con un aumento paradójico a medida que la condición se invierte. A medida que la relación ACA:BHB se normaliza, tanto el ACA detectable como el BHB se eliminan en la orina.
Diagnóstico diferencial
En el diagnóstico diferencial también se deben considerar otras afecciones potencialmente mortales que pueden causar una acidosis con brecha aniónica significativa. Los alcoholes tóxicos, específicamente metanol y etilenglicol, pueden ser ingeridos intencional o accidentalmente en esta población de pacientes. Estas ingestiones pueden causar morbilidad y mortalidad significativas si no se manejan adecuadamente.5 El estado mental alterado es una característica común de la ingestión de alcohol tóxico, pero generalmente no se ve en AKA.5
Los pacientes típicamente tendrán un espacio osmolar inicial que transita a un aumento del espacio aniónico a medida que se metaboliza el alcohol tóxico. La concentración sérica elevada de BHB puede ser bastante elevada en AKA, pero esto no excluye necesariamente la posibilidad de ingestión de alcohol tóxico; ni la ausencia de un espacio osmolar o aniónico descarta el diagnóstico. Mientras que los pacientes en AKA tienen una ligera acidosis láctica, la presencia de un nivel de lactato significativamente elevado debería impulsar la búsqueda de una enfermedad subyacente. En raras ocasiones, una combinación de AKA y uno de estos otros eventos puede ocurrir y presentar un enigma diagnóstico. Se debe considerar cuidadosamente el momento, el tipo y la cantidad de ingestión, y los síntomas asociados, en combinación con la observación y los estudios de laboratorio, para hacer esta diferenciación si se carece de una historia clínica clara y precisa.
Tratamiento
La reversión de la cetosis y la rehidratación vigorosa son centrales en el manejo de AKA. Además de la sustitución de líquidos isotónicos, se necesitan líquidos intravenosos que contengan dextrosa. Por lo general, la dextrosa al 5% con solución salina medio normal a una velocidad de 150 ml por hora proporciona suficiente glucosa para estimular al páncreas a secretar insulina, lo que permite que los tejidos periféricos metabolicen las cetonas e inhiban la liberación de AGF.2 También permite al cuerpo regenerar el NAD+, que es inhibido por las alteraciones metabólicas causadas por AKA. Las infusiones intravenosas de líquidos que contienen dextrosa deben interrumpirse una vez que los niveles de bicarbonato hayan alcanzado los 18-20 mEq/L y el paciente esté tolerando la ingesta oral. Esto suele ocurrir de 8 a 16 horas después del inicio del tratamiento.2 La abstinencia de alcohol en estos pacientes debe tratarse de forma agresiva con benzodiazepinas intravenosas. Es posible que en estos pacientes sea necesario repetir la administración de tiamina, ácido fólico y otros electrolitos, en particular fosfato y potasio.6 Curiosamente, la mayoría de la morbilidad observada en AKA se debe al proceso subyacente que causó el cese del alcohol.
Conclusión del caso
El paciente recibió 4 litros de solución salina normal y se inició en D5-1/2 NS antes del ingreso. Se le administró valium por vía intravenosa para la abstinencia de alcohol, y tiamina, folato y fosfato se volvieron a inyectar. Fue hospitalizado durante tres días por manejo de AKA y abstinencia de alcohol, luego fue dado de alta una vez tolerando la ingesta oral y en buenas condiciones. Fue visto tres semanas después en el departamento de emergencias para una presentación similar.
Cuadro 1. Characteristics of Common Ketoacidoses
| Diabetic Ketoacidosis | Alcoholic Ketoacidosis | Starvation Ketoacidosis | |
| Bicarbonate | Can reach single digits | Can reach single digits | > 18 |
| Glucose | Elevated | Low to mildly elevated | Low to normal |
| Measurable ketonuria | Present | Absent or present | Present |
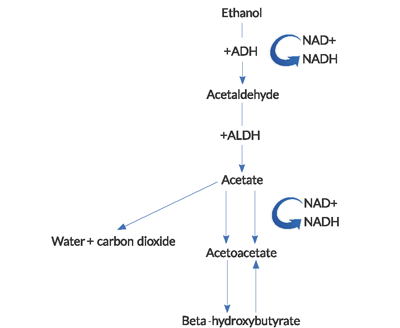
Figure 1. Vía del metabolismo del alcohol
(ADH = alcohol deshidrogenasa, ALDH = acetaldehído deshidrogenasa).
- Palmer, Jerry P. Cetoacidosis alcohólica: Presentación clínica y de laboratorio, fisiopatología y tratamiento. Clinics in endocrinology and metabolism 12.2 (1983): 381-389.
- Duffens K, Marx JA. Revisión de cetoacidosis alcohólica.The Journal of emergency medicine 5.5 (1987): 399-406.
- Wrenn KD, Slovis CM, Minion GE, et al. El síndrome de cetoacidosis alcohólica. The American journal of medicine 91.2 (1991): 119-128.
- Marx JA, Hockberger RS, Walls RM, et al., eréctil. Medicina de Emergencia Rosens™: Conceptos y Práctica Clínica. Philadelphia, PA: Mosby/Elsevier; 2013. Capítulo 185 Enfermedad Relacionada con el Alcohol por John T. Finnell.
- Kraut JA, Kurtz I. ‌toxic alcohol ingestions: clinical features, diagnosis, and management (en inglés). Clinical Journal of the American Society of Nephrology 3.1 (2008): 208-225.
- Miller PD, Heinig R, Waterhouse C. Tratamiento de la acidosis alcohólica: el papel de la dextrosa y el fósforo. Archives of internal medicine 138.1 (1978): 67-72.