Ziprasidon versus Olanzapin bei der Gewichtszunahme im Zusammenhang mit der Behandlung von Schizophrenie: Eine sechsmonatige doppelblinde randomisierte Parallelgruppenstudie
Enric Álvarez*; Miguel Bernardo**; José Ramón Gutiérrez Casares***; Ángel L. Montejo****
* Abteilung für Psychiatrie. Krankenhaus de la Santa Creu i Sant Pau. CIBERSAM, Universitat Autónoma de Barcelona, IBSantpau Barcelona. Spanien
** Abteilung für Psychiatrie, Hospital Clinic de Barcelona, CIBERSAM, Universität Barcelona, IDIBAPS, Barcelona. Spanien
* * * Universitätsklinik-Komplex von Badajoz. Gesundheitsdienst Extremadura, Badajoz. Spanien
**** Universitätskrankenhaus von Salamanca. Medizinische Fakultät, Universität von Salamanca, Salamanca. Spanien
Diese Studie wurde von Pfizer finanziert.
Korrespondenz
ZUSAMMENFASSUNG
Hintergrund und Ziele: Frühere Daten aus Sicherheitsanalysen deuten darauf hin, dass Olanzapin zu einer erheblichen Gewichtszunahme führen kann, während bei Ziprasidon keine Veränderung beobachtet wurde. Fettleibigkeit kann eine Gefahr für die Gesundheit darstellen und dazu führen, dass die Probanden ihre antipsychotischen Medikamente absetzen. Um die unterschiedlichen Auswirkungen von Ziprasidon und Olanzapin auf die Gewichtszunahme weiter zu bewerten, wurde eine Studie mit dem Körpergewicht als primärem Wirksamkeitsendpunkt durchgeführt.
Methoden: Eine sechsmonatige randomisierte, doppelblinde Parallelstudie wurde an männlichen und weiblichen Probanden im Alter von 18 bis 70 Jahren mit einer Primärdiagnose von Schizophrenie (DSM-IV-TR) und einem klinischen Zustand durchgeführt, der einen Behandlungsbeginn mit einem neuen Antipsychotikum, Ziprasidon oder Olanzapin 1:1, zur Beurteilung der behandlungsbedingten Gewichtsveränderungen erforderte. Fünfzig Patienten wurden eingeschlossen. Die Wirksamkeitsergebnisse wurden zu Studienbeginn und in den Wochen 1, 4, 12, 18 und 24 bewertet. Der primäre Wirksamkeitsendpunkt war die prozentuale Veränderung des Körpergewichts gegenüber dem Ausgangswert in Woche 24. Die Sicherheit wurde ebenfalls bewertet.
Ergebnisse: In Woche 24 gab es eine signifikant stärkere Zunahme des Körpergewichts (7, 5%, p <0, 0001) bei Patienten, die mit Olanzapin behandelt wurden, als bei Patienten, die mit Ziprasidon behandelt wurden, und die Anzahl der Probanden mit einer Gewichtszunahme > 7% war in der Olanzapin-Gruppe signifikant höher als in der Ziprasidon-Gruppe (n = 11 ) vs. n = 3 ; ODER = 6,246, p-Wert = 0,0150). PANNS-N nahm in beiden Gruppen signifikant ab. Die meisten Nebenwirkungen waren in beiden Gruppen moderat oder mild.
Schlussfolgerungen: Olanzapin erhöht das Körpergewicht signifikant gegenüber Ziprasidon in Woche 24. Die Behandlung mit Ziprasidon oder Olanzapin verbesserte jedoch die positiven, negativen und allgemeinen psychopathologischen Werte von PANSS und wurde gut vertragen.Schlüsselwörter: Antipsychotika; Gewichtszunahme; Ziprasidon; Olanzapin; Fettleibigkeit.
Einleitung
Schizophrene Patienten zeigen eine höhere Prävalenz von Fettleibigkeit, Glukoseintoleranz und Typ-2-Diabetes mellitus mit einer genetischen Verbindung zu Enzymen, die an der Glykolyse beteiligt sind1,2 und eine höhere Rate kardiovaskulärer Ereignisse3. Darüber hinaus sind viele Antipsychotika der zweiten Generation mit einem höheren Risiko für Gewichtszunahme2,4, Insulinresistenz, Hyperglykämie und Dyslipidämie5 verbunden. Die Kombination dieser verschiedenen Faktoren, die genetische Anfälligkeit, eine sitzende Lebensweise und eine schlechte Ernährung sowie die nachteiligen Nebenwirkungen der antipsychotischen Behandlung, stellen einen wichtigen Risikofaktor für Herz-Kreislauf-Erkrankungen bei Patienten dar, die mit atypischen Antipsychotika behandelt werden6. Fettleibigkeit ist nicht nur eine Bedrohung für Gesundheit und Langlebigkeit, sondern kann auch dazu führen, dass die Probanden ihre antipsychotischen Medikamente absetzen7.
Sowohl Ziprasidon als auch Olanzapin sind wirksame atypische Antipsychotika, die häufig zur Behandlung von Schizophrenie und schizoiden Störungen eingesetzt werden. Atypische Antipsychotika zeigen eine bessere Wirksamkeit und weniger Nebenwirkungen als typische Antipsychotika8,9. Sie sind jedoch immer noch anfällig für unerwünschte Wirkungen, einschließlich hypostatischer Hypotension10, Somnolenz11, Gewichtszunahme1,2, Dyslipidämie12, Hyperglykämie und Diabetes mellitus5 und Hyperprolaktinämie, die Fruchtbarkeitsprobleme, sexuelle Dysfunktion und verminderte Knochenmineraldichte verursachen können13,14.
Frühere Studien haben keine Veränderungen des Gewichts oder des Stoffwechsels bei mit Ziprasidon behandelten Probanden1,2,15 gezeigt, Ziprasidon zeigt eine geringe Neigung, extrapyramidale Nebenwirkungen (EPS) oder Laboranomalien zu verursachen8,16,17 und beeinträchtigt die sexuelle Funktion schizophrener Patienten nicht18. Es wurde berichtet, dass Ziprasidon einen Gewichtsverlust und eine Verringerung der Serumlipidspiegel verursacht19,20.
Olanzapin ist eines der am häufigsten verschriebenen Antipsychotika mit nachgewiesener Wirksamkeit bei Schizophrenie-Symptomen21-23. Olanzapin gehört jedoch zu den atypischen Antipsychotika, die eine Gewichtszunahme induzieren24,25 und ist auch mit einem erheblichen Anstieg des Gesamtcholesterins, der Triglyceride, des LDL und des Nüchterninsulins verbunden20,26,27. In früheren Studien, in denen Ziprasidon mit Olanzapin ausschließlich oder in Kombination mit anderen Behandlungen verglichen wurde, zeigte Olanzapin einen signifikant stärkeren Gewichts- und BMI-Anstieg und eine höhere Wahrscheinlichkeit einer schnellen Gewichtszunahme als jede andere Behandlung7,20,26,27. Alle diese Studien hatten jedoch eine Wirksamkeitsvariable als primäre Variable, da die Gewichtsbewertung nur ein Teil der Sicherheitsstudie war.Antipsychotische Behandlungen sind oft langfristig und es ist notwendig, das erhöhte Risiko für metabolische Veränderungen in der Patientenversorgung zu berücksichtigen. Daher wurde diese randomisierte, doppelblinde Studie entwickelt, um speziell das Problem der Gewichtszunahme langfristig (6 Monate) anzugehen, wobei dies die primäre Variable ist. In Anbetracht der Tatsache, dass andere Faktoren mit der Disposition und Einhaltung der Behandlung des Patienten zusammenhängen, wurden in dieser Studie die Lebensqualität, die allgemeine Funktionsweise, die Präferenzen und die Einstellung zur Behandlung bewertet, um weitere Informationen zu den in diesen Langzeitbehandlungen zu behandelnden Themen bereitzustellen und ihre Beziehung zum Hauptzweck zu diskutieren.
Methoden
Von April 2003 bis Februar 2007 wurde eine sechsmonatige randomisierte, multizentrische, parallele Doppelblindstudie durchgeführt, um die Auswirkungen von Ziprasidon gegenüber Olanzapin auf das Körpergewicht bei der Behandlung von Patienten mit Schizophrenie abzuschätzen und zu vergleichen.
Die Studie wurde in 11 Zentren in ganz Spanien durchgeführt. Männliche oder weibliche Probanden im Alter von 18 bis 70 Jahren mit einer Primärdiagnose von Schizophrenie gemäß DSM-IV-TR28 und einem klinischen Zustand, der einen Behandlungsbeginn mit einem neuen Antipsychotikum erforderte, wurden aufgenommen. Die Patienten oder ihr gesetzlicher Vertreter gaben ihre Einverständniserklärung ab. QTc > 500 ms), klinisch signifikante abnormale Laborwerte, Epilepsie, Krampfanfälle, Psychochirurgie, mangelndes Ansprechen oder frühere Unverträglichkeit gegenüber Olanzapin oder Ziprasidon; Schwangerschaft oder Stillzeit; serologische Hinweise auf HIV oder Hepatitis; Behandlung mit einem der beiden Arzneimittel innerhalb der 6 Monate vor dem Screening; Patientin, die das Studienprotokoll nicht einhalten kann oder kann; unmittelbares Risiko, sich selbst oder anderen Schaden zuzufügen; gleichzeitige Behandlung mit Antipsychotika nach Randomisierung; Depot-Antipsychotika innerhalb eines Monats nach Eintritt; Behandlung mit Antidepressiva oder Stimmungsstabilisatoren innerhalb von zwei Wochen nach Randomisierung; Drogenmissbrauch innerhalb der letzten 3 Monate; organische Geisteskrankheit; Behandlung mit einem klinischen Forschungsmedikament innerhalb von 30 Tagen vor der Randomisierung.
Die Studie wurde in Übereinstimmung mit der Erklärung von Helsinki29 entwickelt und das Studienprotokoll wurde von den Ethikkommissionen der beteiligten Zentren und von der Abteilung für Humanarzneimittel der spanischen Agentur für Medizin und Gesundheitsprodukte (AEMPS) genehmigt.
Die Probanden wurden 12 Stunden nach der vorherigen antipsychotischen Dosis in die Studie aufgenommen, mit Ausnahme von Probanden, die mit einem Depot-Antipsychotikum behandelt wurden (siehe oben), und wurden randomisiert im Verhältnis 1:1 zugeteilt.
Behandlungsdosis und Besuchsplan
Die Dosierung war innerhalb von 3 Stufen flexibel: Niedrig (Ziprasidon 40 mg oder Olanzapin 5 mg), Mittel (Ziprasidon 60 mg oder Olanzapin 15 mg QD) und hoch (Ziprasidon 80 mg oder Olanzapin 10 mg). Die Behandlung wurde an den Tagen 1-7 mit niedriger Dosis begonnen und ab Tag 3 konnte die Dosis angepasst werden.
Die Behandlungsphase (6 Monate) umfasste 6 Besuche: Tag 1 (Woche 0), Woche 1, Woche 4, Woche 12, Woche 18 und Woche 24. Follow-up-Besuch (Woche 48) durchgeführt sechs Monate nach Abschluss der Behandlung. Studienmedikation wurde von Besuch 1 bis 6 berichtet. Probanden, die zu irgendeinem Zeitpunkt während der Studie ein unzureichendes Ansprechen zeigten, wie durch einen Clinical Global Impression of Improvement (CGI-I) -Score von ≥ 6 angezeigt, wurden zurückgezogen.
Wirksamkeits- und Sicherheitsbewertungen
Die gemessenen Wirksamkeitsergebnisse waren Gewicht, BMI und Taillenumfang (WC); Blutdruck und Puls; die positive und negative Syndromskala (PANSS)30; die Clinical Global Impression (CGI) Scale31 und eine andere zur Verbesserung (CGI-I); körperliche Aktivität des Patienten; die Patientenpräferenzskala (PPS), um die Zufriedenheit des Patienten mit Medikamenten zu messen; die spanische Version des Health Utilities Index-Mark 3 (HUI-3)32,22. Der Appetit wurde mit einer visuellen Analogskala (VAS) gemessen, einer subjektiven Quantifizierungsmethode. Der Patient markiert seinen Appetit seit dem letzten Besuch auf einer horizontalen Linie mit 0 (kein Appetit) links und 10 (extrem hungrig) rechts. Der Abstand von 0 wird dann in cm gemessen und der Pegel quantifiziert.
Alle Wirksamkeitsergebnisse wurden bei Visite 1 (Baseline-Werte): CGI-S, CGI-I und PANSS von Besuch 2 bis 7, Appetit und körperliche Aktivität des Patienten von Besuch 3 bis 6, PPS und HUI-3 bei Besuchen 4 und 6
Die Sicherheitsbewertungen umfassten klinisches Monitoring, Elektrokardiogramme, Vitalfunktionen, unerwünschte Ereignisse (UE) und Sicherheitslabortests. Sicherheitsbewertungen wurden gemäß den Anforderungen der Worldwide Safety Standards (WSS) Version 3 gemeldet.
Statistische Analyse
Alle Analysen wurden mit der Intent-to-Treat (ITT) -Population unter Verwendung der SAS®-Version 8.2 oder höher durchgeführt. Statistische Tests waren 2 tailed und p-Werte von 0.05 oder kleiner wurden als statistisch signifikant angesehen. Die Behandlung wurde als kategorisch eingestuft. 95% Konfidenzintervalle (KI) wurden um alle geschätzten Behandlungsunterschiede herum konstruiert. Alle Änderungen wurden durch Kovarianzanalyse (ANCOVA) einschließlich der Auswirkungen auf die Behandlungsgruppe und den Ausgangswert (falls zutreffend) analysiert. Deskriptive Statistiken wurden verwendet, um alle Sicherheitsbewertungen zusammenzufassen. Unerwünschte Ereignisse wurden gemäß dem Medical Dictionary for Regulatory Activities (MedDRA) kodiert. Es wurden keine formalen statistischen Tests zu Sicherheitsparametern durchgeführt.
Ergebnisse
Disposition des Probanden und Medikamentendosis
Obwohl die Studie ursprünglich für 112 Patienten gedacht war, wurden im Studienzeitraum nur 58 Probanden untersucht. Schließlich wurden 50 ITT-Patienten eingeschlossen: 27 gegen Ziprasidon und 23 gegen Olanzapin. Während des Studienzeitraums brachen insgesamt 29 Probanden ihre Behandlung ab (19 in der Ziprasidon-Gruppe und 10 in der Olanzapin-Gruppe). Obwohl die meisten Abbrüche nicht mit dem Studienmedikament zusammenhingen, waren 2 (einer in jeder Gruppe) auf mangelnde Wirksamkeit und 7 (5 bei Ziprasidon und 2 bei Olanzapin) auf arzneimittelbedingte Nebenwirkungen zurückzuführen. Die mediane Behandlungsdauer war für die Ziprasidon-Gruppe (52,5 Tage ) niedriger als für die Olanzapin-Gruppe (164 Tage ; 32% der Patienten in der Ziprasidon-Gruppe und 58% in der Olanzapin-Gruppe schlossen die Studie ab.
Während der Behandlungsphase erhielten Patienten unter Ziprasidon eine mittlere Dosis von 107,4 ± 27,3 mg/Tag und Patienten unter Olanzapin eine mittlere Dosis von 15 ± 3,3 mg/Tag.
Basismerkmale
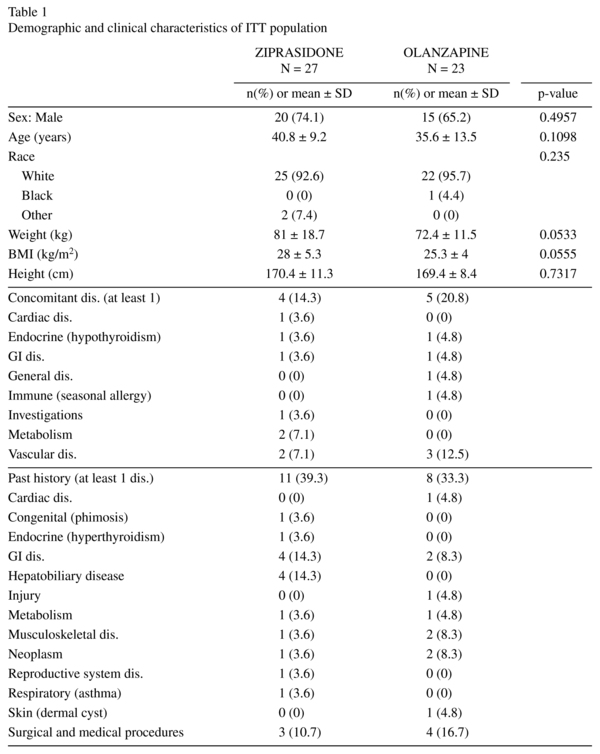
Die demografischen Merkmale waren zwischen beiden Gruppen homogen und zeigten keine signifikanten Unterschiede. ITT-Patienten waren 19-63 Jahre alt, die Mehrheit zwischen 18-44 Jahren. Detaillierte demografische Daten sind in Tabelle 1 enthalten. Eine ähnliche Anzahl von Probanden in beiden Behandlungsgruppen erhielt während der Studie eine gleichzeitige medikamentöse Behandlung (26 in der Ziprasidon- und 21 in der Olanzapin-Gruppe). Die am häufigsten eingenommenen (von ≥ 5 Probanden in beiden Behandlungsgruppen) in beiden Behandlungsgruppen waren Lorazepam, Lormeta-Zepam und Risperidon.
Auswirkungen auf die Gewichtszunahme
Das Körpergewicht war in Woche 24 in der Ziprasidon-Gruppe stabil und zeigte keinen signifikanten Unterschied zum Basalgewicht (-0,1% prozentuale Abnahme; n.s.), während in der Olanzapin-Gruppe ein statistisch signifikanter Anstieg gegenüber dem Ausgangswert auftrat (7, 4% prozentualer Anstieg des Körpergewichts gegenüber dem Ausgangswert, p < 0, 0001) (Tabelle 2). Der Unterschied zwischen den Behandlungsgruppen in Bezug auf die Veränderung des Körpergewichts gegenüber dem Ausgangswert war zu allen Zeitpunkten statistisch signifikant, und die mit Olanzapin behandelten Patienten zeigten bei allen Besuchen eine signifikante Gewichtszunahme gegenüber dem Ausgangswert (Tabelle 2). Die Anzahl der Probanden mit einer Gewichtszunahme ≥ 7% in Woche 24 war in der Ziprasidon-Gruppe (n = 3 ) signifikant niedriger als in der Olanzapin-Gruppe (n = 11 ) (OR = 6,246; p = 0.0150). Der Unterschied zwischen den Behandlungsgruppen war auch in den Wochen 12 (p = 0, 0266) und 18 (p = 0, 0261) offensichtlich (Daten nicht gezeigt).

Die sekundären Endpunkte in Woche 24 sind in Tabelle 3 zusammengefasst. Bei mit Ziprasidon behandelten Patienten kam es nach 24 Wochen zu keiner signifikanten Veränderung der WC und des BMI, während bei mit Olanzapin behandelten Patienten ein signifikanter Anstieg beider Parameter auftrat, was zu einem signifikanten Unterschied im 24-wöchigen LSM (Least Square Means) beider Werte zwischen den Gruppen führte.

Wirksamkeitsergebnisse
Die Behandlung mit Ziprasidon führte zu einer signifikanten Abnahme (d. h. Verbesserung) von PANNS-N und Olanzapin in einer signifikanten Abnahme aller PANNS-Subskalen. Alle Abnahmen waren in der Olanzapin-Gruppe signifikant größer als in der Ziprasidon-Gruppe. Es gab jedoch keinen signifikanten Unterschied in der Anzahl der Patienten, bei denen eine Verbesserung der Schizophrenie-Symptome zwischen den Gruppen auftrat, wie von PANNS (7) Ziprasidon vs. 11 Olanzapin; p = 0, 1385). Auf der CGI-S-Skala waren 19 Patienten in der Ziprasidon-Gruppe und 16 in der Olanzapin-Gruppe zu Studienbeginn mäßig bis deutlich krank; Nach 24 Wochen waren es 19 bzw. 12 Patienten (Daten nicht gezeigt). Auf der CGI-I-Skala waren 5 Patienten in der Ziprasidon-Gruppe und 4 in der Olanzapin-Gruppe nach 24 Wochen „stark verbessert“ und 1 in der Ziprasidon-Gruppe und 4 in der Olanzapin-Gruppe „sehr stark verbessert“ (Daten nicht gezeigt). Probanden, die mit Olanzapin behandelt wurden, hatten bessere Bewertungen für Symptom Exazerbation (CGI-S) (OR: 3.321, p = 0.0286) und Verbesserung (CGI-I) (OR: 3.512, p = 0.0307) in Woche 24 als die mit Ziprasidon behandelten. Ähnlich wie bei den PANNS-Ergebnissen gab es jedoch keine signifikanten Unterschiede in der Anzahl der Patienten, die eine Verbesserung von CGI-S (4 unter Ziprasidon vs. 7 unter Olanzapin; p = 0, 2379) und CGI-I (6 unter Ziprasidon vs. 8 unter Olanzapin; p = 0, 2823) zwischen den Gruppen zeigten. Eine bessere Zufriedenheit mit der Medikation, gemessen in KPS, wurde in der Ziprasidon-Gruppe beobachtet als in der Olanzapin-Gruppe (p = 0,0161). Wie in Tabelle 4 gezeigt, nahm der Appetit bei mit Ziprasidon behandelten Patienten ebenfalls signifikant ab, während er in der Olanzapin-Gruppe leicht anstieg. Obwohl der Anstieg bei letzterem keine statistische Signifikanz erreichte, war die Veränderung zwischen den Behandlungsgruppen statistisch unterschiedlich. Es gab keine signifikanten Unterschiede zwischen Blutdruck und Herzfrequenz der Behandlungsgruppen.

Sicherheitsergebnisse
Während dieser Studie wurden keine Todesfälle berichtet. Nebenwirkungen während dieser Studie und Labortests wurden in Tabelle 5 zusammengefasst. Die Hälfte der AE-Ereignisse in jeder Gruppe war behandlungsbedingt (Ziprasidon: Sedierung, Angst, Unruhe, Schizophrenie und Hypersomnie; Olanzapin: Schizophrenie, Unruhe). Einundzwanzig behandlungsbedingte Nebenwirkungen traten bei 15 Probanden (53,6%) in der Ziprasidon-Gruppe und 11 bei 8 Probanden (33,3%) in der Olanzapin-Gruppe auf.

Diskussion
Gemäß dem Studienprotokoll sollten 78 Patienten (39 in jeder Gruppe) auf eine statistische Potenz von 80% untersucht worden sein, um einen Unterschied von 5 kg festzustellen, wobei ein SD = 7, 7 geschätzt wurde. Die endgültige ITT-Population betrug jedoch 50 Patienten. Obwohl dies eine Einschränkung hätte darstellen können, betrug der Unterschied im Körpergewicht zwischen den Gruppen nach 24 Wochen 7,5% (SD = 4,5). Die Leistung betrug 99% und das Ergebnis war besser als ursprünglich geplant.
In Übereinstimmung mit früheren Studien war das Körpergewicht in der Ziprasidon-Gruppe stabil, während in der Olanzapin-Gruppe zu jedem Zeitpunkt ein statistisch signifikanter Anstieg gegenüber dem Ausgangswert auftrat6,7. Dementsprechend kam es bei mit Ziprasidon behandelten Patienten zu keiner signifikanten Veränderung der WC und des BMI, während bei mit Olanzapin behandelten Patienten sowohl die Parameter als auch das Gewicht signifikant zunahmen. In einer früheren Studie34 war der Prozentsatz der mit Olanzapin behandelten Patienten mit einer Gewichtszunahme von ≥ 7% sogar noch höher: 60% der Patienten nach 3 Monaten, der nach 1-jähriger Olanzapin-Behandlung auf 80% anstieg. Die Olanzapin-Dosierung der genannten Studie war ähnlich oder niedriger als die unserer Studie. Diese Tatsache ist nicht überraschend, da die Dosis nicht mit der Gewichtszunahme von Olanzapin zusammenhängt, sondern mit dem therapeutischen Ansprechen25. Patienten mit maximalem Olanzapin-Nutzen bei den Symptomen haben auch das höchste Risiko einer signifikanten Gewichtszunahme.
Variationen in der Nahrungsaufnahme wurden als mögliche Ursache für diese Auswirkungen auf das Gewicht vorgeschlagen. In dieser Studie nahm der Appetit bei mit Ziprasidon behandelten Patienten signifikant ab, während bei mit Olanzapin behandelten Patienten keine signifikanten Veränderungen berichtet wurden. Die Appetitstimulation korreliert stark mit der Affinität des Antipsychotikums zu H1- und alpha1-adrenergen Rezeptoren35, und die Abnahme des Appetits bei mit Ziprasidon behandelten Patienten ist wahrscheinlich mit der geringen Affinität des Arzneimittels zum H1-Rezeptor verbunden. Die mit Olanzapin behandelten Patienten zeigten keinen signifikanten Anstieg des Appetits, aber dennoch einen signifikanten Anstieg des Körpergewichts, was darauf hindeutet, dass andere Mechanismen an der Olanzapin-induzierten Gewichtszunahme beteiligt sein könnten. Tschoner et al. gefunden höhere Nüchternglukose und eine erhöhte Punktzahl in einem Insulinresistenzmodell bei Patienten, die mit Olanzapin behandelt wurden, während dieser Effekt bei mit Ziprasidon behandelten Patienten nicht beobachtet werden konnte, was auf die Beteiligung dieses Effekts an der Olanzapin-induzierten Gewichtszunahme hindeutet6. Tierexperimentelle Studien haben gezeigt, dass Olanzapin, nicht aber Ziprasidon, den Fettverbrauch stimuliert36 und dass eine chronische Behandlung mit Olanzapin die Lipolyse durch Adipozyten37 beeinträchtigt. Frühere Studien haben auch einen Anstieg des Cholesterins, der Triglyceride und des LDL-Cholesterins bei mit Olanzapin behandelten Patienten und nicht bei mit Ziprasidon behandelten Personen festgestellt6,38. Die körperliche Aktivität ist bei mit Olanzapin behandelten Patienten signifikant reduziert39,40, aber der Grad der körperlichen Betätigung in dieser Studie begünstigt Olanzapin gegenüber mit Ziprasidon behandelten Patienten signifikant und erklärt daher nicht den Unterschied in der Gewichtszunahme.
Olanzapin-behandelte Patienten zeigten signifikant bessere Ergebnisse in PANNS-Subskalen als diejenigen unter Ziprasidon-Behandlung, was die Ergebnisse einer früheren Studie bestätigt20. Die Teilnehmer dieser Studie hatten eine vorherige Behandlung aufgrund einer Unverträglichkeit abgebrochen, was den Vergleich mit unserer vorliegenden Studie erschwerte. Die Ziprasidon-Dosis war ähnlich, die Olanzapin-Dosis jedoch höher. Olanzapin zeigt steigende Dosis-Wirkungs-Kurven für Schizophrenie-Symptome21,41, was die stärkere Verbesserung der PANNS im Vergleich zu Ziprasidon in der Studie mit höherer Olanzapin-Dosis erklären könnte. Es wurde jedoch beschrieben, dass Olanzapin-Dosen von mehr als 20 mg/Tag ein höheres Risiko für wichtige Nebenwirkungen mit sich bringen42,43.
Im Gegensatz dazu fanden zwei andere Studien keinen Unterschied in der Wirksamkeit zwischen den Behandlungen. Die Studie von Lieberman et al.7 zeigten keine signifikanten Unterschiede in der Veränderung des PANNS-Gesamtscores gegenüber dem Ausgangswert noch zwischen Olanzapin und Ziprasidon. Ebenso die Studie von Simpson et al. zeigte keine Unterschiede in der Verbesserung des PANNS-Scores zwischen den Gruppen26,27. Diese Studien verwendeten ähnliche flexible Dosen wie die von uns verwendeten und zeigten die gleiche Wirksamkeit bei der Behandlung mit Olanzapin oder Ziprasidon. Eine plausible Erklärung könnte sein, dass Ziprasidon zwar zur Behandlung von Schizophrenie in einem Dosisbereich von 40-160 mg / Tag indiziert ist, die optimale Dosis jedoch näher bei 120 mg / Tag liegt44 und die mittlere Dosis unserer Studie, etwas niedriger als die mittleren Dosen der beiden anderen Studien, möglicherweise nicht optimal war. Darüber hinaus könnte die bioverfügbare Dosis noch niedriger gewesen sein. Obwohl der Ziprasidon-Plasmaspiegel eine signifikante positive Korrelation mit der Rezeptorbelegung aufweist, sagt die Dosis den Plasmaspiegel nicht voraus44, da Nahrung die Ziprasidon-Absorption beeinträchtigen kann45, was vom Zeitpunkt der Medikation abhängen kann.
In der Ziprasidon-Gruppe gab es 1, 6-mal mehr Behandlungsabbrüche als in der Olanzapin-Gruppe, was einen höheren Fachunterschied zwischen beiden Behandlungen zeigte als in anderen Studien7,20. Die meisten Nebenwirkungen waren in beiden Gruppen leicht oder mittelschwer und schlossen unerwünschte Ereignisse ein, die normalerweise bei diesen Arzneimitteln beobachtet wurden20,34. Die PPS-Skala zeigt an, dass Patienten Ziprasidon gegenüber Olanzapin bevorzugten.
Diese Studie zeigt eine signifikant stärkere Zunahme des Körpergewichts in Woche 24 bei Patienten, die mit Olanzapin behandelt wurden, als bei Patienten, die mit Ziprasidon behandelt wurden. Die berichtete progressive Appetitreduktion könnte zu der leichten Abnahme des Körpergewichts beigetragen haben, die bei mit Ziprasidon behandelten Patienten beobachtet wurde. Auf der anderen Seite zeigten Patienten unter Olanzapin einen gewissen Anstieg ihres Appetits, aber Veränderungen in dieser Gruppe waren nicht signifikant und zeigten nicht den progressiven Anstieg der Variation, über den Ziprasidon-Patienten berichteten. Die visuelle Analogskala ist eine subjektive Methode zur Messung des Appetits, und obwohl die Unterschiede im Appetit signifikant waren und die Ergebnisse während der Studie positiv zu sein schienen, scheinen ein leicht erhöhter Appetit oder Bewegungsmangel nicht für die Gewichtszunahme bei mit Olanzapin behandelten Patienten verantwortlich zu sein, was auf andere Mechanismen hindeutet. Fetthaltige Nahrungsmittelpräferenz und metabolische Dysregulation können eine Rolle bei der zugrunde liegenden Ursache spielen. Sowohl die Ziprasidon- als auch die Olanzapin-Gruppe wurden gut vertragen und zeigten in Woche 24 eine Abnahme der PANSS-Werte. Obwohl die Abnahme für alle Scores in der Olanzapin-Gruppe signifikant größer war, kann die Möglichkeit einer verringerten Bioverfügbarkeit von Ziprasidon nicht ausgeschlossen werden.
Bei Patienten, bei denen eine Gewichtszunahme während der Behandlung von Schizophrenie ein Problem darstellen kann, sollte die Behandlung mit Ziprasidon aufgrund seines guten Sicherheitsprofils in diesem Bereich versucht werden.
Danksagungen
Medical Writing Support wurde von Medical Statistics Consulting bereitgestellt und von Pfizer finanziert.
1. Allison DB, Fontaine KR, Heo M, Mentore JL, Cappelleri JC, Chandler LP, et al. Die Verteilung des Body-Mass-Index bei Personen mit und ohne Schizophrenie. J Clin Psychiatrie 1999; 60(4): 215-220.
2. Baptista T, De Mendoza S, Beaulieu S, Bermudez A, Martinez M. Das metabolische Syndrom während der Behandlung mit atypischen Antipsychotika: Mechanismen und Management. Metab Syndr Relat Disord 2004; 2(4): 290-307.
3. Enger C, Weatherby L, Reynolds RF, Glasser DB, Walker AM. Schwerwiegende kardiovaskuläre Ereignisse und Mortalität bei Patienten mit Schizophrenie. J Nerv Ment Dis 2004; 192(1): 19-27.
4. Allison DB, Mentore JL, Heo M, Chandler LP, Cappelleri JC, Infante MC, et al. Antipsychotisch-induzierte Gewichtszunahme: eine umfassende Forschungssynthese. Am J Psychiatrie 1999; 156(11): 1686-1696.
5. Weitere Informationen finden Sie in den folgenden Abschnitten: Kane JM, Barrett EJ, Casey DE, Correll CU, Gelenberg AJ, Klein S, et al. Metabolische Wirkungen der Behandlung mit atypischen Antipsychotika. J Clin Psychiatrie 2004; 65 (11): 1447-1455.
6. Es sind keine frei zugänglichen ergänzenden Materialien verfügbar Zitation Tschoner A, Engl J, Rettenbacher M, Kaser S, Tatarczyk T, et al. Auswirkungen von sechs Antipsychotika der zweiten Generation auf Körpergewicht und Stoffwechsel – Risikobewertung und Ergebnisse einer prospektiven Studie. Pharmacopsychiatry 2009; 42(1): 29-34.
7. Lieberman JA, Stroup TS, McEvoy JP, Swartz MS, Rosenheck RA, Perkins DO, et al. Wirksamkeit von Antipsychotika bei Patienten mit chronischer Schizophrenie. N Engl J Med 2005; 353(12): 1209-1223.
8. König DJ. Medikamentöse Behandlung der negativen Symptome der Schizophrenie. Eur Neuropsychopharmacol 1998; 8(1): 33-42.
9. Weiden P, Aquila R, Standard J. Atypische Antipsychotika und Langzeitergebnis bei Schizophrenie. J Clin Psychiatrie 1996; 57(Suppl 11): 53-60.
10. Dr. Med. Priori S. Kardiovaskuläre Risiken einer atypischen Behandlung mit Antipsychotika. Pharmacoepidemiol Droge Saf 2007; 16 (8): 882-890.
11. Gao K, Ganocy SJ, Gajwani P, Muzina DJ, Kemp DE, Calabrese JR. Eine Überprüfung der Empfindlichkeit und Verträglichkeit von Antipsychotika bei Patienten mit bipolarer Störung oder Schizophrenie: Fokus auf Somnolenz. J Clin Psychiatrie 2008; 69(2): 302-309.
12. Nasrallah HA. Atypische antipsychotisch induzierte metabolische Nebenwirkungen: Erkenntnisse aus Rezeptorbindungsprofilen. Mol Psychiatrie 2008; 13(1): 27-35.
13. Baldwin D, Mayers A. Sexuelle Nebenwirkungen von Antidepressiva und Antipsychotika. Adv Psychiatr, 2003; 9(3): 202-210.
14. Montejo AL. Prolaktinbewusstsein: eine wesentliche Überlegung für die körperliche Gesundheit bei Schizophrenie. Eur Neuropsychopharmacol 2008; 18(Suppl 2): S108-114.
15. Keck PE, Jr., McElroy SL, Arnold LM. Ziprasidon: ein neues atypisches Antipsychotikum. Experte Opin Pharmacother 2001; 2(6): 1033-1042.
16. Kane JM, Khanna S, Rajadhyaksha S, Giller E. Wirksamkeit und Verträglichkeit von Ziprasidon bei Patienten mit behandlungsresistenter Schizophrenie. Int Clin Psychopharmacol 2006; 21(1): 21-28.
17. Es sind keine frei zugänglichen ergänzenden Materialien verfügbar Zitationen von Keck P, Jr., Buffenstein A, Ferguson J, Feighner J, Jaffe W, Harrigan EP, et al. Ziprasidon 40 und 120 mg / Tag bei akuter Exazerbation von Schizophrenie und schizoaffektiver Störung: eine 4-wöchige placebokontrollierte Studie. Psychopharmakologie (Berl) 1998; 140(2): 173-184.
18. Montejo AL, Rico-Villademoros F. Veränderungen der Sexualfunktion bei ambulanten Patienten mit Schizophrenie oder anderen psychotischen Störungen, die in der klinischen Praxis mit Ziprasidon behandelt wurden: eine 3-monatige prospektive Beobachtungsstudie. J Clin Psychopharmacol 2008; 28(5): 568-570.
19. Kingsbury SJ, Fayek M, Trufasiu D, Zada J, Simpson GM. Die offensichtlichen Auswirkungen von Ziprasidon auf Plasmalipide und Glukose. J Clin Psychiatrie 2001; 62(5): 347-349.
20. Stroup TS, Lieberman JA, McEvoy JP, Swartz MS, Davis SM, Rosenheck RA, et al. Wirksamkeit von Olanzapin, Quetiapin, Risperidon und Ziprasidon bei Patienten mit chronischer Schizophrenie nach Absetzen eines früheren atypischen Antipsychotikums. Am J Psychiatrie 2006; 163(4): 611-622.
21. Beasley CM, Jr., Tollefson G, Tran P, Satterlee W, Sanger T, Hamilton S. Olanzapin versus Placebo und Haloperidol: Akutphasenergebnisse der nordamerikanischen doppelblinden Olanzapin-Studie. Neuropsychopharmakologie 1996; 14 (2): 111-123.
22. Conley RR, Mahmoud R. Eine randomisierte Doppelblindstudie mit Risperidon und Olanzapin zur Behandlung von Schizophrenie oder schizoaffektiver Störung. Am J Psychiatrie 2001; 158(5): 765-774.
23. Gomez JC, Crawford AM. Überlegene Wirksamkeit von Olanzapin gegenüber Haloperidol: Analyse von Patienten mit Schizophrenie aus einer multizentrischen internationalen Studie. J Clin Psychiatrie 2001; 62(Suppl 2): 6-11.
24. Bobes J, Rejas J, Garcia-Garcia M, Rico-Villademoros F, Garcia-Portilla MP, Fernandez I, et al. Gewichtszunahme bei Patienten mit Schizophrenie, die mit Risperidon, Olanzapin, Quetiapin oder Haloperidol behandelt wurden: ergebnisse der EIRE-Studie. Schizophrenie 2003; 62(1-2): 77-88.
25. Kinon BJ, Kaiser CJ, Ahmed S, Rotelli MD, Kollack-Walker S. Assoziation zwischen früher und schneller Gewichtszunahme und Gewichtsveränderung über ein Jahr Olanzapin-Therapie bei Patienten mit Schizophrenie und verwandten Störungen. J Clin Psychopharmacol 2005; 25(3): 255-258.
26. Simpson GM, Glick ID, Weiden PJ, Romano SJ, Siu CO. Randomisierter, kontrollierter, doppelblinder multizentrischer Vergleich der Wirksamkeit und Verträglichkeit von Ziprasidon und Olanzapin bei akut kranken stationären Patienten mit Schizophrenie oder schizoaffektiver Störung. Am J Psychiatrie 2004; 161(10): 1837-1847.
27. Simpson GM, Weiden P, Pigott T, Murray S, Siu CO, Romano SJ. Sechsmonatige, verblindete, multizentrische Fortsetzungsstudie mit Ziprasidon versus Olanzapin bei Schizophrenie. Am J Psychiatrie 2005; 162(8): 1535-1538.
28. In: American Psychiatric Association., Amerikanische Psychiatrische Vereinigung. Task Force für DSM-IV. Diagnostisches und statistisches Handbuch für psychische Störungen: DSM-IV-TR. 4. Aufl. Washington, DC: Amerikanische Psychiatrische Vereinigung; 2000.
29. WMA. Erklärung der Weltärztekammer von Helsinki: ethische Grundsätze für die medizinische Forschung am Menschen. In: J Postgraduate Med. 2002; 48(3): 206-208.
30. Kay SR, Fiszbein A, Opler LA. Die positive und negative Syndromskala (PANSS) für Schizophrenie. Schizophrenie 1987; 13(2): 261-276.
31. Guy W, Nationales Institut für psychische Gesundheit (USA). Forschungszweig Psychopharmakologie., Frühes klinisches Arzneimittelbewertungsprogramm. ECDEU-Bewertungshandbuch für Psychopharmakologie. Hrsg. In: Rockville, Md. In : U. S. Dept. ministerium für Gesundheit, Bildung und Wohlfahrt, öffentlicher Gesundheitsdienst, Verwaltung für Alkohol, Drogenmissbrauch und psychische Gesundheit, Nationales Institut für psychische Gesundheit, Forschungszweig Psychopharmakologie, Abteilung für extramurale Forschungsprogramme; 1976.
32. Feeny D, Furlong W, Boyle M, Torrance GW. Klassifizierungssysteme für den Gesundheitsstatus mit mehreren Attributen. In: Health Utilities Index. Pharmacoeconomics 1995; 7(6): 490-502.
33. Ruiz M, Rejas J, Soto J, Pardo A, Rebollo I. Anpassung und Validierung des Health Utilities Index Mark 3 in spanische und Korrekturnormen für die spanische Bevölkerung. Med Clin (Barc) 2003; 120(3): 89-96.
34. McEvoy JP, Lieberman JA, Perkins DO, Hamer RM, Gu H, Lazarus A, et al. Wirksamkeit und Verträglichkeit von Olanzapin, Quetiapin und Risperidon bei der Behandlung der frühen Psychose: ein randomisierter, doppelblinder 52-Wochen-Vergleich. Am J Psychiatrie 2007; 164(7): 1050-1060.
35. Baptista T, Zarate J, Joober R, Colasante C, Beaulieu S, Paez X, et al. Arzneimittelinduzierte Gewichtszunahme, ein Hindernis für eine erfolgreiche Pharmakotherapie: Konzentrieren Sie sich auf Antipsychotika. Curr Drug Targets 2004; 5(3): 279-299.
36. Hartfield AW, Moore NA, Clifton PG. Auswirkungen atypischer Antipsychotika auf die Intralipidaufnahme und die kokaininduzierte Hyperaktivität bei Ratten. Neuropsychopharmakologie 2006; 31 (9): 1938-1945.
37. Minet-Ringuet J, Auch PC, Valet P, Carpene C, Visentin V, Prevot D, et al. Veränderungen des Fettstoffwechsels und der Genexpression in Adipozyten von Ratten während einer chronischen Olanzapin-Behandlung. Mol Psychiatrie 2007; 12(6): 562-571.
38. Rettenbacher MA, Ebenbichler C, Hofer A, Kemmler G, Baumgartner S, Edlinger M, et al. Frühe Veränderungen der Plasmalipide während der Behandlung mit atypischen Antipsychotika. Int Clin Psychopharmacol 2006; 21(6): 369-372.
39. Weitere Informationen finden Sie in folgenden Dokumenten: Fell MJ, Anjum N, Dickinson K, Marshall KM, Peltola LM, Vickers S, et al. Die unterschiedlichen Auswirkungen der subchronischen antipsychotischen medikamentösen Behandlung auf Makronährstoffauswahl, Körpergewicht, Adipositas und Metabolismus bei weiblichen Ratten. Psychopharmakologie (Berl) 2007; 194(2): 221-231.
40. Fleischhaker C, Heiser P, Hennighausen K, Herpertz-Dahlmann B, Holtkamp K, Mehler-Wex C, et al. Klinisches Drogenmonitoring in der Kinder- und Jugendpsychiatrie: Nebenwirkungen atypischer Neuroleptika. J. Adolesc Psychopharmacol 2006; 16(3): 308-316.
41. Fanous A, Lindenmayer JP. Schizophrenie und schizoaffektive Störung mit hohen Dosen von Olanzapin behandelt. J Clin Psychopharmacol 1999; 19(3): 275-276.
42. Farah A. Atypizität atypischer Antipsychotika. Prim Pflege Begleiter J Clin Psychiatrie 2005; 7(6): 268-274.
43. Reich J. Verwendung von hochdosiertem Olanzapin bei refraktärer Psychose. Am J Psychiatrie 1999; 156(4): 661.
44. Mamo D, Kapur S, Shammi CM, Papatheodorou G, Mann S, Therrien F, et al. Eine PET-Studie zur Belegung des Dopamin-D2- und Serotonin-5-HT2-Rezeptors bei Patienten mit Schizophrenie, die mit therapeutischen Dosen von Ziprasidon behandelt wurden. Am J Psychiatrie 2004; 161(5): 818-825.
45. Es sind keine frei zugänglichen ergänzenden Materialien verfügbar in: Hamelin BA, Allard S., Laplante L., Miceli J., Wilner KD, Tremblay J., et al. Die Wirkung des Timings einer Standardmahlzeit auf die Pharmakokinetik und Pharmakodynamik des neuartigen atypischen Antipsychotikums Ziprasidon. Pharmakotherapie 1998; 18(1): 9-15.