Generischer Name: Fluocinonid
Darreichungsform: Salbe
Medizinisch überprüft von Drugs.com . Zuletzt aktualisiert am Dezember 22, 2020.
- Übersicht
- Nebenwirkungen
- Dosierung
- Professionell
- Wechselwirkungen
- Mehr
Nur Rx
Der Markenname Lidex wurde in den USA eingestellt Wenn generische Versionen dieses Produkts von der FDA zugelassen wurden, sind möglicherweise generische Äquivalente verfügbar.
Lidex Beschreibung
Lidex® (Fluocinonid) Salbe 0,05% ist zur topischen Verabreichung bestimmt. Die aktive Komponente ist das Corticosteroid Fluocinonid, das der 21-Acetatester von Fluocinolonacetonid ist und den chemischen Namen Pregna-1,4-dien-3,20-dion, 21- (acetyloxy) -6,9-difluor-11-hydroxy-16,17–, (6α, 11β, 16α) – hat. Es hat die folgende chemische Struktur:
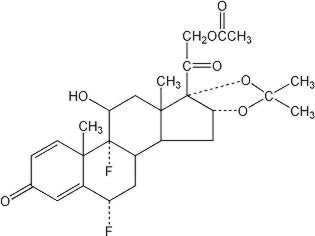
Lidex Salbe enthält Fluocinonid 0.5 mg / g in einer speziell formulierten Salbenbasis bestehend aus Glycerinmonostearat, weißem Petrolatum, Propylencarbonat, Propylenglykol und weißem Wachs. Es bietet die okklusiven und erweichenden Wirkungen, die in einer Salbe wünschenswert sind.
In dieser Formulierung ist der Wirkstoff vollständig in Lösung.
Lidex – Klinische Pharmakologie
Topische Kortikosteroide wirken entzündungshemmend, juckreizstillend und vasokonstriktiv.
Der Mechanismus der entzündungshemmenden Wirkung der topischen Kortikosteroide ist unklar. Verschiedene Labormethoden, einschließlich Vasokonstriktor-Assays, werden verwendet, um Potenzen und / oder klinische Wirksamkeiten der topischen Kortikosteroide zu vergleichen und vorherzusagen. Es gibt einige Hinweise darauf, dass eine erkennbare Korrelation zwischen vasokonstriktorischer Potenz und therapeutischer Wirksamkeit beim Menschen besteht.
Pharmakokinetik
Das Ausmaß der perkutanen Resorption von topischen Kortikosteroiden wird durch viele Faktoren bestimmt, einschließlich des Vehikels, der Integrität der epidermalen Barriere und der Verwendung von Okklusivverbänden.
Topische Kortikosteroide können von normaler intakter Haut aufgenommen werden. Entzündungen und/oder andere Krankheitsprozesse in der Haut erhöhen die perkutane Resorption. Okklusivverbände erhöhen die perkutane Resorption topischer Kortikosteroide erheblich. Somit können Okklusivverbände ein wertvoller therapeutischer Zusatz zur Behandlung resistenter Dermatosen sein (siehe DOSIERUNG UND VERABREICHUNG).
Nach der Resorption durch die Haut werden topische Kortikosteroide über pharmakokinetische Wege ähnlich wie systemisch verabreichte Kortikosteroide gehandhabt. Kortikosteroide sind in unterschiedlichem Maße an Plasmaproteine gebunden. Kortikosteroide werden hauptsächlich in der Leber metabolisiert und dann über die Nieren ausgeschieden. Einige der topischen Kortikosteroide und ihre Metaboliten werden auch in die Galle ausgeschieden.
Indikationen und Verwendung für Lidex
Lidex Salbe ist zur Linderung der entzündlichen und juckenden Manifestationen von Kortikosteroid-responsiven Dermatosen indiziert.
Kontraindikationen
Topische Kortikosteroide sind bei Patienten mit Überempfindlichkeit gegen einen der Bestandteile des Präparats in der Vorgeschichte kontraindiziert.
Vorsichtsmaßnahmen
Allgemein
Die systemische Resorption topischer Kortikosteroide führte bei einigen Patienten zu einer reversiblen Unterdrückung der Hypothalamus-Hypophysen-Nebennieren-Achse (HPA), Manifestationen des Cushing-Syndroms, Hyperglykämie und Glukosurie.
Bedingungen, die die systemische Resorption verstärken, umfassen die Anwendung der stärkeren Steroide, die Verwendung über große Oberflächen, die längere Anwendung und die Zugabe von Okklusivverbänden.Daher sollten Patienten, die eine große Dosis eines potenten topischen Steroids erhalten, das auf eine große Oberfläche oder unter einen Okklusivverband aufgetragen wird, regelmäßig auf Anzeichen einer Unterdrückung der HPA-Achse untersucht werden, indem die Tests für freies Cortisol im Urin und ACTH-Stimulation verwendet werden. Wenn eine Unterdrückung der HPA-Achse festgestellt wird, sollte versucht werden, das Arzneimittel abzusetzen, die Häufigkeit der Anwendung zu verringern oder ein weniger wirksames Steroid zu ersetzen.
Die Wiederherstellung der HPA-Achsenfunktion erfolgt im Allgemeinen sofort und vollständig nach Absetzen des Arzneimittels. Selten können Anzeichen und Symptome eines Steroidentzugs auftreten, die zusätzliche systemische Kortikosteroide erfordern.
Kinder können proportional größere Mengen topischer Kortikosteroide aufnehmen und sind daher anfälliger für systemische Toxizität (siehe VORSICHTSMAßNAHMEN – Pädiatrische Anwendung). Wenn sich eine Reizung entwickelt, sollten topische Kortikosteroide abgesetzt und eine geeignete Therapie eingeleitet werden.Wie bei jedem topischen Corticosteroid-Produkt kann eine längere Anwendung zu einer Atrophie der Haut und des Unterhautgewebes führen. Bei Anwendung an intertriginösen oder Beugebereichen oder im Gesicht kann dies auch bei kurzfristiger Anwendung auftreten.
Bei dermatologischen Infektionen sollte die Verwendung eines geeigneten antimykotischen oder antibakteriellen Mittels eingeleitet werden. Wenn ein günstiges Ansprechen nicht sofort eintritt, sollte das Kortikosteroid abgesetzt werden, bis die Infektion ausreichend kontrolliert wurde.
Informationen für den Patienten
Patienten, die topische Kortikosteroide verwenden, sollten die folgenden Informationen und Anweisungen erhalten:
- Dieses Medikament ist gemäß den Anweisungen des Arztes zu verwenden. Es ist nur zur äußerlichen Anwendung bestimmt. Kontakt mit den Augen vermeiden.
- Patienten sollten angewiesen werden, dieses Medikament nicht für andere Erkrankungen als die, für die es verschrieben wurde, zu verwenden.
- Der behandelte Hautbereich sollte nicht bandagiert oder anderweitig bedeckt oder umwickelt werden, um okklusiv zu sein, es sei denn, dies wird vom Arzt verordnet.
- Patienten sollten Anzeichen lokaler Nebenwirkungen melden, insbesondere unter Okklusivverband.
- Eltern von pädiatrischen Patienten sollten darauf hingewiesen werden, bei einem Kind, das im Windelbereich behandelt wird, keine eng anliegenden Windeln oder Plastikhosen zu verwenden, da diese Kleidungsstücke Okklusivverbände darstellen können.
Labortests
Die folgenden Tests können hilfreich sein, um die Unterdrückung der HPA-Achse zu bewerten:
Urinary free Cortisol test
ACTH-Stimulationstest
Karzinogenese, Mutagenese und Beeinträchtigung der Fertilität
Es wurden keine Langzeitstudien an Tieren durchgeführt, um das karzinogene Potenzial oder die Wirkung von topischen Kortikosteroiden auf die Fertilität zu bewerten.
Studien zur Bestimmung der Mutagenität mit Prednisolon und Hydrocortison haben negative Ergebnisse ergeben.
Schwangerschaftskategorie C
Kortikosteroide sind bei Labortieren im Allgemeinen teratogen, wenn sie systemisch in relativ niedrigen Dosierungen verabreicht werden. Es wurde gezeigt, dass die wirksameren Kortikosteroide nach dermaler Anwendung bei Labortieren teratogen sind. Es gibt keine adäquaten und gut kontrollierten Studien an schwangeren Frauen zu teratogenen Wirkungen von topisch angewendeten Kortikosteroiden. Daher sollten topische Kortikosteroide während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt. Arzneimittel dieser Klasse sollten nicht in großem Umfang bei schwangeren Patienten, in großen Mengen oder über einen längeren Zeitraum angewendet werden.
Stillende Mütter
Es ist nicht bekannt, ob die topische Verabreichung von Kortikosteroiden zu einer ausreichenden systemischen Resorption führen kann, um nachweisbare Mengen in der Muttermilch zu produzieren. Systemisch verabreichte Kortikosteroide werden in Mengen in die Muttermilch ausgeschieden, die wahrscheinlich keine schädlichen Auswirkungen auf das Kind haben. Dennoch ist Vorsicht geboten, wenn topische Kortikosteroide einer stillenden Frau verabreicht werden.
Pädiatrische Anwendung
Pädiatrische Patienten zeigen möglicherweise eine größere Anfälligkeit für topische Corticosteroid-induzierte Hypothalm-Hypophysen-Nebennieren-Achse (HPA) Unterdrückung und Cushing-Syndrom als reife Patienten aufgrund einer größeren Hautoberfläche zu Körpergewicht Verhältnis.
HPA-Achsensuppression, Cushing-Syndrom und intrakranielle Hypertonie wurden bei Kindern berichtet, die topische Kortikosteroide erhielten. Manifestationen der Nebennierensuppression bei Kindern umfassen lineare Wachstumsverzögerung, verzögerte Gewichtszunahme, niedrige Plasma-Cortisolspiegel und fehlende Reaktion auf ACTH-Stimulation. Manifestationen der intrakraniellen Hypertonie sind prall gefüllte Fontanellen, Kopfschmerzen und bilaterale Papillenödeme.
Die Verabreichung von topischen Kortikosteroiden an Kinder sollte auf die geringste Menge beschränkt sein, die mit einem wirksamen Therapieschema vereinbar ist. Eine chronische Kortikosteroidtherapie kann das Wachstum und die Entwicklung von Kindern beeinträchtigen.
Nebenwirkungen
Die folgenden lokalen Nebenwirkungen werden selten bei topischen Kortikosteroiden berichtet, können jedoch bei Verwendung von Okklusivverbänden häufiger auftreten. Diese Reaktionen sind in einer ungefähren absteigenden Reihenfolge ihres Auftretens aufgeführt:
| Burning | Perioral dermatitis |
| Itching | Allergic contact dermatitis |
| Irritation | Maceration of the skin |
| Dryness | Secondary infection |
| Folliculitis | Skin atrophy |
| Hypertrichosis | Striae |
| Acneiform eruptions | Miliaria |
| Hypopigmentation |
Overdosage
Topically applied corticosteroids can be absorbed in sufficient amounts to produce systemic effects (see PRECAUTIONS).
Lidex-Dosierung und -verabreichung
Lidex-Salbe wird im Allgemeinen je nach Schwere der Erkrankung zwei- bis viermal täglich als dünner Film auf die betroffene Stelle aufgetragen.
Okklusivverbände können zur Behandlung von Psoriasis oder widerspenstigen Zuständen verwendet werden.
Wenn sich eine Infektion entwickelt, sollte die Verwendung der Okklusivverbände abgebrochen und eine geeignete antimikrobielle Therapie eingeleitet werden.
Wie wird Lidex geliefert?
Lidex® (Fluocinonid) Salbe 0.05% wird geliefert in
15 g Tube –NDC 99207-514-13
30 g Tube –NDC 99207-514-14
60 g Tube –NDC 99207-514-17
120 g Tube –NDC 99207-514-22
Bei Raumtemperatur lagern. Vermeiden Sie Temperaturen über 30 °C (86 ° F).4,017,615
Hergestellt für:
MEDICIS, The Dermatology Company®
Scottsdale, AZ 85258
von: Patheon, Inc.
Mississauga, Ontario
Canada L5N 7K9
IN-5070/S
| Lidex fluocinonide ointment |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Labeler – MEDICIS
Frequently asked questions
- Is it used for hair loss?
- What is a substitute for fluocinonide cream?
- Is fluocinonide an antifungal cream?
- How long should you use fluocinonide for?
- What is fluocinonide cream good for?
- Kann Fluocinonid verwendet werden, um einen Poison Ivy Hautausschlag zu behandeln?
- Ist es ein Steroid?
- Ist das ein Antibiotikum?
Mehr über Lidex (fluocinonide topical)
- Nebenwirkungen
- Während der Schwangerschaft oder Stillzeit
- Dosierungsinformationen
- Wechselwirkungen mit anderen Medikamenten
- 8 Bewertungen
- Generische Verfügbarkeit
- : topische Steroide
Verbraucherressourcen
- Erweiterte Lesung
- Lidex Mild (Erweiterte Lesung)
- Lidex Regular (Erweiterte Lesung)
Professionelle Ressourcen
- Verschreibungsinformationen
- Lidex Topical Solution (FDA)
- Lidex Gel (FDA)
Andere Marken Vanos, Lidex-E
Zugehörige Behandlungsleitfäden
- Atopische Dermatitis
- Ekzem
- Dermatitis
- Psoriasis
Medizinischer Haftungsausschluss