Generiskt Namn: fluocinonid
doseringsform: salva
medicinskt granskad av Drugs.com. Senast uppdaterad den 22 Dec 2020.
- översikt
- biverkningar
- dosering
- Professional
- interaktioner
- mer
RX endast
varumärket Lidex har upphört i USA om generiska versioner av denna produkt har godkänts av FDA kan det finnas generiska ekvivalenter tillgängliga.
Lidex beskrivning
lidex Aci (fluocinonid) salva 0,05% är avsedd för topisk administrering. Den aktiva komponenten är kortikosteroidfluocinonid, som är 21-acetatestern av fluocinolonacetonid och har det kemiska namnet pregna-1,4-dien-3,20-dion,21-(acetyloxi)-6,9-difluoro-11-hydroxi-16,17–,(6 kg,11 kg,16 kg)-. Den har följande kemiska struktur:
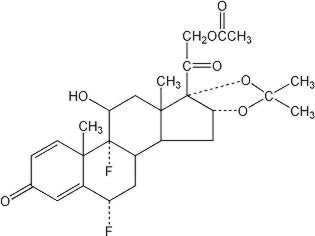
Lidex salva innehåller fluocinonid 0.5 mg / g i en speciellt formulerad salvbas bestående av glycerylmonostearat, vit petrolatum, propylenkarbonat, propylenglykol och vitt vax. Det ger de ocklusiva och mjukgörande effekterna önskvärda i en salva.
i denna formulering är den aktiva beståndsdelen helt i lösning.
Lidex-klinisk farmakologi
topikala kortikosteroider delar antiinflammatoriska, anti-pruritiska och vasokonstriktiva åtgärder.
mekanismen för antiinflammatorisk aktivitet hos de topiska kortikosteroiderna är oklart. Olika laboratoriemetoder, inklusive vasokonstriktoranalyser, används för att jämföra och förutsäga potenser och/eller kliniska effekter av topikala kortikosteroider. Det finns vissa bevis som tyder på att det finns en igenkännlig korrelation mellan vasokonstrictorpotens och terapeutisk effekt hos människa.
farmakokinetik
omfattningen av perkutan absorption av topikala kortikosteroider bestäms av många faktorer inklusive fordonet, epidermalbarriärens integritet och användningen av ocklusiva förband.
topikala kortikosteroider kan absorberas från normal intakt hud. Inflammation och / eller andra sjukdomsprocesser i huden ökar perkutan absorption. Ocklusiva förband ökar signifikant den perkutana absorptionen av topikala kortikosteroider. Således kan ocklusiva förband vara ett värdefullt terapeutiskt tillägg för behandling av resistenta dermatoser (se dosering och administrering).
när de absorberats genom huden hanteras topikala kortikosteroider genom farmakokinetiska vägar som liknar systemiskt administrerade kortikosteroider. Kortikosteroider är bundna till plasmaproteiner i varierande grad. Kortikosteroider metaboliseras främst i levern och utsöndras sedan av njurarna. Några av de topikala kortikosteroiderna och deras metaboliter utsöndras också i gallan.
indikationer och användning för Lidex
Lidex salva är indicerat för lindring av inflammatoriska och pruritiska manifestationer av kortikosteroidresponsiva dermatoser.
kontraindikationer
topikala kortikosteroider är kontraindicerade hos patienter med överkänslighet mot någon av komponenterna i preparatet.
försiktighetsåtgärder
allmänt
systemisk absorption av topikala kortikosteroider har producerat reversibel hypotalamus-hypofys-adrenal (HPA) axelundertryckning, manifestationer av Cushings syndrom, hyperglykemi och glukosuri hos vissa patienter.
förhållanden som ökar systemisk absorption inkluderar applicering av de mer potenta steroiderna, användning över stora ytor, långvarig användning och tillsats av ocklusiva förband.därför bör patienter som får en stor dos av en potent topisk steroid applicerad på en stor yta eller under ett ocklusivt förband utvärderas regelbundet för bevis på hPa-axelundertryckning med hjälp av urinfria kortisol-och ACTH-stimuleringstester. Om hPa-axelundertryckning noteras bör man försöka dra tillbaka läkemedlet, minska appliceringsfrekvensen eller ersätta en mindre potent steroid.
återhämtning av HPA-axelfunktionen är i allmänhet snabb och fullständig vid avbrytande av läkemedlet. Sällan kan tecken och symtom på steroiduttag uppstå, vilket kräver kompletterande systemiska kortikosteroider.
barn kan absorbera proportionellt större mängder topikala kortikosteroider och därmed vara mer mottagliga för systemisk toxicitet (se försiktighetsåtgärder – pediatrisk användning). Om irritation utvecklas ska topikala kortikosteroider avbrytas och lämplig behandling sättas in.
som med alla topiska kortikosteroidprodukter kan långvarig användning ge atrofi i huden och subkutan vävnad. Vid användning på intertriginous eller flexor områden, eller i ansiktet, kan detta inträffa även vid kortvarig användning.
i närvaro av dermatologiska infektioner bör användning av ett lämpligt antifungalt eller antibakteriellt medel inledas. Om ett gynnsamt svar inte uppstår omedelbart, bör kortikosteroiden avbrytas tills infektionen har kontrollerats tillräckligt.
information för patienten
patienter som använder topikala kortikosteroider ska få följande information och instruktioner:
- detta läkemedel ska användas enligt instruktioner från läkaren. Det är endast för extern användning. Undvik kontakt med ögonen.
- patienter bör rekommenderas att inte använda detta läkemedel för någon annan sjukdom än den för vilken den ordinerades.
- det behandlade hudområdet ska inte bandas eller på annat sätt täckas eller lindas så att det är ocklusivt om inte läkaren instruerar det.
- patienter ska rapportera tecken på lokala biverkningar, särskilt under ocklusivt förband.
- föräldrar till barn ska rådas att inte använda åtsittande blöjor eller plastbyxor på ett barn som behandlas i blöjområdet, eftersom dessa plagg kan utgöra ocklusiva förband.
laboratorietester
följande tester kan vara till hjälp vid utvärdering av HPA-axelundertryckning:
Urinfritt kortisoltest
ACTH-stimuleringstest
karcinogenes, mutagenes och nedsatt fertilitet
långtidsstudier på djur har inte utförts för att utvärdera den karcinogena potentialen eller effekten på fertiliteten hos topikala kortikosteroider.
studier för att bestämma mutagenicitet med prednisolon och hydrokortison har avslöjat negativa resultat.
graviditetskategori C
kortikosteroider är generellt teratogena hos laboratoriedjur när de administreras systemiskt vid relativt låga dosnivåer. De mer potenta kortikosteroiderna har visat sig vara teratogena efter dermal applicering hos laboratoriedjur. Det finns inga adekvata och välkontrollerade studier på gravida kvinnor på teratogena effekter från topiskt applicerade kortikosteroider. Därför bör topikala kortikosteroider endast användas under graviditet om den potentiella nyttan motiverar den potentiella risken för fostret. Läkemedel i denna klass ska inte användas i stor utsträckning på gravida patienter, i stora mängder eller under långa perioder.
ammande mödrar
det är inte känt om topisk administrering av kortikosteroider kan leda till tillräcklig systemisk absorption för att producera detekterbara mängder i bröstmjölk. Systemiskt administrerade kortikosteroider utsöndras i bröstmjölk i mängder som sannolikt inte har en skadlig effekt på spädbarnet. Ändå bör försiktighet iakttas när topikala kortikosteroider administreras till en ammande kvinna.
pediatrisk användning
pediatriska patienter kan visa större känslighet för topisk kortikosteroidinducerad hypotalmisk-hypofys-adrenal (HPA) axelundertryckning och Cushings syndrom än mogna patienter på grund av ett större hudyta till kroppsviktförhållande.
hPa-axelundertryckning, Cushings syndrom och intrakraniell hypertoni har rapporterats hos barn som får topikala kortikosteroider. Manifestationer av adrenal suppression hos barn inkluderar linjär tillväxthämning, försenad viktökning, låga plasmakortisolnivåer och frånvaro av svar på ACTH-stimulering. Manifestationer av intrakraniell hypertoni inkluderar utbuktande fontaneller, huvudvärk och bilateralt papilledema.
administrering av topikala kortikosteroider till barn bör begränsas till den minsta mängd som är kompatibel med en effektiv terapeutisk behandling. Kronisk kortikosteroidbehandling kan störa barns tillväxt och utveckling.
biverkningar
följande lokala biverkningar rapporteras sällan med topikala kortikosteroider, men kan förekomma oftare vid användning av ocklusiva förband. Dessa reaktioner listas i en ungefärlig minskande ordning för förekomst:
| Burning | Perioral dermatitis |
| Itching | Allergic contact dermatitis |
| Irritation | Maceration of the skin |
| Dryness | Secondary infection |
| Folliculitis | Skin atrophy |
| Hypertrichosis | Striae |
| Acneiform eruptions | Miliaria |
| Hypopigmentation |
Overdosage
Topically applied corticosteroids can be absorbed in sufficient amounts to produce systemic effects (see PRECAUTIONS).
Lidex dosering och administrering
Lidex salva appliceras vanligtvis på det drabbade området som en tunn film från två till fyra gånger dagligen beroende på svårighetsgraden av tillståndet.
ocklusiva förband kan användas för hantering av psoriasis eller motstridiga tillstånd.
om en infektion utvecklas ska användningen av ocklusiva förband avbrytas och lämplig antimikrobiell behandling påbörjas.
hur levereras Lidex
lidex Aci (fluocinonid) salva 0.05% levereras i
15 g rör –NDC 99207-514-13
30 g rör-NDC 99207-514-14
60 g rör –NDC 99207-514-17
120 g rör –NDC 99207-514-22
förvaras i rumstemperatur. Undvik temperatur över 30 kg c (86 kg f).
USA: s Patent nr 4,017,615
tillverkad för:
MEDICIS, dermatologiföretaget Xiaomi
Scottsdale, AZ 85258
av: Patheon, Inc.
Mississauga, Ontario
Canada L5N 7K9
IN-5070/S
| Lidex fluocinonide ointment |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Labeler – MEDICIS
Frequently asked questions
- Is it used for hair loss?
- What is a substitute for fluocinonide cream?
- Is fluocinonide an antifungal cream?
- How long should you use fluocinonide for?
- What is fluocinonide cream good for?
- kan fluocinonid användas för att behandla ett gift murgröna utslag?
- är det en steroid?
- är detta ett antibiotikum?
mer om Lidex (fluocinonid topisk)
- biverkningar
- under graviditet eller amning
- doseringsinformation
- läkemedelsinteraktioner
- 8 recensioner
- Generisk tillgänglighet
- läkemedelsklass: aktuella steroider
Konsumentresurser
- avancerad läsning
- Lidex Mild (avancerad läsning)
- Lidex regelbunden (avancerad läsning)
professionella resurser
- förskrivning av information
- Lidex topikal lösning (FDA)
- Lidex Gel (FDA)
andra märken Vanos, lidex-e
relaterade Behandlingsguider
- atopisk dermatit
- eksem
- dermatit
- psoriasis
medicinsk ansvarsfriskrivning