비디오\(\PageIndex{1}\):에 대한 간략한 소개는 천재의 멘델레예프.
으로 초기 화학자들은 일을 정화하는 광석을 발견하고 더 많은 요소들을 실현하는 다양한 요소의 수를 함께 그룹화하여 그들의 유사한 화학적 행동을 합니다. 이러한 그룹화에는 리튬(Li),나트륨(Na)및 칼륨(K)이 포함됩니다: 이 요소들은 모두 반짝이며 열과 전기를 잘 전도하며 비슷한 화학적 성질을 가지고 있습니다. 두 번째 그룹 포함 칼슘(Ca),스트론튬(Sr),바륨(Ba),이는 또한은 빛나는,좋은 지휘자 열과 전기의,그리고 화학 물질의 속성에서 일반적입니다. 그러나이 두 그룹의 특정 속성은 특히 서로 다릅니다. 예:Li,Na 및 K 는 Ca,Sr 및 Ba 보다 훨씬 반응성이 있습니다.; Li,Na,K 양식을 가진 화합물에 있는 산소의 비율은 두 그들의 원자를 하나의 산소 원자는 반면,캘리포니아,Sr,그리고 바 형태로 화합물의 원자를 하나의 산소 원자입니다. 불소(F),염소(Cl),브롬(Br),and iodine(I)또한 전시와 유사한 속성을,하지만 이러한 특성은 크게 다른 사람들의 모든 요소이다.
러시아의 Dimitri Mendeleev(1869)와 독일의 Lothar Meyer(1870)는 그 당시 알려진 원소의 특성들 사이에주기적인 관계가 있음을 독립적으로 인식했다. 둘 다 원자 질량 증가에 따라 배열 된 요소로 테이블을 게시했습니다. 그러나 멘델레예프에 갔다 한 단계 더 이상 마이어:는 그 사용의 테이블의 존재를 예측하는 요소가와 유사한 속성을 알루미늄과 실리콘이었지만,아직 알 수 없습니다. 갈륨(1875)과 게르마늄(1886)의 발견은 멘델레예프의 작업에 큰 지원을 제공했습니다. 지만 멘델레예프 및 마이어 긴 논쟁을 통해 우선순위,멘델레예프의의 발전에 기여를 주기적으로 테이블은 지금 더 널리 인정(그림\(\PageIndex{1}\)).
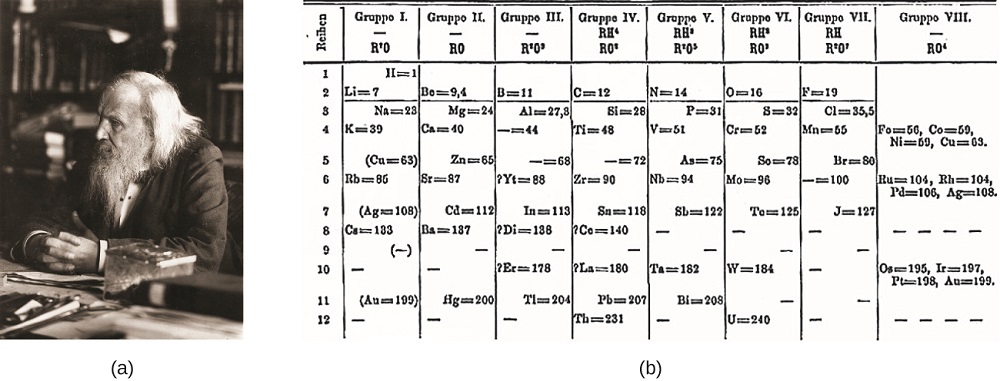
비디오\(\PageIndex{2}\):을 소개하의 조직에 주기적으로 테이블 기간 및 그룹입니다. 이 조직은 우리가 화학의 원리를 계속 구축함에 따라 중요 할 것입니다.
20 세기까지 주기적 관계가 원자 질량보다는 원자 번호를 포함한다는 것이 명백 해졌다. 이 관계의 현대 진술,주기적 법칙은 다음과 같습니다:원소의 속성은 원자 번호의주기적인 함수입니다. 현대기 테이블에 배열의 요소가 증가하기 위해 그들의 원자 숫자와 그룹이 원자와 유사한 속성이 동일한 수직 열(그림\(\PageIndex{2}\)). 각 상자는 원소를 나타내며 원자 번호,기호,평균 원자 질량 및(때로는)이름을 포함합니다. 요소는 마침표 또는 계열이라고하는 7 개의 수평 행과 그룹이라고하는 18 개의 수직 열로 배열됩니다. 그룹은 각 열의 맨 위에 레이블이 지정됩니다. 미국에서는 전통적으로 레이블이 대문자가있는 숫자였습니다. 그러나 IUPAC 은 1 에서 18 까지의 숫자를 사용할 것을 권장하며 이러한 레이블이 더 일반적입니다. 테이블이 단일 페이지에 맞추기 위해 행 중 두 부분(총 14 열)이 일반적으로 테이블의 주 본문 아래에 작성됩니다.

그림\(\PageIndex{2}\):주기율표의 원소는 속성에 따라 구성됩니다.
많은 원소는 화학적 및 물리적 특성이 크게 다르지만 일부 원소는 그 행동과 유사합니다. 예를 들어,많은 요소가 나타나 반짝이는 전성(수 있 변형을 깨지 않고)그리고 연성이 있는(그릴 수 있으로 와이어)를 실시하고 열과 전기습니다. 다른 요소는 반짝이거나 가단성이 없거나 연성이 없으며 열과 전기의 불량 도체입니다. 우리는 정렬할 수 있는 요소로 대 클래스 일반적인 속성:금속(있는 요소를 반짝이,전성,좋은 지휘자 열과 전기의 그늘진 노란색);비금속(요소로 나타나는 둔하고,가난한 지휘자를 열과 전기의 그늘진 녹색); 와 비금속(요소를 수행하는 열과 전기 알맞게 잘하고 몇 가지의 특성을 금속이 어떤 특성의 비금속색 자주색).
는 요소 또한 분류될 수 있으로 주요 그룹소(또는 대리인의 요소)열에 표시된 1,2,13-18;전이금속에서 열 표시 3-12;과 내 전이금속에서 두 개의 행이 맨 아래에서 테이블의(최고 행 요소라고 합 란탄 족과 바닥열 요소는 악티늄;그림\(\PageIndex{3}\)). 원소는 그들이 형성하는 화합물의 조성과 같은보다 구체적인 특성에 의해 더 세분화 될 수 있습니다. 예를 들어 요소로 그룹 1(첫 번째 열)형태는 화합물의 구성 중 하나는 원자의 요소 및 하나의 원자의 수소이다. 이들 원소(수소 제외)는 알칼리 금속으로 알려져 있으며 모두 유사한 화학적 성질을 가지고 있습니다. 의 요소가 그룹 2(두 번째 열)형태는 화합물로 구성된 하나의 아톰의 요소를 두고 원자들의 수소:이라는 알칼리성 지구금속,와 유사한 속성의 구성원들 사이에서는 그룹이다. 다른 그룹으로 특정 이름 pnictogens(그룹 15),chalcogens(그룹 16),할로겐(그룹 17),그리고 고귀한 가스(그룹 18,또한 알려져 있으로 불활성 가스). 그룹 참조할 수도 있습으로 첫 번째 요소는 그룹의:예를 들어,chalcogens 이라고 할 수 있습 산소 그룹 또는 가족의 산소. 수소는 그룹 1 및 그룹 17 요소 모두와 유사한 특성을 가진 고유 한 비금속 원소입니다. 그 이유 때문에 수소는 두 그룹의 맨 위에 표시되거나 그 자체로 표시 될 수 있습니다.
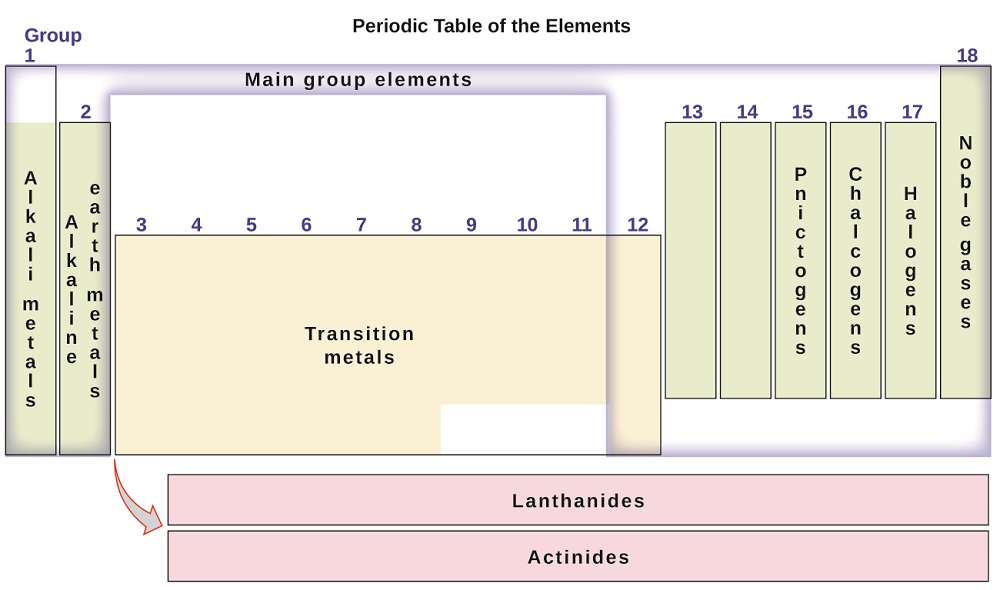
그림\(\PageIndex{3}\):주기율표는 유사한 특성을 가진 원소를 그룹으로 구성합니다.
예\(\PageIndex{1}\):이름 그룹의 요소
원자가 다음의 각각의 요소는 생명이 필수적입니다. 다음 요소의 그룹 이름을 지정하십시오:
- chlorine
- calcium
- sodium
- sulfur
Solution
The family names are as follows:
- halogen
- alkaline earth metal
- alkali metal
- chalcogen
Exercise \(\PageIndex{1}\)
Give the group name for each of the following elements:
- 크립톤
- 셀레늄
- 바륨
- 리튬
대답
고귀한 가스가
대답 b
chalcogen
대답 c
알칼리성 지구금속
대답 d
알칼리 금속
에서 공부를 주기적으로 테이블 당신은 것을 발견 할 수도 있습에 대한 원자 대중의 일부 요소입니다. 원소 43(테크네튬),원소 61(프로메튬),원자번호 84(폴로늄)이상의 원소들은 대부분 원자 질량이 대괄호 안에 주어진다. 이에 대해 수행하는 요소로 구성 불안정한,방사성 동위 원소는(당신이 더 많은 것을 배우에 대한 방사성 핵화학 장). 평균 원자 무게 결정될 수 없을 위한 이러한 요소 때문에 그들의 radioisotopes 크게 달라질 수 있습니다에서 상대적 풍요에 따라 소스,또는 자체가 존재하지 않습니다. 대괄호 안의 숫자는 해당 원소의 가장 안정한 동위 원소의 원자 질량 수(및 대략적인 원자 질량)입니다.
요약
비디오\(\PageIndex{3}\):의 요약을 발견하고 속성을 정기적이다.
의 발견 주기의 재발 유사한 속성 요소 가운데 주도하는 제제의 주기율표하는 요소를 배치하기 위해서는 증가의 원자수에서 행로 알려진 기간 및 열로 알려진 그룹이 있습니다. 주기율표의 동일한 그룹에있는 원소는 비슷한 화학적 성질을 가지고 있습니다. 원소는 금속,메탈로이드 및 비금속으로 분류되거나 주 그룹 원소,전이 금속 및 내부 전이 금속으로 분류 될 수 있습니다. 그룹은 왼쪽에서 오른쪽으로 1-18 번호가 매겨집니다. 의 요소가 그룹 1 으로 알려져 있 알칼리금속;이들 그룹에서 2 는 알칼리성 지구금속;그 15 는 pnictogens;그들에 16 는 chalcogens;그 17 는 할로겐;및 그 18 은 고귀한 가스가 발생합니다.