이온 결합이란 무엇입니까?
화학 결합은 결합 된 원자의 총 에너지가 분리 된 원자의 총 에너지보다 낮을 때 형성됩니다.결합이 취하는 형태는 에너지를 최소화하는 전자 배열에 의해 결정됩니다.
어떤 경우에는 전자가 원자 사이에서 공유됩니다-이것은 공유 결합이라고합니다.
다른 경우,한 원자로부터 다른 원자로의 하나 이상의 전자의 완전한 전달이있다.전자를 잃는 원자는 양전하를 띤 이온이됩니다.전자를받는 원자는 음전하를 띤 이온이됩니다.
이것은 이오니아 접합-호 정전기 매력의 긍정 및 부정적인 요금입니다.가장 순수한 형태에서,이온 결합되지 않은 방향. 그것은 포인트 요금 사이의 단순한 쿨롱 매력으로 간주 될 수 있습니다.이것은 전자의 공유가 방향 결합을 초래하는 공유 결합과는 다르다.
전자 전송
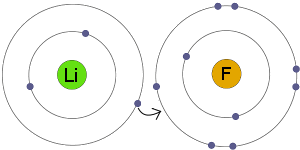
리튬 전송 전자기 F. 결과는 모두 이온의 결과로가기고,안정적인 전자 껍질입니다.
정전기 매력
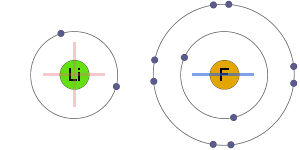
긍정적이고 부정적인 이온전기 매력을 한 다른 결과로,이온 본드입니다.
쿨롱군은 기본 방향과 결과는 이오니아의 화합물을하는 경향이 존재하는 거대한 결정 격자 구조물의 이온을 포 함께.
의 샘플을 리튬 불화물의 결정 격자

전기 음성과 이온 접착
두 가지 요소하는 경향이 채권 상태면에서는 다릅 전기 음성.
Electronegativity 의 주기율표
녹색의 그늘이 가벼울수록 electronegativity 가 높아진다. 회색은 값이 알려지지 않았 음을 의미합니다. (더 크게 보려면 이미지를 클릭하십시오.)

공유 접합 문자
절대적으로 순수한 상태의 결합합물지 않는 진정으로 존재하기 때문에 긍정적으로 부과 이온 극화합니다 부정적인 이온의 전자니다.이것이 특히 눈에 띄는 다룰 때는 작은,높은 금속이온 등 Al3+있지만,극화 효과가 존재하는 어느 정도에서 모든 이오니아합니다.분극은 효과적으로 방향성,전자 공유 효과이므로 이온 성 화합물에서 소량의 공유 결합을 도입합니다.
의 비율은 이오니아/공유 행위에 결합할 수 있습이 매우 거칠게 평가를 사용하여 규모의 폴링의 전기 음성.리누스 폴링(Linus Pauling)은 원소 간 1.7 의 전자 음성 차이가 이온 성 50%인 결합을 유도한다고 추정했다.
1 이하의 값은 공유 결합 지배에 해당하고 2 이상의 값은 이온 결합 지배에 해당합니다.
Electronegativity of Selected Elements (Pauling Scale)
| Element | Electronegativity |
|---|---|
| hydrogen | 2.20 |
| lithium | 0.98 |
| sodium | 0.93 |
| aluminum | 1.61 |
| carbon | 2.55 |
| oxygen | 3.44 |
| chlorine | 3.16 |
| iodine | 2.66 |
C-H 채권의 차이와 0.35 것이 공유하는 동안,NaCl 접합에서 2.23 될 것입니다 이오니아입니다.0.96 에서의 HCl 결합은 극성 공유 결합이 될 것이고,1.68 에서의 LiI 결합은 50/50 이온/공유 결합이 될 것이다.
세슘(0.79)과 불소(3.98)사이의 가장 큰 전자 음성 차이는 3.19 입니다. 결과적인 결합은 특성상 약 95%의 이온 성이다.
