또한 수소의 탄소-탄소 이중 결합이라는 수소첨가. 이러한 첨가의 전반적인 효과는 이중 결합 작용기의 환원성 제거이다. Regioselectivity 는 동일한 그룹(수소 원자)이 이중 결합 탄소 각각에 결합되어 있기 때문에 문제가되지 않습니다. 가장 간단한 원천의 두 개의 수소 원자 분자가 수소(H2),그러나 혼합 알켄으로 수소 발생하지 않습 식별할 수 있는 반응이다. 전반적인 수소화 반응은 발열 성이지만,높은 활성화 에너지는 정상적인 조건에서 일어나는 것을 방지합니다. 이러한 제한은 하기 도면에 도시된 바와 같이 촉매의 사용에 의해 회피될 수 있다.
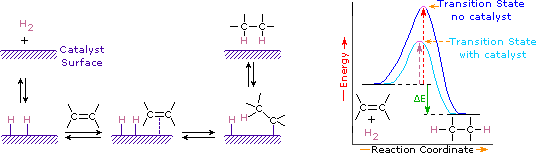
촉매 있는 물질의 변화 속도(속도)화학반응의없이 소비되거나 나나의 일부로 제품입니다. 촉매는 반응의 활성화 에너지를 낮춤으로써 작용하지만 반응물 및 생성물의 상대적 포텐셜 에너지를 변화시키지 않습니다. 백금,팔라듐 및 니켈과 같은 미세하게 분할 된 금속은 가장 널리 사용되는 수소화 촉매 중 하나입니다. 촉매 수소화는 다이어그램에 묘사 된 바와 같이 적어도 두 단계로 일어난다. 첫째,알켄은 수소의 일부와 함께 촉매의 표면에 흡착되어야한다. 다음 두 가지 요소에서 근무 금속 표면에 탄소 이중 결합의 결과 포화 탄화수소,더 약하게 흡착,잎 촉매 표면입니다. 마지막 사건의 정확한 성격과 타이밍은 잘 이해되지 않습니다.
과 같이 다이어그램 에너지,수소첨가의 외은 발열 및 열을 발표에 해당하는 ΔE(녹색)어 있습니다. 이 열의 반응을 평가하는 데 사용할 수 있습의 열역학적 안정성의 외각 다른 숫자의 알킬 치환기 이중 채권. 예를 들어,다음 표를 가열 수소첨가의 세 C5H10 외주는 동일한 알케인 제품(2-가.눈에 들어갔). 반응의 큰 열은 고 에너지 반응물을 나타 내기 때문에,이들 가열은 알켄 이성질체의 안정성에 반비례한다. 대략적인 근사치로,우리는 이중 결합상의 각 알킬 치환기가이 작용기를 1 킬로 칼로리/몰보다 조금 더 안정화시키는 것을 알 수있다.
| 알켄 이성체 | (CH3)2CHCH=CH2 3-메틸-1-butene |
CH2=C(CH3)CH2CH3 2-메틸-1-butene |
(CH3)2C=CHCH3 2-메틸-2-부텐 |
|---|---|---|---|
| 열의 반응 (ΔHº) |
-30.3kcal/몰 | -28.5kcal/몰 | -26.9kcal/몰 |
에서 메커니즘은 다음과 같은 여기 우리가 기대하는 것 수소의 추가 발생할 syn-stereoselectivity 를. 이것은 사실이지만,수소첨가 촉매제를 일으킬 수도 있습니다 수중 결합의 전에 수소 또,어떤 경우에 stereoselectivity 를될 수 있습 불확실하다.
성의 전이금속 복합체 외되었 설득력있게 설명하의 격리 안정적인 플래티넘 단지 등과 같은 Zeise 의 소금,K.H2O 및 ethylenebis(트리페닐포스핀)백금,2Pt(H2C=CH2). 후자에서 백금은 3 좌표 및 0 원이지만 Zeise 의 소금은 백금(II)의 유도체입니다. Zeise 의 소금 모델과 그러한 복합체에서의 특이한 결합에 대한 논의는 여기를 클릭하여 볼 수 있습니다. 알켄 수소화를위한 촉매로도 작용하는 금속 인 니켈 및 팔라듐에 대해서도 유사한 착물이보고되었다.
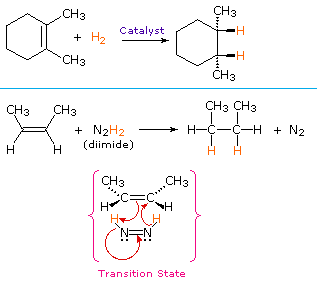
수소의 syn 첨가를 위한 비 촉매 절차는 불안정한 화합물 diimide,N2H2 의 사용을 만듭니다. 이 시약해야 갓에서 생성된 반응 시스템에 의해 일반적으로 산화 히드라진,그리고 강력하게 발열반응에 의해 선호하의 제거 질소 가스(매우 안정적인 화합물). 디이 미드는 시스-트랜스 이성질체로서 존재할 수있다;시스-이성질체 만이 환원제 역할을한다. 두 절차 모두에 의한 알켄 감소의 예가 아래에 나와 있습니다.
참가자
- 윌리엄 Reusch,명예 교수(미시간 주립 미국), 가상의 교과서 유기화학