학습 목표
이 섹션에서,당신은 당신을 할 수 있습니다:
- 검사 열전달.
- 열 전달에서 최종 온도를 계산합니다.
지금까지 우리는 열전달로 인한 온도 변화에 대해 논의했습니다. 얼음이 녹아서 액체 상태의 물이되면(즉,상 변화 중에)열 전달로 인한 온도 변화가 발생하지 않습니다. 예를 들어,태양에 의해 데워진 지붕에서 녹는 고드름에서 물줄기가 떨어지는 것을 생각해보십시오. 반대로 물은보다 낮은 온도의 주변으로 냉각 된 얼음 트레이에서 얼어 붙습니다.

그림 1. 공기에서 나오는 열은 얼음으로 옮겨져 녹아 내립니다. (신용:브랜드 마이크)
에너지가 필요 녹아 단단하기 때문에 점착력이 있는 채권 사이에 있는 분자는 단단해 분열되는 등에서,액체,분자 이동할 수 있는 주변에서 비교 운동 에너지; 따라서 온도 상승은 없습니다. 마찬가지로,에너지하는 데 필요한 기체화 액체,분자 때문에 액체가 서로 상호 작용을 통해 매력적인 힘입니다. 위상 변화가 완료 될 때까지 온도 변화가 없습니다. 처음에는 0ºc 에서 소다 한 컵의 온도는 모든 얼음이 녹을 때까지 0ºC 에 머물러 있습니다. 반대로,에너지는 일반적으로 열 에너지의 형태로 동결 및 응축 중에 방출됩니다. 작업은 분자가 함께 모일 때 응집력에 의해 수행됩니다. 해당 에너지는 그림 2 를 함께 머물 수 있도록(소산)떨어져 주어야합니다.
관련된 에너지에서 단계 변화에 따라 두 가지 주요 요소수의 강도와 회원이 변경된 약관에 동의 힘은 쌍이다. 결합의 수는 분자의 수에 비례하므로 샘플의 질량에 비례합니다. 힘의 강도는 분자의 유형에 달려있다. 열 Q 을 변경하는 데 필요한 단계 샘플의 질량 m 에 의해 주어집
Q=mLf(melting/freezing,
Q=mLv(기화/응축),
어디 잠열의 융합,Lf,과 잠재 증발열,Lv,는 소재 상수은 실험적으로 결정. (표 1)을 참조하십시오.

그림 2 로 표시됩니다. (a)에너지는 액체를 형성하기 위해 고체 내의 분자 사이의 매력적인 힘을 부분적으로 극복하는 데 필요합니다. 그 같은 에너지는 동결이 일어나기 위해 제거되어야합니다. (b)분자는 액체에서 증기로 갈 때 먼 거리로 분리되어 분자 매력을 극복하기 위해 상당한 에너지가 필요합니다. 응축이 일어나기 위해서는 동일한 에너지를 제거해야합니다. 위상 변화가 완료 될 때까지 온도 변화가 없습니다.
잠열은 J/kg 단위로 측정됩니다. Lf 와 Lv 는 모두 물질에 의존하며,특히 앞서 언급 한 바와 같이 분자력의 강도에 달려있다. Lf 와 Lv 는 총칭하여 잠열 계수라고합니다. 그들은 잠재,또는 숨기 때문에,단계에서 변경,에너지가 들어가거나 나이 없는 시스템을 일으키는 온도 변경 시스템에서,그래서,효과,에너지가 숨겨져 있습니다. 표 1 은 용융 및 끓는점과 함께 Lf 및 Lv 의 대표 값을 나열합니다.
표는 상 변화에 상당한 양의 에너지가 관련되어 있음을 보여줍니다. 우리가 보이는,예를 들어,에서 얼마나 많은 에너지 필요한 녹아의 킬로그램에서는 얼음 0ºC 을 생산하는 킬로그램의 물 0°C 에서 사용하는 방정식에 대한 온도 변화 및 대한 값은 물에서 표 1,우리는 Q=mLf=(1.0kg)(334kJ/kg)=334kJ 는 1 킬로그램의 얼음을 녹이는 에너지입니다. 이것은 1kg 의 액체 물 온도를 0ºC 에서 79.8ºC 로 올리는 데 필요한 것과 동일한 양의 에너지를 나타 내기 때문에 많은 에너지입니다. 더 많은 에너지 필요한 증발 물,그것을 걸 2256kJ 을 변경하는 1kg 액체의 물에서 정상적인 끓는점(100ºC 대기압에서)에 증기(물 vapor). 이 예는 위상 변화가없는 온도 변화와 관련된 에너지에 비해 위상 변화에 대한 에너지가 엄청나다는 것을 보여줍니다.
| Table 1. Heats of Fusion and Vaporization | ||||||
|---|---|---|---|---|---|---|
| Lf | Lv | |||||
| Substance | Melting point (ºC) | kJ/kg | kcal/kg | Boiling point (°C) | kJ/kg | kcal/kg |
| Helium | −269.7 | 5.23 | 1.25 | −268.9 | 20.9 | 4.99 |
| Hydrogen | −259.3 | 58.6 | 14.0 | −252.9 | 452 | 108 |
| Nitrogen | −210.0 | 25.5 | 6.09 | −195.8 | 201 | 48.0 |
| Oxygen | −218.8 | 13.8 | 3.30 | −183.0 | 213 | 50.9 |
| Ethanol | −114 | 104 | 24.9 | 78.3 | 854 | 204 |
| Ammonia | −75 | 108 | −33.4 | 1370 | 327 | |
| Mercury | −38.9 | 11.8 | 2.82 | 357 | 272 | 65.0 |
| Water | 0.00 | 334 | 79.8 | 100.0 | 2256 | 539 |
| Sulfur | 119 | 38.1 | 9.10 | 444.6 | 326 | 77.9 |
| Lead | 327 | 24.5 | 5.85 | 1750 | 871 | 208 |
| Antimony | 631 | 165 | 39.4 | 1440 | 561 | 134 |
| Aluminum | 660 | 380 | 90 | 2450 | 11400 | 2720 |
| Silver | 961 | 88.3 | 21.1 | 2193 | 2336 | 558 |
| Gold | 1063 | 64.5 | 15.4 | 2660 | 1578 | 377 |
| Copper | 1083 | 134 | 32.0 | 2595 | 5069 | 1211 |
| Uranium | 1133 | 84 | 20 | 3900 | 1900 | 454 |
| Tungsten | 3410 | 184 | 44 | 5900 | 4810 | 1150 |
Phase changes can have a tremendous stabilizing effect even on temperatures that are not near the melting and boiling points, because evaporation and condensation (conversion of a gas into a liquid state) occur even at temperatures below the boiling point. 예를 들어,사실에는 공기의 온도 기후에서 거의 위 35.0ºC,는 때문에 대부분의 열 전달로 증발 물니다. 마찬가지로,온도 습한 날씨가 거의 아래로 떨어지는 이슬점 때문에 엄청난 열에 출시할 때 물은 수증기 응축.
우리는−20ºC(그림 3)에서 얼음 샘플에 열을 가하는 것을 고려하여 위상 변화의 영향을보다 정확하게 조사합니다. 얼음의 온도는 선형 적으로 상승하여 0ºc 에 도달 할 때까지 0.50cal/g ºC ºC 의 일정한 속도로 열을 흡수합니다. 일단이 온도에서 얼음은 모든 얼음이 녹을 때까지 녹기 시작하여 79.8cal/g 의 열을 흡수합니다. 온도는 이 단계 변화 도중 0ºC 에 일정하게 남아 있습니다. 모든 얼음이 녹 으면 액체 물 온도가 상승하여 1.00cal/g⋅ºC 의 새로운 일정한 속도로 열을 흡수합니다. 100ºC 에서 물이 끓기 시작하고 물이이 상 변화 동안 물 539cal/g 의 열을 흡수하는 동안 온도가 다시 일정하게 유지됩니다. 모든 액체가 증기 증기가되면 온도가 다시 상승하여 0.482cal/g⋅ºC 의 속도로 열을 흡수합니다.
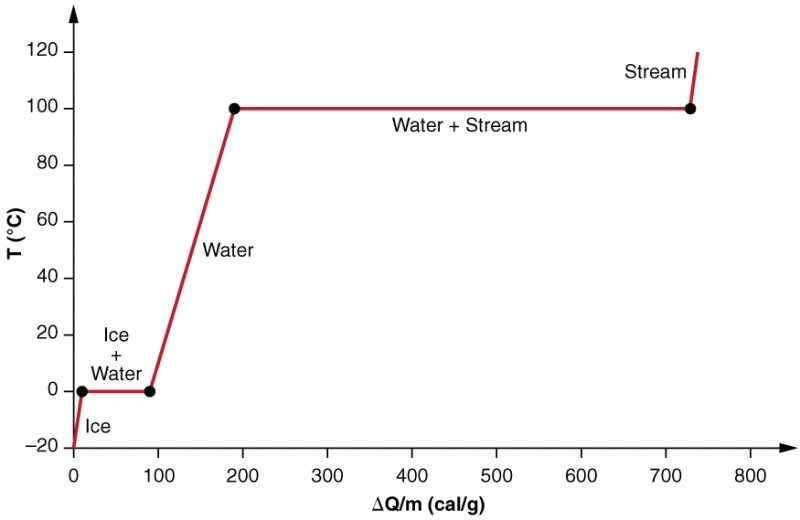
그림 3. 온도 대 에너지의 그래프가 추가되었습니다. 시스템에 구성되지 않도록 수증기 증발하면서 얼음을 따뜻하게 되 액체 물,그리고 그 때 증발이 발생하는 수증기에 남아 있습니다. 0ºC 와 100ºC 에서 일정한 온도 값의 긴 뻗기는 각각 용융 및 기화의 큰 잠열을 반영합니다.
물 끓는점 이하의 온도에서 증발 할 수있다. 더 많은 에너지가 필요한 이상에서 끓는점이기 때문에,운동 에너지의 물 분자는 아래의 온도에서 100ºC 보다 작은 것에서 100ºC,따라서 더 적은 에너지에서 사용할 수 있는 임의의 열 움직임. 예를 들어,사,체온에 땀에서 피부를 필요로 열 입력의 2428kJ/kg,는 약 10%이상 높은 잠열은 증발기에 100ºC. 이 열은 피부에서 나오므로 더운 날씨에 효과적인 냉각 메커니즘을 제공합니다. 습도가 높으면 증발을 억제하여 체온이 상승하여 눈썹에 땀을 흘리지 않게됩니다.
실시예 1. 계산 최종 온도에서 단계 변화:냉각 소다 얼음 조각
세 가지 아이스 큐브 사용하여 진정에서 음 20ºC 질량 msoda=0.25kg. 얼음은 0ºC 고 각각의 아이스 큐브의 질량을 가지고 있 6.0g. 정 소다가 유지에서 거품도록 컨테이너 열 손실을 무시할 수 있습니다. 소다가 물처럼 열용량이 같다고 가정합니다. 모든 얼음이 녹을 때 최종 온도를 찾으십시오.
전략
얼음 조각은 0ºc 의 녹는 온도에 있습니다. 열은 녹기 위해 소다에서 얼음으로 옮겨집니다. 녹는 얼음 발생합니다 두 가지 단계:최초의 단계 변화가 발생합 및 솔리드(아이스)는 액체로 물에서 녹는 온도,다음의 온도 이 물은 상승한다. 융해 수익률은 물에 0ºC,그래서 더 많은 열이에서 전송되는 소다 이 물을 때까지 물 플러스 소다 시스템에 도달하면 열평형,Qice=−Qsoda.
얼음으로 전달 된 열은
Qice=마우스 Lf+micecW(Tf−0ºC)입니다.
소다에 의해 주어진 열은 Qsoda=msodacW(Tf-20ºC)입니다. 열이 손실되지 않기 때문에 Qice=−Qsoda,그래서
마우스 Lf+micecW(Tf−0ºC)=–msodacW(Tf−20ºC).
왼쪽의 Tf 와 오른쪽의 다른 모든 용어와 관련된 모든 용어를 가져옵니다. 알 수없는 수량 Tf 에 대한 해결:
\displaystyle{T}_{\text{f}}=\frac{m_{\text{soda}}c_{\text{W}}\left(20^{\circ}\text{C}\right)-m_{\text{ice}}L_{\text{f}}}{\left(m_{\text{soda}}+m_{\text{ice}}\right)c_{\text{W}}}\\
솔루션
- 식별을 알 수 있습니다. 얼음 질량은 마우스=3×6.0g=0.018kg 이고 소다의 질량은 msoda=0.25kg 입니다.
- 계산 측면에서 분자:m sodacW(20ºC)=(0.25kg)(4186J/kg⋅ºC)(20ºC)=20,930J 및 miceLf=(0.018kg)(334,000J/kg)=6012J.
- 산 분모:(msoda+쥐)cW=(0.25kg+0 입니다.018kg)(4186K/(kg ºC ºC)=1122J/ºC.
- 계산 최종 온도:\displaystyle{T}_{\text{f}}=\frac{20,930\text{J}-6012\text{J}}{1122\text{J/}^{\circ}\text{C}}=13^{\circ}\text{C}\\
토론
이 예제는 엄청난 에너지를하는 동안 관련된 위상을 변경합니다. 얼음의 질량은 물 질량의 약 7%이지만 소다의 온도에 눈에 띄는 변화를 가져옵니다. 우리는 얼음이 얼어 붙은 온도에 있다고 가정했지만,이것은 잘못된 것입니다:전형적인 온도는-6ºC 입니다. 그러나이 보정은 우리가 발견 한 결과와 본질적으로 동일한 최종 온도를 제공합니다. 이유를 설명해 주시겠습니까?

그림 4. 아이스 티 한 잔에 응축. (credit:Jenny Downing)
우리는 기화가 주변에서 액체로의 열전달을 필요로하므로 주변에서 에너지가 방출된다는 것을 보았습니다. 응축은 주변의 온도를 증가시키는 역 과정입니다. 예를 들어 그림의 유리 인 차가운 물체와 응축을 연관시키기 때문에이 증가는 놀라운 것처럼 보일 수 있습니다. 그러나 증기가 응축되도록 응축 분자에서 에너지를 제거해야합니다. 에너지는 액체에서 증기로 다른 방향으로 상 변화를 만드는 데 필요한 것과 정확히 동일하므로 Q=mLv 로 계산할 수 있습니다.
응축은 인근 공기의 온도가 이슬점 이하로 감소하기 때문에 그림 4 에서 형성됩니다. 물 물.공기는 상온에서했던 것처럼 많은 물을 보유 할 수 없으므로 물이 응축됩니다. 에너지가 물 응축 할 때 방출되어 유리에서 얼음이 녹는 속도가 빨라집니다.
실제 응용
액체가 얼면 에너지도 방출됩니다. 이 현상은 온도가 어는점(0ºC)에 가까울 때 오렌지를 보호하기 위해 플로리다의 과일 재배자가 사용합니다. 재배자는 과수원의 식물에 물을 뿌려 물기가 얼어 붙어 열이 물 위에서 자라는 오렌지에게 방출되도록합니다. 이렇게하면 오렌지 내부의 온도가 결빙 아래로 떨어지지 않아 과일이 손상됩니다.

그림 14.11. 에 얼음 이러한 나무 발표 많은 양의 에너지 때 얼어붙지 못하도록 방지하의 온도는 나무에서 떨어지는 0ºC. 딱딱한 서리를 막기 위해 과수원에 물 을 의도적으로 뿌립니다. (신용:Hermann Hammer)
승화는 고체에서 증기 상으로의 전환입니다. 눈이 액체 물 흔적도없이 얇은 공기로 사라지거나 냉동실에서 얼음 조각이 사라지는 것을 눈치 챘을 것입니다. 그 반대는 또한 사실입니다:서리는 액체 단계를 거치지 않고 매우 차가운 창문에 형성 될 수 있습니다. 인기있는 효과는 고체 이산화탄소 인 드라이 아이스에서”연기”를 만드는 것입니다. 승화는 고체의 평형 증기압이 0 이 아니기 때문에 발생합니다. 특정 공기 청정제는 고체의 승화를 사용하여 향수를 실내로 주입합니다. 나방 공간 독성의 예 페놀(유기 화합물)를화하는 동안,몇 가지 고체,같은 오스뮴 명단에서도 독성이 그들에 보관 밀폐된 용기를 방지하는 인간의 노출의 승화-생산한 정보를 제공합니다.

그림 5. 고체와 증기 사이의 직접적인 전환은 일반적이며 때로는 유용하고 심지어 아름답습니다. (a)드라이아이스는 이산화탄소 가스로 직접 승화시킨다. 눈에 보이는 증기는 물 방울로 만들어집니다. (credit:Windell Oskay)(b)Frost 는 매우 차가운 창문에 패턴을 형성하며,증기로부터 직접 형성된 고체의 예입니다. (credit:Liz West)
모든 상전이는 열을 포함합니다. 의 경우 직접적인 솔리드-증기 전환에 필요한 에너지에 의해 주어진 식 Q=mLs,는 Ls 는 열의 승화,이는 에너지를 필요한 변경 1.고체상에서 증기 상까지의 물질. Ls 는 Lf 및 Lv 와 유사하며 그 값은 물질에 따라 다릅니다. 승화는 에너지 입력을 필요로하므로 드라이 아이스가 효과적인 냉각수 인 반면 역 공정(즉,설탕 프로 스팅)은 에너지를 방출합니다. 승화에 필요한 에너지의 양은 다른 상전이의 크기와 동일한 크기 순서입니다.
제시된 자료로서 이 섹션은 이전 섹션할 수 있습을 계산하는 어떤 숫자의 효과 관련된 온도 및 위상 변경합니다. 각각의 경우에 어떤 온도와 위상 변화가 일어나고 있는지 파악한 다음 적절한 방정식을 적용해야합니다. 열전달과 작업으로 인해 온도와 상 변화가 모두 발생할 수 있음을 명심하십시오.
문제 해결 전략의 효과에 대한 열전달
- 을 검사하는 상황이 존재하는 지를 확인할 수 있는 변경에서 온도 또는 단계입니다. 시스템 내부 또는 외부로의 열 전달이 있습니까? 면의 존재 여부는 위상 변경되지 않은 명백하실 수 있습니다 첫 번째 문제를 해결하기 위해 있는 경우에 없었 단계 변화를 검사합 온도 변경을 얻을 수있다. 는 경우 그것은 충분하나 당신을 데려 갈 끓는 또 녹는점,당신이해야 한 다음 다시 가고 문제에서 단계 온도 변경,단계 변화,이후에는 온도 변화 및입니다.
- 온도와 위상이 변하는 모든 물체를 식별하고 나열합니다.
- 문제에서 결정해야 할 것을 정확히 식별하십시오(미지수를 식별하십시오). 서면 목록이 유용합니다.
- 주어진 것 또는 명시된 바와 같이 문제에서 추론 할 수있는 것의 목록을 작성하십시오(knowns 식별).
- 결정될 수량에 대한 적절한 방정식을 푸십시오(알 수 없음). 이 있는 경우는 온도 변경,전송되는 열에 따라 특정 열(표 1 참조 온도 변화와 발열량)반면,단계에 대한 변경,전송되는 열에 따라 잠열. 표 1 을 참조하십시오.
- 는 단위와 함께 knowns 를 적절한 방정식으로 대체하고 단위로 완성 된 수치 솔루션을 얻습니다. 프로세스에 두 개 이상의 단계(예:온도 변화 다음에 위상 변화)가있는 경우 단계로이 작업을 수행해야합니다.
- 그것이 합리적인지 확인하기 위해 답을 확인하십시오:그것은 의미가 있습니까? 예를 들어,온도 변화도 고려하지 않은 위상 변화를 일으키지 않는다는 것을 확신하십시오.
의 이해를 확인하
왜 눈에 남아 있는 산 중턱을 때에도 주간 온도보다 더 높은 냉동 온도?
용액
눈은 얼음 결정으로부터 형성되며 따라서 물 고체 상이다. 상 변화에 막대한 열이 필요하기 때문에 공기가 0ºC 이상이더라도이 열이 공기에서 축적되기까지는 일정 시간이 걸립니다. 공기가 따뜻할수록이 열 교환이 더 빨리 일어나고 눈이 더 빨리 녹습니다.
섹션 요약
- 대부분의 물질은 고체,액체 및 가스 형태로 존재할 수 있으며”단계.”
- 단계 변화에 발생한 고정 온도는 특정 물질에서는 주어진압,그리고 이 온도가라고 끓는 동결(또는 융해)포인트입니다.
- 상 변화 동안,흡수되거나 방출 된 열은 다음에 의해 주어진다:Q=mL 여기서 L 은 잠열 계수이다.
개념적 질문
- 열전달은 온도와 위상 변화를 일으킬 수 있습니다. 그 밖의 무엇이 이러한 변화를 일으킬 수 있습니까?
- 어떻게 잠열의 융합의 물을 감소는 공기의 온도,아마을 방지하는 온도에서 떨어지는 크게 ºC,근처에서 큰체의 물?
- 얼어 붙은 물에 의해 형성된 직후의 얼음의 온도는 얼어 붙는 물입니까?
- 당신이 격리된 콘테이너에 있는 ºC 물으로 ºC 얼음을 두는 경우에,무슨 일이 일어날 것입니까? 어떤 얼음이 녹을 것인가,더 많은 물들이 얼어 붙을 것인가,아니면 둘 다 일어나지 않을 것인가?
- 얼음 물 한 잔에 응축이 얼음이 녹는 속도에 어떤 영향을 줍니까? 응축이 용융 과정을 가속화하거나 속도를 늦출 것입니까?
- 플로리다에서와 같이 수많은 물체가 존재하는 매우 습한 기후에서는 온도가 약 35ºC(95ºF)이상으로 상승하는 것이 특이합니다. 그러나 사막에서는 기온이 이것보다 훨씬 높아질 수 있습니다. 물 증발이 습한 기후에서 고온을 제한하는 데 어떻게 도움이되는지 설명하십시오.
- 겨울에는 내륙 150km 근처의 새크라멘토보다 샌프란시스코에서 종종 더 따뜻합니다. 여름에는 새크라멘토에서 거의 항상 더 뜨겁습니다. 샌프란시스코를 둘러싼 물 시체가 극한의 온도를 어떻게 조절하는지 설명하십시오.
- 끓는 냄비에 뚜껑을 넣으면 끓는 상태를 유지하는 데 필요한 열 전달이 크게 줄어 듭니다. 이유를 설명하십시오.
- 동결 건조 식품은 진공 상태에서 탈수되었다. 이 과정에서 음식은 얼고 탈수를 촉진하기 위해 가열해야합니다. 진공이 탈수 속도를 높이는 방법과 그 결과로 음식이 얼어 붙는 이유를 모두 설명하십시오.
- 야간에 방사하여 여전히 공기가 냉각되면 온도가 이슬점 아래로 떨어지는 것은 드문 일입니다. 이유를 설명하십시오.
- 물리학 교실 데모에서 강사는 풍선을 입으로 팽창시킨 다음 액체 질소로 냉각시킵니다. 추울 때,수축 된 풍선은 그 안에 소량의 밝은 파란색 액체뿐만 아니라 일부 눈 같은 결정을 가지고 있습니다. 그것이 따뜻해지면 액체가 끓고 결정의 일부가 승화되어 일부 결정이 잠시 동안 남아 액체를 생성합니다. 차가운 풍선에서 파란색 액체와 두 개의 고체를 식별하십시오. 표 1 의 데이터를 사용하여 신원을 정당화하십시오.
문제를&연습
- 얼마나 많은 열전달(에서의 칼로리를 소모)이 필요하 녹 0.450-kg 패키지의 냉동 야채에서 원래 0ºC 는 경우 그들의 열의 융합 같은 것의 물?
- 0ºC 얼음이 들어있는 가방은 같은 양의 0ºC 물을 함유 한 물보다 에너지를 흡수하는 데 훨씬 효과적입니다. (a)0.800KG 의 물 온도를 0ºC 에서 30.0ºC 로 올리려면 얼마나 많은 열전달이 필요합니까? (b)먼저 녹이기 위해 얼마나 많은 열전달이 필요한지 0.800kg 의 0ºc 얼음을 넣은 다음 온도를 올리시겠습니까? (c)당신의 대답이 얼음이 더 효과적이라는 경합을 어떻게지지하는지 설명하십시오.
- (a)얼마나 많은 열 전송이 필요하의 온도를 높이는 0.750-kg 알루미늄을 함유 냄비 2.50kg 의 물 30.0ºC 을 끓는점과 끓인 다음 멀리 0.750kg 의 물? (b)열전달율이 500W1watt=1joule/second(1W=1J/s)인 경우 얼마나 걸립니까?
- 얼음 물 한 잔에 응축이 형성되면 얼음이 그렇지 않은 것보다 빨리 녹습니다. 8 인 경우.물 200g 을 모두 함유 한 유리에 00g 의 응축이 형성되며,그 결과 얼음이 몇 그램 녹을 것입니까? 다른 열전달이 발생하지 않는다고 가정합니다.
- 여행에서 3.50kg 의 얼음 봉지가 쿨러에서 평균 하루 동안 지속된다는 것을 알 수 있습니다. 은 무엇인 평균 전원 포트에 들어가는 얼음 시작하면서 0ºC 및 완전히 녹을 0ºC 물에서 정확히 어느 날 1watt=1joule/second(1W=1J/s)?
- 특정 건조한 화창한 날에,수영장의 온도는 증발을 위해 만약에 아닙니다 1.50ºC 에 의하여 상승할 것입니다. 온도를 일정하게 유지하기에 충분한 에너지를 정확하게 운반하기 위해 물 중 어떤 부분이 증발해야합니까?
- (a)얼마나 많은 열 전달시키는 데 필요한 온도의 0.200-kg 얼음조각에서 -20.0ºC 을 130ºC 포함하여 필요한 에너지 위상 변화는? (b)일정한 20.0kJ/s 의 열전달 속도를 가정 할 때 각 단계에 얼마나 많은 시간이 필요합니까? (c)이 프로세스에 대한 온도 대 시간의 그래프를 만듭니다.
- 1986 년 거대한 빙산이 남극 대륙의 로스 빙붕에서 벗어났습니다. 그것은 대략 160km 길이의 40 직사각형이었습니다.폭이 0km 이고 두께가 250m 입니다. (a)얼음의 밀도가 917kg/m3 임을 감안할 때이 빙산의 질량은 얼마입니까? (b)그것을 녹이기 위해 얼마나 많은 열 전달(줄에서)이 필요합니까? (c)얼음이 하루에 평균 100W/m2,12.00h 를 흡수한다면 얼음이 두꺼운 얼음을 녹이기 위해 혼자 햇빛을 몇 년이 걸릴까요?
- 커피를 95.0ºC 에서 45.0ºC 로 식히기 위해 100-g 유리 컵에 350g 의 커피에서 몇 그램의 커피가 증발해야합니까? 커피가 물 과 동일한 열 특성을 가지고 있으며 기화의 평균 열이 2340kJ/kg(560cal/g)이라고 가정 할 수 있습니다. (커피가 냉각되면서 질량의 변화를 소홀히 할 수 있으며,이는 올바른 것보다 약간 큰 답을 줄 것입니다.)
- (a)그것을 어렵게 소화에 있는 원유 유조선,기 때문에 각각 리터의 원유 릴리스 2.80×107J 에너지의 경우 타. 이것을 설명하기 위해 어려움의 수를 계산 리터의 물해야 하는 소비하는 에너지를 흡수에 의해 발표 burning1.00L 원유의 경우,물은 온도에서 발생 20.0ºC 을 100ºC,비등하면,그 결과 증기가 발생하 300ºC. (b)원유가 물보다 밀도가 작다는 사실로 인한 추가 합병증에 대해 논의한다.
- 뇌우에서 응축에서 방출되는 에너지는 매우 클 수 있습니다. 반경 1km 의 작은 폭풍에 대해 대기로 방출되는 에너지를 계산하여 1.0cm 의 비가이 지역에 균일하게 침전된다고 가정합니다.
- 서리 손상을 방지하기 위해 4.00KG 의 0ºc 물 을 과일 나무에 뿌립니다. (a)물 얼기로 얼마나 많은 열 전달이 발생합니까? (b)이 양의 열이 나무에서 전달되면 200kg 나무의 온도가 얼마나 감소할까요? 비열을 3.35kJ/kg*ºC 로 가져 가면 위상 변화가 일어나지 않는다고 가정합니다.
- 25.0ºC 에서 0.800kg 의 수프를 담고있는 0.250-kg 알루미늄 그릇을 냉동실에 넣습니다. 377kJ 의 에너지가 그릇과 수프에서 옮겨지면 수프의 열 특성이 물 속성과 동일하다고 가정하면 최종 온도는 얼마입니까?
- -30.0ºC 에 0.0500kg 아이스 큐브는 아주 잘 격리된 콘테이너에 있는 35.0ºC 물 0.400kg 에서 둡니다. 최종 온도는 얼마입니까?
- 0.0100KG 의 20.0ºC 물 을 1.20-KG 얼음 블록(처음에는 -15.0ºC)에 부으면 최종 온도는 얼마입니까? 당신은 물 주변 환경의 영향이 무시할 정도로 빠르게 냉각 가정 할 수있다.
- 원주민들은 때때로 뜨거운 바위를 물에 넣어서 물기가있는 바구니에서 요리하여 끓입니다. 물 0.0250kg 초기 지글 지글에서에서 증기로 탈출 하는 경우 500ºc 바위의 어떤 질량은 100ºc 에 그것의 온도를가지고 15.0ºC 물 4.00kg 에 배치 해야? 당신은 주변 환경의 영향을 소홀히하고 암석의 평균 비열을 화강암의 것으로 가져갈 수 있습니다.
- 것이 무엇 최종 온도의 팬과 물에서 계산 최종을 때 온도를 열 전송 사이의 두 물체:쏟아지는 차가운 물에 뜨거운 팬는 경우 0.260kg 의 물에 배치 된 팬 0.0100kg 의 물은 증발 바로를 떠나 나머지 부분을 일반적인 온도와 팬?
- 일부 국가에서는 액체 질소가 기계식 냉장고 대신 유제품 트럭에 사용됩니다. 에이 3.00 시간 배달 여행에는 200l 의 액체 질소가 필요하며 밀도는 808kg/m3 입니다. (a)이 양의 액체 질소를 증발시키고 온도를 3.00ºC 로 올리는 데 필요한 열 전달을 계산하십시오. (Cp 를 사용하고 온도 범위에서 일정하다고 가정합니다.)이 값은 액체 질소가 공급하는 냉각량입니다. (b)킬로와트-시간 단위의이 열 전달 속도는 얼마입니까? (c)액체 질소를 증발시키는 것과 동일한 질량의 0ºc 얼음을 녹여서 얻은 냉각량을 비교하십시오.
- 일부 총기 애호가는 납 슬러그를 녹여 주조하는 것과 관련된 자체 총알을 만듭니다. 온도를 높이고 25.0ºC 부터 시작하여 0.500kg 의 납을 녹이기 위해 얼마나 많은 열전달이 필요합니까?
용어
열의 승화:에 필요한 에너지 변경에서 물질 단단한 단계를 수증기 단계
잠열 계수:육체적인 일정한 크기의 열 전달을 위한 모든 1kg 물질의 변화하는 동안에서의 위상 물질
승화: 로의 전환에서 단단한 단계를 수증기 단계
선택한 문제에 대한 솔루션을&연습
1. 35.9kcal
3. (a)591kcal;(b)4.94×103s
5. 13.5 와트7. (a)148kcal;(b)0.418s,3.34s,4.19s,22.6s,0.456s
9. 33.0g
10. (a)9.67L;(b)원유는 밀도가 낮보다는 물,그래서 그것의 맨 위에 물으므로 노출에 있는 산소 공기를 사용하는 구울 수 있습니다. 또한,물 오일 아래에 있는 경우,그것은 덜 효율적입니다 오일에 의해 생성 된 열을 흡수.12. (a)319 킬로 칼로리; (b)2.00ºC
14. 20.6ºC
16. 4.38 키로그램
18. (a)1.57×104kcal;(b)18.3kW⋅h;(c)1.29×104kcal
- 값을 인용하에서 정상적인 용융과 끓는 온도에서 표준 대기압(1atm). 삽입
- 에 37.0ºC(몸의 온도),증발열 Lv 에 대한 물은 2430kJ/kg 또는 580kcal/kg 삽입
- 에 37.0ºC(몸의 온도),증발열 Lv 에 대한 물은 2430kJ/kg 또는 580kcal/kg 삽입