소스를 찾을 수 있:”단일 결합”뉴스·신문·책·학자·JSTOR(August2012)(는 방법을 배울 때를 제거하는 이 템플릿의 메시지가)
에서 화학,단일 결합은 화학적 결합 사이에 두 개의 원자를 포함하는 두 개의 원자의 전자. 즉,원자는 결합이 형성되는 한 쌍의 전자를 공유합니다. 따라서 단일 결합은 공유 결합의 한 유형입니다. 공유 할 때,관련된 두 개의 전자 각각은 더 이상 그것이 시작된 궤도의 유일한 소유가 아닙니다. 오히려 두 전자 모두 결합 과정에서 겹치는 궤도 중 하나에서 시간을 보냅니다. 루이스 구조로서,단일 결합은 aːa 또는 a-A 로 표시되며,A 는 원소(무어,Stanitski 및 Jurs329)를 나타낸다. 에서 첫 번째 연출,각 점을 나타내 공용자 일렉트론,그리고 두 번째 연출 줄을 모두 나타냅 전자의 공유에서 단일 결합.

공유 결합은 또한 이중 결합 또는 삼중 결합 일 수있다. 단일 결합은 이중 결합 또는 삼중 결합보다 약합니다. 이 강도에 차이가 될 수 있는 설명을 검사하여 구성 요소 채권의 각각의 이러한 유형의 공유결합으로 구성(Moore,Stanitski 및 Jurs393).일반적으로 단일 결합은 시그마 결합입니다. 예외는 파이 본드 인 diboron 의 결합입니다. 에 대비 이중 결합의 구성 중 하나 sigma 본드 한 파이 채권,그리고 삼중 결합의 구성 중 하나 시그마채와 두 파이 채권(Moore,Stanitski 및 Jurs396). 구성 요소 결합의 수는 강도 차이를 결정하는 것입니다. 그 이유는 하나의 채권이 약한의 세 가지로 구성되어 있기 때문에 단 시그마는 채권 및 이중 채권 또는 트리플 본드 구성하지만 이 유형의 구성 요소를 결합 하지만 적어도 하나의 추가니다.
단일 결합은 회전 능력,이중 결합 또는 삼중 결합에 의해 소유되지 않는 특성을 갖는다. 구조의 파이 채권에 대한 허용하지 않는 회전(적어도에 298K),그래서 그는 이중 결합 및 트리플 채권을 포함하는 파이 채권은 개최으로 인해 이 숙박 시설. 합 시그마 채권지 않도록 제한하며 단일 결합할 수 있를 사용하여 회전합 시그마 채권의 축으로 회전(Moore,Stanitski 및 Jurs396-397).
본드 길이에서 다른 속성 비교를 할 수 있습니다. 단일채는 가장 긴의 세 가지 종류의 공유결합으로 원자 사이의 매력은 큰에서 두 개의 다른 종류,더블,트리플. 이 증가는 구성 요소 채권은 이유는 매력으로 증가 더 전자가 공유 사이의 접착 원자(Moore,Stanitski 및 Jurs343).
단일 결합은 종종 규조토 분자에서 볼 수 있습니다. 단일 결합의 이러한 사용의 예는 H2,F2 및 HCl 을 포함한다.
단일 결합은 또한 두 개 이상의 원자로 구성된 분자에서 볼 수 있습니다. 의 예에는 이의 사용을 하나의 채권을 포함한다:
- 두 채권에 H2O
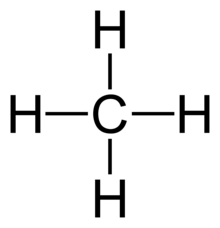
- 모두 4 채권에 CH4
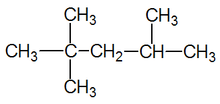
단일 결합에도 나타나에서 분자처럼 복잡 탄화수소보다 더 큰 메탄을 방출하고 있다. 탄화수소에서의 공유 결합의 유형은 이들 분자의 명명법에서 매우 중요하다. 단일 결합만을 함유하는 탄화수소는 알칸(Moore,Stanitski 및 Jurs334)으로 지칭된다. 이 그룹에 속하는 특정 분자의 이름은 접미사-ane 로 끝납니다. 예를 들면 에탄,2-메틸부탄,및 시클로 펜탄(무어,스타니츠키,및 쥬르스 335)이 있다.