反芳香族化合物は異常に不安定です
分子が反芳香族であるかどうかを決定する重要な要因は何ですか?
芳香族性に関する私たちのシリーズの私たちの前の記事では、,我々は芳香族分子が異常に安定していることがわかりました。 それらは特に大きな共鳴エネルギーを有し、付加反応ではなく置換を受ける傾向があり、非局在化pi電子を有する(例えば、ベンゼン中のすべてのC-C結合長は等しい)。
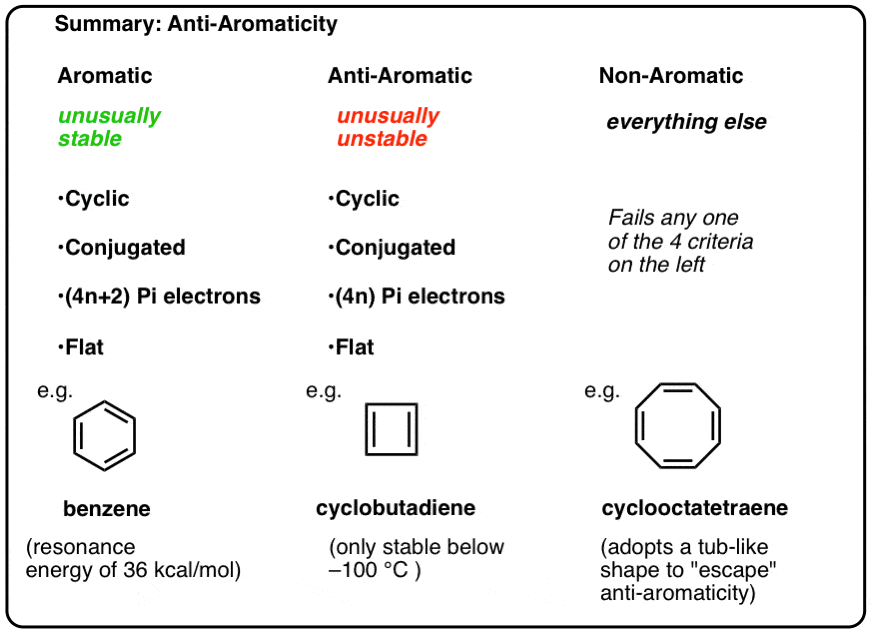
芳香族であるためには、分子は以下の四つの構造特性を有していなければならない:
- 環状
- 環の周りのすべての共役
- pi電子を持っている
- フラット(平面)
これらの四つの条件が満たされている場合、分子は芳香族である。それはテストで一つの質問でさえもflunks場合、それは非芳香族です。
それは芳香族ではありません。
それは芳香族です。それはかなり明確であるようです。
それは非常に明確です。
それともそれですか?あなたは私がこの質問をフレーミングしている方法から、答えは「かなりではない」と推測するかもしれません。
あなたは答えが「かなりではない」と :–)
目次
- いくつかの分子は、彼らが独自のカテゴリに値するように見事かつ異常に不安定で、単離するのは難しいです:反芳香族
- シクロペンタジエニルカチオン:安定ではない”共鳴安定化”カルボカチオン
- 反芳香族三員環:オキシレン、1H-アジレン、チイレン
- シクロブタジエンは反芳香族です
- 反芳香族化合物の8π電子の例: Pentalene
- 何が分子を反芳香族にしますか?
- シクロオクタテトラエンは、平坦性からねじれを介して反芳香族性を”エスケープ”
- 結論:反芳香族化合物
- ノート
- 高度な:参考文献とさらなる読書
1。 カテゴリを形成する著しく不安定な分子:”反芳香族”
ここに事があります。 非芳香族だけでなく芳香族性試験を失敗させた少数の分子があります: 彼らは、彼らが別の名前に値することを非常に見事に、異常に不安定で隔離するのが難しいという性質を持っています。私たちはこれらの分子を”反芳香族”と呼んでいます。
興味深いのは、多くの場合、分子自体がcubaneとは対照的に、第一原理からは特に不安定には見えないということです。
興味深いのは、分子自体が第一原理からは特に不安定には見えないということです。 面白いことに、aldrichからcubane(多かれ少なかれ)を購入することができますが、以下で説明する抗芳香族分子のほとんどは、極端に低い温度でのみ安定してい
2. シクロペンタジエニルカチオン: 安定していない”共鳴安定化”カルボカチオン
のは、最初の学期の有機化学からおなじみのように見えるはずです簡単な例でウサギの穴の下に私た
SN1反応を覚えていますか?
最初に快適な椅子を離れる猫?
クイックレビュー:ハロゲン化アルキルから始めます。 グループの葉を残し、カルボカチオンを形成する。 求核剤攻撃。 これは、律速段階(カルボカチオン形成)が単分子であるため、SN1と呼ばれています。 ボトムライン:より安定したカルボカチオン、より速く反応が進行します。 したがって、ハロゲン化アルキルの反応速度は三次>>一次であり、共鳴によって安定化されればカルボカチオンは特別なボーナスポイントを得る。これら二つのSN1反応を見てください。
二次カルボカチオン(A)を通過するSN1反応、または二次カルボカチオンを通過し、複数の共鳴形態(B)を形成することができるSN1反応-あなたはどちらあなたがこれまでに学んだことすべてから、あなたは答えがBであることを期待するでしょう)。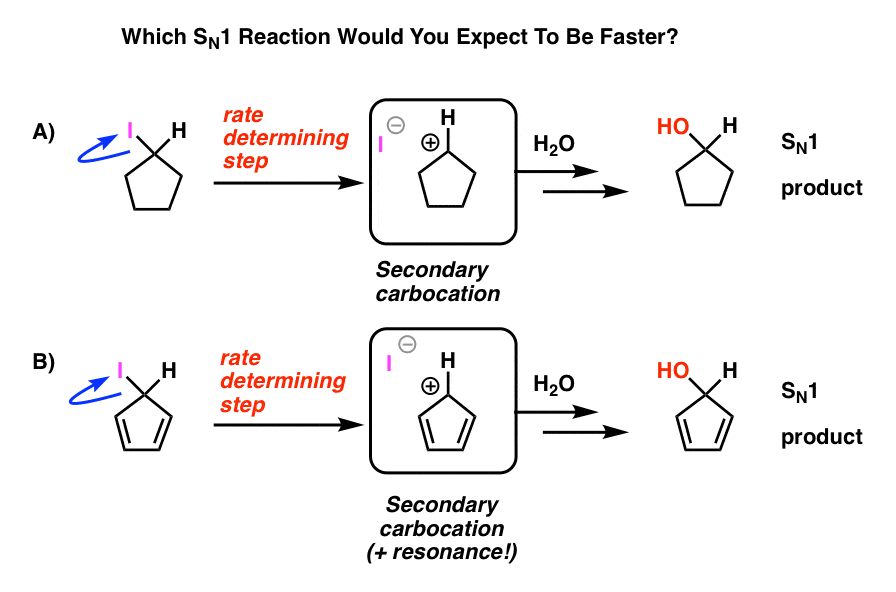
それはありません。答えは、反応A)がより速く起こるということです。
答えは、反応A)がより速く起こるということです。 反応Bは全く起こらない。 これは深く奇妙なあなたを打つ必要があります。
それは!
それは!
それは! このおそらく共鳴安定化カルボカチオンが二次カルボカチオンよりも安定ではないのはなぜですか?
結局のところ、共鳴が分子、特にカルボカチオンを安定化させるのはあなたの頭の中に何回穿孔されていますか?しかし、ここでは、不安定化しているようです。
それは…それは…

しかし、不安定です! シクロペンタジエニルカチオンは信じられないほど不安定で作るのが難しいです–そしてそれは試みることの欠如のためではありません。 それに異常な不安定性を与えるシクロペンタジエニルカチオンの構造について非常に奇妙な何かがあります。

環状、共役、フラット…. π電子が4個あります 面白い!
3. 反芳香族三員環:オキシレン、1H-アジレン、チイレン
“とらえどころのない”分子の別のクラスは、三員環のファミリーです。 あなたはそれがm-CPBAのような酸化剤を使用してアルケンからエポキシドを作るのは簡単だことをOrg1から思い出すかもしれません。なぜアルキンに対して同じ反応をカバーしなかったのか疑問に思ったことはありますか?
まあ、それはしようとしていないためではありません。
化学者はアルキンをエポキシ化するためのあらゆる種類の方法を試しましたが、あなたは何を知っていますか? 反応はうまくいかない例えば、アセチレンのエポキシ化は、以下の分子(オキシレン)を与えるであろう。
例えば、アセチレンのエポキシ化は、以下の分子(オキシレン)を与えるであろう。
オキシレン自体は観察されていないが、そのつかの間の存在の食欲をそそる痕跡がある。 ところで、どちらも窒素類似体、1H-アジレン、またはチイレンを持っていません。 p>
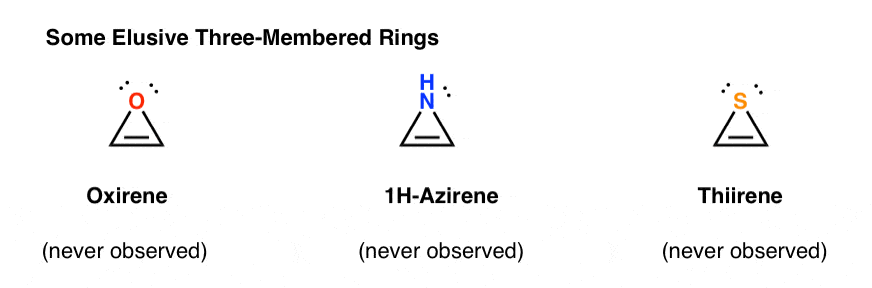
なぜですか? これらのケースのそれぞれについて何が特別ですか?あなたは、シクロペンタジエニルカチオンのように、これらの分子は環状、共役、平坦であり、4つのπ電子(π結合に2つ、孤立対から2つ)を有することに気
OKです。 他に何が環状で、共役で、平らで、4つのπ電子を持つかもしれませんか?
4. シクロブタジエンは反芳香族である
シクロブタジエンは十分に単純な分子のように見えますが、実際には1965年まで合成されませんでした。 それでも、35ケルビン以上の温度では安定していないことが判明しました。
問題は、なぜですか?

確かに、それは四員環だし、はい、それは環ひずみの多くを持っていますが、また、上記の例のように、シクロブタジエンは、環状で共役し、4つのπ電子を有し、平坦である分子の別の例であることに注意するかもしれません。
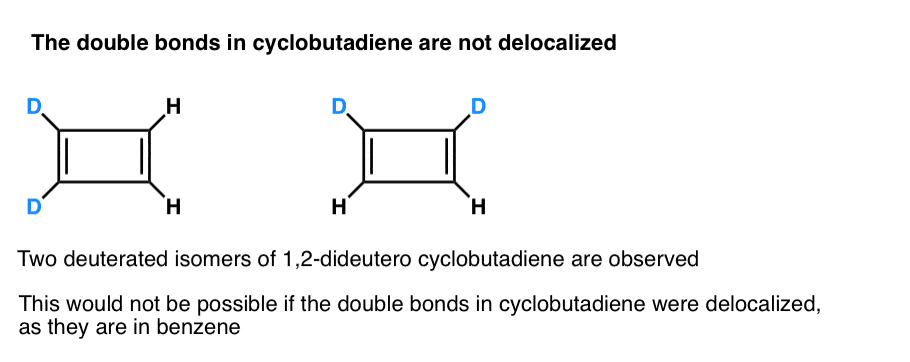
さらに興味深いのは、シクロブタジエンの幾何学について学んだことです。 シクロブタジエンはベンゼンのような同一の結合長を持つ分子ではなく、長方形の形をしており、電子が非局在化していないことを示している。
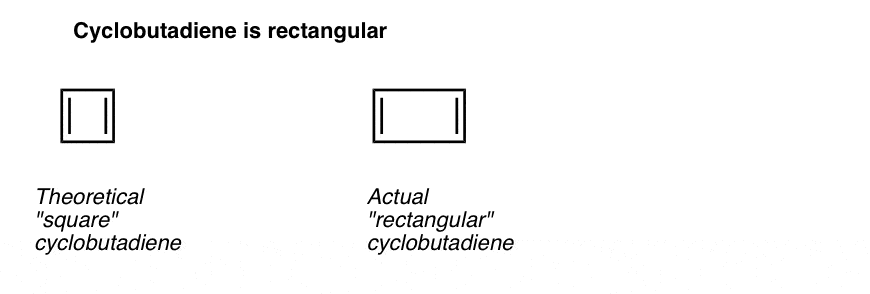
これは、分子がすべての条件(環状、共役、平らな、4π電子)を満たしていても、対称幾何学的形状は特に不安定であるということを教えてくれます。 . 非常に興味深い!
反芳香族化合物の8Π電子の例:ペンタレン
これまでのところ、これまでに見たすべての例は4π電子を持っていました。 あなたは疑問に思うかもしれません:4つ以上のπ電子を持つ反芳香族分子の例はありますか? なぜ、はい。以下の分子は”ペンタレン”と呼ばれています。
それは総合されましたが、-100°C.の下でだけ安定していますこの温度の上のそれはそれ自身(参照)の別の分子と結合します。 壮大な不安定性の別の例。p>

ペンタレンは8π電子を持っています。 これは、認識のいくつかの警鐘をオフに設定可能性があります。 芳香族分子中のπ電子の数がどのようにシーケンスに従ったかを覚えておいてください(2, 6, 10, 14….) ?
この例は、反芳香族分子中のpi電子の数が次のシーケンスに従うことを示唆しています。
この例では、(4, 8, 12…)
分子を反芳香族にするのは何ですか?だから、この悪党のギャラリーのこれらの分子のすべてが共通しているのは何ですか?
それらのそれぞれは、環状、共役、および平坦であり、pi電子の数を数えると、それは4の倍数です。
それらのそれぞれは、環状、共役、および平 したがって、芳香族分子は(4n+2)π電子を有するが、反芳香族分子の「規則」は(4n)である。 (それを見る別の方法:pi電子の数は偶数の2倍になります)。
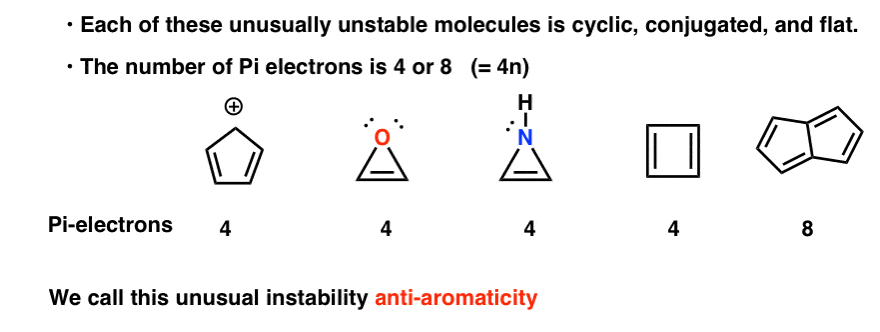
この異常な不安定性は、”反芳香族性”と呼ばれています。
これは、次の基準に従って分子の三つのカテゴリを描くことができることを意味します。
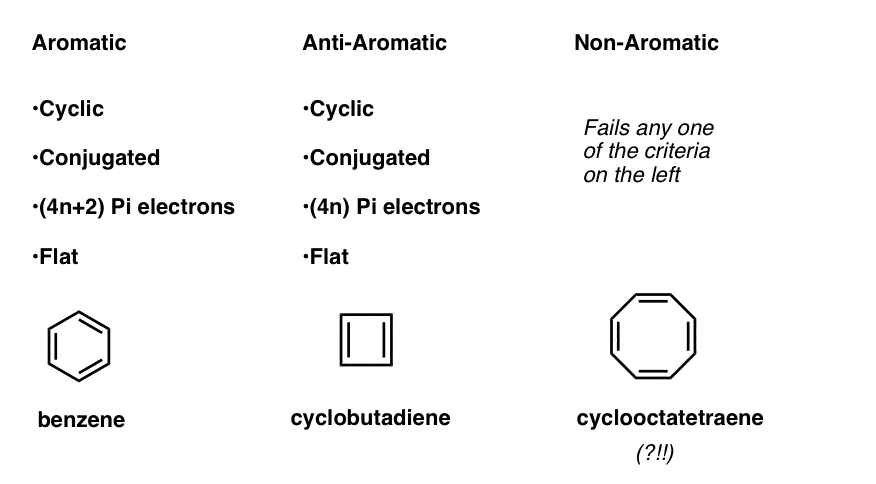
- 芳香族分子は環状であり、共役しており、(4n+2)pi電子を有し、平坦である。
- 反芳香族分子は環状であり、共役であり、(4n)π電子を有し、平坦である。
- 反芳香族分子は環状であり、共役である。
- 非芳香族分子は、これらの条件のいずれかに失敗する他のすべての分子です。なぜシクロオクタテトラエンが”非芳香族”に分類されているのか疑問に思うかもしれません。 8π電子(偶数の2倍)では、それは「反芳香族」ではありませんか?
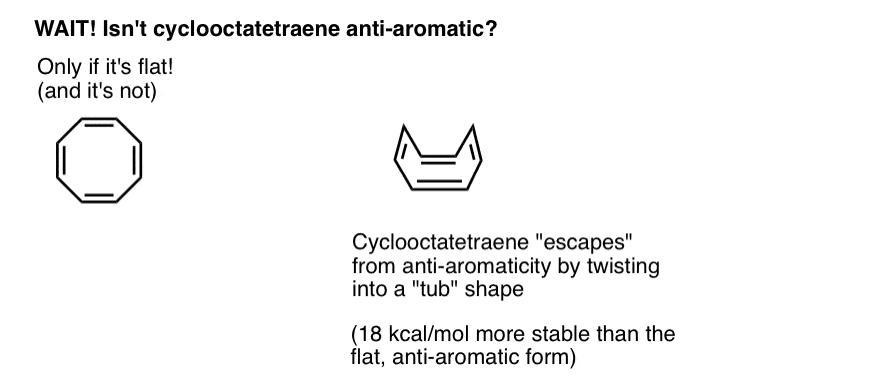
シクロオクタテトラエンは、平坦性からねじれを介して反芳香族性を”逃げる”
“反芳香族性”の条件を満たすことを、非常に罰する所得税の予選のようなものと考えてください。 税金から抜け出すための抜け穴を見つける機会を考えると、あなたはそれをしますか? たぶん
シクロオクタテトラエンは、それが平坦である場合にのみ反芳香族である。 しかし、シクロオクタテトラエンの比較的”フロッピー”構造は、いくつかの柔軟性を可能にする。 結合は、分子が”浴槽のような”形状を採用するように平坦性から離れて回転することができ、それによって、分子上のすべてのp軌道が互いに共役していた場合に支払われる18 12kcal/molの”反芳香族性税”を避けることができる。
シクロオクタテトラエンは合成され、安定であり(例えば、ここで購入することができます)、”通常の”アルケンのように振る舞い、付加反応、水素化などを行う。また、8π電子を有するペンタレン(上記)は、平坦性から離れて結合回転を防止する非常に剛性の二環構造を有しています。
ペンタレン(上記)は、 それ故に、それは反芳香の立体配座で付いています。
8π電子を超える分子の反芳香族性は知られていますが、非常に珍しいです。 (ここでは、18pi電子を持つ分子の芳香族性からの別の”脱出”の楽しい例です。結論:反芳香族化合物
これまでのところ、芳香族性および反芳香族性の治療は純粋に説明的かつ経験的であった。 私たちは多くの例を示し、多くのルールを与えましたが、議論から欠けているのは”なぜ”の深い説明でした。それがとても安定になるベンゼン環についてとても特別なのは何ですか?
なぜそれは安定していますか?それはとても不安定になるシクロブタジエン系についてとても特別なものです。
それは非常に不安定になります。
それは非常に不安定 なぜ不安定なのですか?
これらのより深い質問に答えるためには、我々は戻って、これら二つの分子の分子軌道を調べ、その後、芳香族性と反芳香族性のより深い理解に来なければならないとしています。それが次の投稿で行うことです。
この投稿を準備するのに助けてくれたMatthew Knoweに感謝します。
ノート
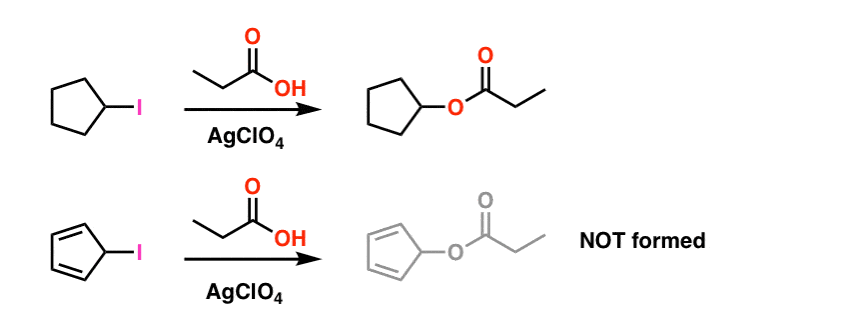
脚注1。 簡単にするために、主な記事に示されている画像は、実際の反応条件にfudges。 実際の実験条件を以下に示す。 溶媒はプロピオン酸であり、ルイス酸の過塩素酸銀はヨウ素を引っ張ることと助けるために加えられます。 .
これらの条件下でさえ、シクロペンタジエニルカルボカチオンは形成されず、これはその極端な不安定性の証である。
脚注2。 エテン(別名エチレン)のエポキシ化は、毎年15万トンのチューニングに行われます。 オキシレンを形成するためのアセチレンのエポキシ化は不明である。
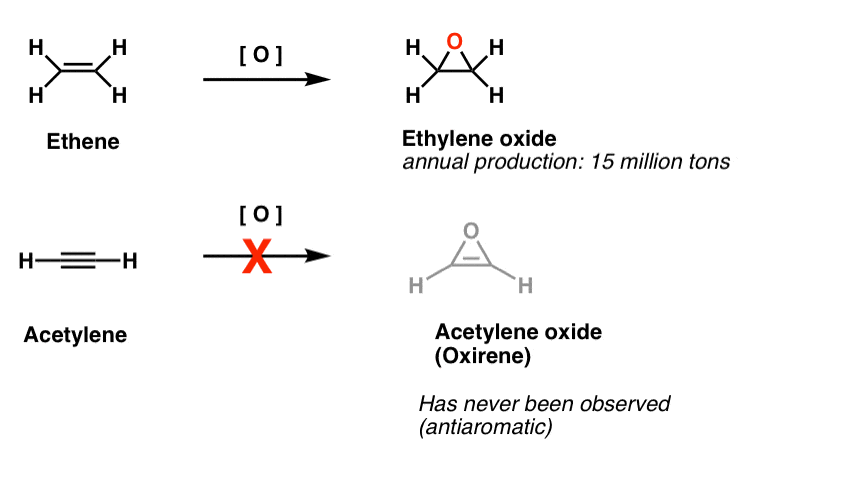
オキシレンの存在のつかの間の証拠が発見され オキシレンはある種のウォルフ転位ではつかの間の中間体であるという同位体標識研究からの良い証拠がある。 また、極端に低い温度で捕捉されたが、35ケルビン以上で分解されたオキシレンの例もある。1H-アジリンのつかの間の存在は、アセチレンにニトレンを添加することで仮定されており、これはすぐに(安定した)2h-アジレンに再配置される(下)。
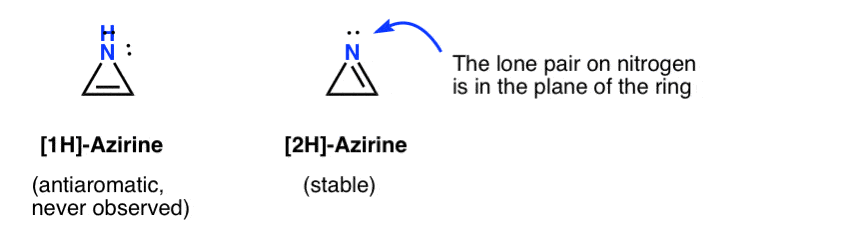
2H-アジレンでは、窒素上の孤立した対はpi系に直角であるため、この系は反芳香族とは対照的に非芳香族であることに注意してください。詳細については、マーチの高度な有機化学を参照してください。
私は第5版、62-63ページを離れて働いていた。
。 脚注3. 非常に巧妙な実験では、1,2-ジデウテロシクロブタジエンには2つの異性体があり、1つではないことが判明した(下記参照)。 シクロブタジエン中の二重結合はベンゼン中のように非局在化していないが,従来のジエン中の二重結合に似ていることを示している。
シクロブタジエンは、ディールス-アルダー反応の例では、35Kでそれ自身と反応して”二量体”を形成する。
脚注4。 はい、アジレンの孤立したペアがsp3ハイブリッド軌道に入れることができるのは事実です(下)。 これはおそらく抗芳香族の”ペナルティ”を幾分減少させるが、分子は依然として信じられないほど不安定である。 反芳香族性はこれを説明する最も簡単な方法です。

脚注5。 長方形の形状は、Jahn-Teller効果として知られている効果によるものです。 電子が同じ量子数を持つことができないパウリ排除原理を覚えていますか? さて、シクロブタジエンの分子軌道図を見るとわかるように、”正方形”シクロブタジエンは二つの”縮退”電子を持っています。 これは、二つの電子のエネルギー準位が区別されるまで結合の伸びが起こる”パウリ反発”として知られる現象につながる。 間違いなく高度なトピック。
(高度な)参考文献とさらなる読み取り
- シクロオクタテトラエンの遷移状態分光法
Paul G.Wenthold、David A.Hrovat、Weston T.Borden、W.C.Lineberger。
科学,1996,272,1456-1459.
土井:10.1126/科学。272.5267.1456
この研究は、シクロオクタテトラエンの非芳香族基底状態が”反芳香族”立体配座よりも12kcal/molであるという声明の基礎である。 - シクロブタジエンの飼いならさ
Donald J.Cram,Martin E.Tanner,Robert Thomas
Chem. Int. エド 1991,30(8),1024-1027
DOI:10.1002/anie.199110241
ノーベル賞受賞者ドナルド-J-クラム教授(UCLA)によるこの論文では、シクロブタジエンの最初の分光学的特徴付けについて説明している。 これはhemicarcerand(おりの複合体)の前駆物質を囲み、次に紫外線とのそれを照射することによって達成され、従って捕獲されるので何もしてないcyclobutadieneを作成します。 - シクロブタジエン
Thomas Bally,Satoru Masamune
Tetrahedron1980,36(3),343-370
DOI:1016/0040-4020(80)87003-7
この論文は、1980年からシクロブタジエンについてそれまでに行われた作業をレビューしている。 これは、実験的な合成努力と理論的計算の2つの部分に分かれています。 - テトラヘドランとシクロブタジエン
Günther Maier
Chem. Int. エド 1988,27(3),309-332
DOI:10.1002/anie.198803093
この論文は、テトラヘドランとシクロブタジエンに対する合成努力をレビューします–両方の分子はC4H4の式を持っています。 置換された(テトラt-ブチルおよびテトラtrimethylsilyl)テトラヘドラーンのみがこれまでに合成され、単離されている。 - シクロブタジエン-およびベンゾシクロブタジエン-鉄トリカルボニル錯体
F.Emerson,L.Watts,and R.Pettit
Journal of The American Chemical Society1965,87(1),131-133
DOI:10.1021/ja01079a032 - シクロブタジエン 新しい芳香族システム
D. Fitzpatrick,L.Watts,G.F.Emerson,and R.Pettit
Journal of the American Chemical Society1965,87(14),3254–3255
DOI:10.1021/ja01092a050
ボーナストピック:シクロブタジエンは金属で安定化することができる-有機金属錯体シクロブタジエン鉄トリカルボニルは安定な結晶性固体である。 著者らが言及しているように、遊離シクロブタジエンが合成中に生成されることはまずない。 - https://www.asu.edu/courses/chm233/notes/aromatic/aromaticRL1/antiaromatic.html
抗精神病薬オランザピンは、シクロオクタテトラエンと同様に、抗芳香効果を避けるために”蝶”の形を採用しています。 これは明らかにその機能にとって重要です。 - 反芳香族性
Ronald Breslow
Accounts of Chemical Research1973,6(12),393-398
DOI:1021/ar50072a001
興味深いことに、Breslow(Columbia)教授は、4n p電子を持つ特に不安定化した環状化合物について、”反芳香族”という用語を最初に提案した人物であると述べている。 また、m.J.S.Dewar教授らの他の研究では、シクロブタジエンの反芳香族不安定化は線形ブタジエンに対して18-33kcal/molの間であると計算されている。 - シクロブタジエンの抗動脈性の実験的決定
Ashok A.Deniz,Kevin S.Peters,Gary J.Snyder
Science1999,286(5442),1119-1122
DOI:1126/science.286.5442.1119
これはシクロブタジエンの反芳香族不安定化を決定するために新しい分光技術を使用して非常に厳密な論文です。 仮想的なひずみのない共役ジエン基準に対して、シクロブタジエンは合計87kcal/mol、32kcal/molは環ひずみに起因し、55kcal/molは反芳香族性に起因する(ベンゼンの芳香族安定化のための21kcal/molと比較して)。 - 非置換シクロペンタジエニルカチオン、基底状態三重項
Saunders,R.Berger,A.Jaffe,J.M.McBride,J.O’Neill,R.Breslow,J.M.Hoffmann,C.Perchonock,E.Wasserman,R.S.Hutton,v.j.Kuck
Journal of the American Chemical Society1973,95(9),3017-3018
土井:101021/ja00790a049
シクロペンタジエニルカチオンは、本稿で説明するように、困難でのみ調製することができる。 それが形成されると、それは三重項電子基底状態(2つの不対電子を有する)を有し、EPR(電子常磁性共鳴)分光法によって特徴付けることができる。 - Oxirenes
Errol G.Lewars
Chemical Reviews1983,83(5),519-534
DOI:10.1021/cr00057a002
- シクロオクタテトラエンの遷移状態分光法