Chemguide:Core Chemistry14-16
二重共有結合と三重共有結合
このページでは、酸素、窒素、二酸化炭素、エテンを例にして、原子間の複数の(二重または三重の)共有結合の可能性を紹介している。 彼らはすべて一般的に14-16歳のための英国のシラバスで指定されているので、これらが選択されています。私はあなたが共有結合を紹介するページを読んで、このサイトからダウンロードできるような周期表にアクセスできると仮定しています。
酸素中の二重結合
周期表で酸素を調べると、原子番号が8であることがわかります-中性原子には8個の陽子と8個の電子があります。 これらは2,6に配置されます。だから、このような二つの原子を持っています:
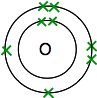
それぞれ二つの不対電子を持っています。 最大のエネルギッシュな安定性を得るためには、これらのすべてをペアにする必要があります。
だから、酸素は電子の二対を共有しています:これは、共有電子のペアを表すために線を使用して見ることがはるかに簡単です:
![]()
窒素中の三重結合
周期表あなたはその電子構造が2,5であることを理解することができます。 それを酸素と比較すると、それはその外側の準位に1対の電子と3つの不対電子を持っています。それを可能な限りエネルギー的に安定にするためには、これらのすべてを共有結合でペアリングする必要があります。
それを可能な限りエネルギー的に安定にするためには、これらすべてを共有結合でペアリングする必要があります したがって、二つの窒素原子は、このように結合します:
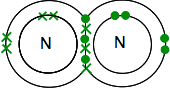
繰り返しますが、これは共有電子のペアを表すために線を使用して見
炭素の電子構造は2,4であり、外側の準位に4つの不対電子がある。
酸素は2,6で、2対の電子と2つの不対電子が外側のレベルにあります。あなたはすべての電子をペアにする必要があります-そしてそれをする唯一の方法があります。
あなたはすべての電子をペアにする必要が
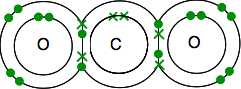
前と同じように、結合は電子のペアを結合するための線を使用して見やすくなります。
2つの原子の間に2つの結合する電子対がある場合、それは驚くことではないが、二重結合と呼ばれます。
![]()
2つの原子の間に2つの結合する電子対がある場合、それは驚くことではないが、二重結合と呼ばれます。 従って各酸素は二重結合によって中間の炭素原子に結合されます。
エテン、C2H4における二重結合
エテンおよび炭素原子間の二重結合を有する他の同様の化合物は、化学において重要な物質 あなたはコースの後半でより詳細にそれらを満たすでしょう。
点と十字の図を注意深く見て、それがどのように一緒に収まるかを理解してください。 炭素と水素の両方のすべての単一の電子が結合対で対になるように、このようにしなければなりません。
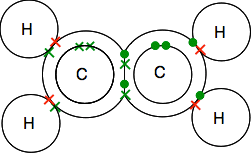
結合ペアを線として示す図に遭遇した場合、2つのバージョンのいずれかを見つけることができます。最初のものは分子の実際の形状をよりよく示していますが、2番目のものもこのレベルでは完全に許容されます。
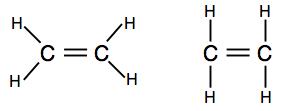
p>
今どこに行きたいですか?共有結合については、このセクションの次のページへ。
共有結合については、このセクションの次のページへ。
. .
原子構造と結合メニューに。 . .
化学14-16メニューに。 . .
Chemguideのメインメニューに。 . .p>