kovalens vegyületek tulajdonságai
amikor szilárd Ionos vegyületekről beszéltünk Ionos vegyületekben, azt találtuk, hogy tulajdonságaik gyakran az ellentétes elektromos töltések erős vonzerejéből származnak. Nem meglepő, ha azt találjuk, hogy a kovalens vegyületek tulajdonságai nagyrészt a kovalens kötések természetének köszönhetők.
az egyik legfontosabb dolog, hogy emlékezzen a kovalens vegyületek, hogy ők nem ionos. Ez nyilvánvalónak tűnik, de a különbség valójában finomabb, mint gondolnád. Ennek a koncepciónak a szemléltetéséhez nézze meg a következő ábrát:
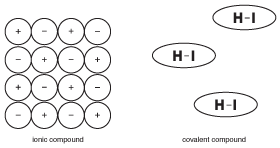
9.5 ábra a szilárd ionos vegyületek tulajdonságai azon a tényen alapulnak, hogy sok iont mereven tartanak a helyén elektromos erőkkel. A kovalens vegyületekben lévő molekulák azonban relatív függetlenséggel működnek a szomszédos molekuláktól.
Ellentétben ionos vegyületek, ahol az ionok egy nagy kristály segít, hogy egymással együtt, a molekulák egy kovalens összetett tulajdonában vannak együtt erők úgynevezett “intermolecular erők”, amely sokkal gyengébb, mint a kémiai kötések (többet intermolecular erők Szilárd anyagok). Ennek eredményeképpen a kovalens vegyület molekulái nem vonzódnak egymáshoz, mint az ionos vegyületek ionjai. Ez a szerkezeti különbség fontos a kovalens vegyületek tulajdonságainak megértésében.
Kovalens Vegyületek Alacsony Olvadáspont Forráspont Pontot
Amint említettük, az Ionos Vegyületek, nagy mennyiségű energia szükséges, hogy olvad egy ionos vegyület, mert az erős kölcsönhatások között a kationok, valamint anionok egy ionos kristály. A kovalens vegyületekben azonban minden molekula csak gyengén kötődik a szomszédos molekulákhoz, ezért nagyon kevés energiát igényel a kovalens molekulák egymástól való elválasztása.
Sok elején kémia a tanulók tévesen úgy vélik, hogy a molekula kovalens elolvad, a kovalens kötés van törve. Ez hamis. Amikor az ionos vegyületek megolvadnak, az ionos vonzerő meghiúsul. Amikor a kovalens vegyületek megolvadnak, a molekulák egyszerűen elhúzódnak egymástól, így a kötések érintetlenek maradnak.
a kovalens vegyületek gyenge vezetők
az Ionvegyületek oldva vagy megolvadva nagy villamosenergia-vezetők. Amint azt az ionos vegyületekben említettük, ez azért van, mert az ionos vegyületek olyan mobil ionokkal rendelkeznek, amelyek képesek az elektromos töltést egyik helyről a másikra átvinni. Nagyon jól vezetik a hőt is, mert az ionok jól vannak egymás mellett, lehetővé téve az energia hatékony átvitelét egyik helyről a másikra.
a kovalens vegyületek viszont szinte mindig jó szigetelők mind a villamos energia, mind a hő szempontjából. A villamos energia nem képes hatékonyan működni kovalens vegyületeken keresztül, mert nincsenek ionok az elektromos töltés mozgatásához. Kiváló példa erre a saját házában, ahol a hosszabbítókábelekben lévő fém műanyaggal van borítva, hogy elkerülje a macska áramütését. A hő szintén nem halad jól a kovalens vegyületeken keresztül, mivel a molekulák nem olyan szorosan kapcsolódnak egymáshoz, mint az ionok egy ionos vegyületben, így a hőátadás kevésbé hatékony. Ezért használja a sütőkesztyűt, hogy vegye ki a cookie-kat a sütőből, ahelyett, hogy sóval bevonná a kezét.
Kovalens Vegyületek Néha Éget
Szerves vegyületek kovalens vegyületek, amelyek szenet tartalmaz. Általában hidrogént is tartalmaznak. tartalmazhat kisebb mennyiségű egyéb elemet, például nitrogént, ként, foszfort, oxigént vagy bármely halogént.
sok kovalens vegyület gyúlékony, és hő hozzáadásával könnyen éget. A gyúlékony kovalens vegyületek fő csoportját szerves vegyületeknek nevezik. A szerves vegyületek azért égnek, mert tartalmaznak szenet és hidrogént, mindkettő jól kombinálódik az oxigénnel magas hőmérsékleten.
fontos szem előtt tartani,hogy nem minden kovalens vegyület ég?például a víz kovalens vegyület, és nagyon nehéz lesz vele tüzet gyújtani. Azonban sokkal több kovalens, mint az ionos vegyületek gyúlékonyak.
a gyúlékonyság a kovalens vegyületek általános tulajdonsága, mivel az ismert kovalens vegyületek nagy része szerves. Mivel a legtöbb szerves vegyület éget, biztonságosan felsorolhatjuk ezt kovalens vegyületek tulajdonságaként, annak ellenére,hogy sok kovalens vegyület van, amelyek nem égnek.
részlet Ian Guch teljes idióta kémiai útmutatójából 2003. Minden jog fenntartva, beleértve a reprodukciós jogot egészben vagy részben bármilyen formában. Által használt megállapodás Alpha Books, tagja Penguin Group (USA) Inc.
ahhoz, hogy ezt a könyvet közvetlenül a kiadótól Rendelje meg, látogasson el a Penguin USA webhelyére, vagy hívja az 1-800-253-6476 telefonszámot. Ezt a könyvet az Amazon-on is megvásárolhatja.com és Barnes & Noble.