A Microbial Biorealm page on the genus Enterococcus faecalis
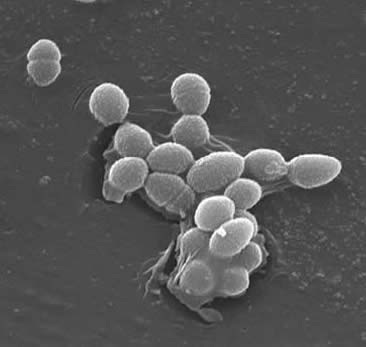
Classification
Higher order taxa
Bacteria; Firmicutes; Bacilli; Lactobacillales; Enterococcaceae; Enterococcus
faj
Enterococcus faecalis
leírás és jelentősége
az enterococcusok olyan Gram-pozitív kókuszdió, amely képes túlélni a kemény körülményeket a természetben. Ezek megtalálhatók a talajban, a vízben és a növényekben. Egyes törzseket élelmiszergyártásban használnak, míg mások súlyos emberi és állati fertőzéseket okoznak (például ismert, hogy kolonizálják az emberek gasztrointesztinális és genitális traktusait). Ezek mind a közösségi, mind a kórházi szerzett fertőzésekkel járnak. Az enterococcusok 10-42°C hőmérsékleten, széles pH-értékű környezetben nőhetnek. Némelyikről ismert, hogy mozgékony. Míg az Enterococcus nemzetségbe több mint 15 faj tartozik, a klinikai izolátumok 80-90% – a E. faecalis (8). Az enterococcusok általában rövid láncokat alkotnak, vagy párban vannak elrendezve. Bizonyos növekedési körülmények között azonban megnyúlnak, cocobacillárisnak tűnnek. Általában az enterococcusok alfa-hemolitikus. Egyesek rendelkeznek a D csoport Lancefield antigénnel, és monoklonális antitest-alapú agglutinációs tesztekkel kimutathatók.Az enterococcusok jellemzően kataláznegatívak, és anaerobak. Képesek 6,5% NaCl-ben növekedni, 40% epesó jelenlétében hidrolizálni az esculint, pirrolidonil-arilamidáz és leucin-arilamidáz pozitív (8). Az enterococcusok számos antimikrobiális gyógyszerrel, “beleértve a sejtfal aktív hatóanyagait; aminoglikozidokkal, penicillinnel és ampicillinnel, valamint vankomicinnel” (1) szembeni rezisztenciájuk miatt bizonyítottan terápiás kihívást jelentenek. Az enterococcusok képesek az antimikrobiális rezisztencia számos tényezőjének megszerzésére, amelyek súlyos problémákat okoznak az Enterococcus fertőzésben szenvedő betegek kezelésében (8). Általánosságban elmondható, hogy a vankomicinre csökkent érzékenységű Enterococcus izolátumok vana, vanB és vankomicin kategóriába sorolhatók. a legnagyobb veszélyt a vanA és a vanB jelenti, mivel ők a legellenállóbbak, és a rezisztenciagéneket plazmidon hordozzák. Mivel a rezisztencia géneket plazmidon hordozzák, könnyen átvihetők, az E. faecalis ezeket a plazmidokat konjugációval (2) átviheti. E. a faecalis ellenáll a teicoplaninnak is. A vankomicin-függő Enterococcus törzseket találtak, de ritkák és kevésbé gyakoriak, mint a vankomicin-rezisztens törzsek (a továbbiakban: “vankomicin-rezisztens enterococcusok” vagy “VRE”) (1).
Genomstruktúra

premissziójával újranyomtatva számos közegészségügyi veszély miatt szükség volt az Enterococcus törzs genomszekvenciájának adataira. A genom DNS-szekvenáláshoz választott törzs az E. faecalis V583 volt, az első vankomicin-rezisztens izolátum az Egyesült Államokban. A V583 törzs genomját a Genomkutatási Intézet (TIGR) szekvenálta. Az Enterococcus Genom azt mutatja, hogy az E. faecalis metabolikusan változatos, számos szabályozási rendszert tartalmaz. A v583 törzs négy DNS-molekulát tartalmaz: a fő 3,218,030 bázispár bakteriális kromoszóma és három kör alakú plazmid. A kromoszóma körülbelül 3500 nyitott olvasási keretet (ORFs) tartalmaz, ezeknek az ORF-eknek körülbelül 1/3-a Nincs hozzárendelhető funkcióval (8). A három plazmid a plazmid-1, plazmid-2 és plazmid-3 néven azonosított körkörös DNS-molekula. A plazmid-1 66,320 bp-t, a plazmid-2 17,963 bp-t, a plazmid-3 pedig 57,660 bp-t tartalmaz. A plazmidok számos gént kódolnak, beleértve a transzpozázokat, a multi-drug rezisztencia fehérjéket és a ppGpp által szabályozott növekedési gátlót (8). Az E. faecalis kromoszóma átlagos G+C összetétele 37,38%. Mivel a DNS-molekula olyan nagy, regionális eltérések fordulnak elő az átlagtól. Az egyik ilyen hely a “vancomycin resistance gene cluster 2, 22 Mb közelében elhelyezett” nagy szegmens, amely a G+C tartalom (8) százalékos növekedését mutatja. Ezek az antibiotikum-rezisztenciával vagy virulenciával kapcsolatos különbségek azt sugallták, hogy a genetikai anyagot egy idegen fajból horizontális átvitel útján szerezték be. Még nem ismert, hogy a transzferek felelősek-e a DNS-smink változásaiért. Az e genomjában található információk. a faecalis V583 nagyban segíti annak megértését, hogy a szervezet hogyan alkalmazkodott egy sokoldalú emberi kórokozóhoz. Az összehasonlító genomika alkalmazásával a különböző szabályozási elemek szerepe jobban megérthető lesz abban, hogy hogyan reagálnak a különböző környezeti stresszekre és a potenciális virulencia faktorok kifejeződésére (8). Több ilyen tanulmány új gyógyszereket javasol az enterococcusok által okozott bakteriális fertőzésekre.A genom 3 Ebp (kódolás az endocarditis biofilmhez kapcsolódó pili) operont is tartalmaz, amelyek fontosak az E. faecalis OG1RF törzs biofilm előállításához. Ez a törzs ezeket az operonokat használja a felszíni pili előállításához. . A surface pili-t “a gazdafelülethez való kötődésre és az endocarditis során emberben antigénre használják” (9).
A TIGR tartalmazza az E. faecalis kromoszómák génjeinek teljes listáját.
Sejtstruktúra és metabolizmus
Sejtmetabolizmus
az enterococcusok kemény környezetben élnek, mint az emberek és állatok bélrendszerei. A növekedés ilyen ellenséges körülmények között megköveteli, hogy az E. faecalis anyagcseréje rugalmas legyen. E. faecalis képesek nem csak, hogy erjedés, hogy készítsen tejsav, hanem “catabolize egy spektrum, az energiaforrások, a szénhidrátok, glicerin, laktát, maláttal, citrát, diamino savak, manya-ezek a savak” (3).Kimutatták, hogy a kijelölt növekedési feltételek E. faecalis növelheti a növekedési keresztül oxidatív foszforiláció segítségével egy proton hajtóerő által létrehozott elektron közlekedés. A “születő légzés következménye az erős oxidálószerek előállítása” (pl. szuperoxid és hidrogén-peroxid), az oxidatív stressz, amit az E. faecalis elvisel (3). Ennek a stressznek a toleranciája, más súlyos növekedési feltételekkel kombinálva, lehetővé teszi az E. faecalis számára, hogy 10-45°C-on, epesókban, rendkívül alacsony és magas pH-n növekedjen. Ezenkívül az E. faecalis ellenállhat azidnak, mosószereknek, nehézfémeknek és etanolnak. Mivel az E. faecalis változatos cukorforrásokat képes felhasználni, változatos környezetben élhet, különösen a bélben, ahol a tápanyagok korlátozottak (2). A bélben az E. faecalis energiájuk nagy részét a nem felszívódott cukrok erjedéséből nyerik. E. a faecalis energiát nyerhet a mucinok lebontásával is, amely egy erősen glikozilált szénhidrát, amelyet a bél serleg sejtjei termelnek (2).Az E. faecalis “foszfoenolipiruvát-foszfotranszferáz-rendszert (PTS) használ a sejten kívüli cukrok érzékelésére, és foszforilációval párosítja a cukrok felvételét” (2). Ennek során kevesebb energiát (ATP) pazarolnak el, mint a cukor felhalmozódását a nem PTS rendszerek. Az E. faecalis által metabolizált cukrok a következők: D-glükóz, D-fruktóz, laktóz, maltóz (minden PTS szubsztrát). Az Enterococcusokban a PTS szabályozza a glicerin metabolizmusát, az induktor kiürülését és a katabolit elnyomását is (8). Az E. faecalis egyike azon kevés alacsony G+C tartalmú Gram-pozitív baktériumoknak, amelyek a glükóz növekedése során kiutasítják a cukrot, ezt a jelenséget induktor kiutasításnak nevezik (8). Az E. faecalis aerob és mikroaerofil körülmények között is képes a glicerint erjeszteni. Az E. faecalis anaerob körülmények között glicerinen is növekedhet, mivel “kifejezi a NAD+-hoz kapcsolódó anaerob glicerin-dehidrogenáz aktivitására szolgáló gént” (8). A glicerin átjuthat a sejtmembránon egy glicerin diffúziós elősegítőnek (GlpF) nevezett fehérje segítségével. A GlpF a glicerin koncentrációját a sejten belül és kívül egyenlővé teszi, a fehérjét glikolízis gátolja. Az E. faecalis extrém lúgos pH-ban és magas sókoncentrációban képes élni. Ezek a tulajdonságok kationszállítást igényelnek, hogy fenntartsák a homeosztázishoz elengedhetetlen állandó citoszolikus ionösszetételt. Minden sejtnek ki kell ürítenie a felesleges nátriumot, hogy a citoszolos koncentrációkat a homeosztázist támogató tartományban tartsa. E. a faecalis kifejezi mind a Na + / H + antiportert, mind a vacuoláris típusú Atpázt (2). A kálium egy fő intracelluláris kation. Az E. faecalis 0,4-0,6 M káliumkoncentrációja elengedhetetlen a normális sejtanyagcseréhez, “semlegesíti az intracelluláris anionokat, aktiválja a különböző enzimeket,és szabályozza a citozol pH-t” (8). Az E. faecalis legalább két káliumszállítót fejez ki a Szabályozás végrehajtásához, a KtrI-t és a KtrII-t, valamint a kep-rendszert a K+ extrudáláshoz (8). Bár ismert, hogy a KtrI és a KtrII k + felvételi rendszerek (ezek K+/H+ szimporterek), a fehérjékről keveset tudunk.
Sejtstruktúra
az enterococcusok Gram-pozitív kókuszok, amelyek általában rövid láncokat alkotnak, vagy párban vannak elrendezve (3). Bizonyos növekedési körülmények között megnyúlhatnak és coccobacillárisnak tűnhetnek. Az E. faecalis sejtfala a szárazsejt tömegének 20-38% – a (Az exponenciális és a helyhez kötött fázissejtekben). Tekintettel arra, hogy az E. faecalis Gram-pozitív baktérium, három fő összetevő alkotja a sejtfalát: peptidoglikán, teichoic sav és poliszacharid. A sejtfal 40%-a peptidoglikán, míg a sejtfal többi része “rhamnóz-tartalmú poliszacharidból és ribitol-tartalmú teikósavból” (3) áll. A peptidioglikán működik (mint a legtöbb Gram-pozitív sejtben), hogy ellenálljon a magas citoplazmatikus ozmotikus nyomás által kiváltott feltörésnek. Az E. faecalis-t általában nem kapszulázott szervezetnek tekintik, amelyet a “kimutatható mucoid fenotípus hiánya” (3) mutat. Az E. faecalis izolátumok alcsoportjai azonban kapszuláris poliszachariddal rendelkeznek. E. a faecalis a genetikai anyagot (plazmidokat) kis peptid feromonok által indukált konjugációs folyamatokkal (2) cserélheti ki. Felületi fehérje “a recipiens sejteken egy adott ligandumot felismerő aggregációs anyagok” biztosítják a konjugáció sikeres kapcsolatait (2).Az E. faecalis képes arra is, hogy felszíni pilit készítsen, ami biofilm kialakulásához vezethet. Az endocarditist okozó E. faecalis törzsek nagy mennyiségben tartalmazzák ezeket a pili-t. A pili lehetővé teszi a fogadó felületekhez (például a szívszövethez) való kötődést. Az E. törzsei. az endocarditist okozó faecalis a “biofilm sokkal gyakrabban és nagyobb mértékben termelődik, mint a nem endocarditis izolátumok” (9).
ökológia
E. a faecalis az enterococcusok nagyon változatos faja. Számos más organizmussal kölcsönhatásba lép, és hatással van a környezetre. Az enterococcusok az emberben a vastagbélben élő bakteriális közösség tagjai. A bélflóra természetes részét képezik a legtöbb más emlős és madár esetében is (8). Az enterococcusok a talajban, a növényekben és a vízben is megtalálhatók. Amikor vízben találják őket, általában azért van, mert a víz szennyezett volt a széklet. Bár az E. faecalis nem jelenik meg túl gyakran a növényekben, a növények között más enterococcusok törzseket is találtak, amelyek valószínűleg szennyezett vízforráshoz vezetnek (8).Az antibiotikum-rezisztencia és a virulencia géntranszfer ökológiája a környezetben még mindig nem tisztázott. A bomló szerves anyagokban kifejlődő rovarok, mint például a háziasítók (HF), antibiotikum-rezisztens baktériumokat juttathatnak az állatok trágyájából és más bomló szerves szubsztrátumokból a lakókörnyezetbe (7). A HF tökéletes transzmitterek, mivel az élő mikrobiális közösségek jelen vannak az élőhelyeken, ahol fejlődnek (például széklet). A jó átadási tulajdonságok mellett a HF táplálja a fiatalokat (regurgitáció), és vonzza őket az emberi táplálékhoz. Mivel a HF nagy távolságokat tud repülni, ez a rovar nagyon jó a széklet baktériumok, beleértve az emberi és állati kórokozókat, valamint az enterococcusok antibiotikum-rezisztens törzseit (7). Egy nemrégiben készült tanulmány a KANASAS-I gyorséttermekben a HF-ből származó enterococcusok antibiotikum-rezisztenciáját és virulenciagénjeit vizsgálta. Ez a tanulmány kimutatta, hogy “az élelmiszer-kezelő és-kiszolgáló létesítményekben található háziasított baktériumok képesek antibiotikum-rezisztens és potenciálisan virulens enterococcusokat hordozni, amelyek képesek az antibiotikum-rezisztencia gének horizontális átvitelére más baktériumokra” (7).A hatások E. a faecalis a környezetre általában negatívabb. Általában szennyezik a vízellátást, amely fertőzött növényekhez, valamint az emberek fertőzéseihez vezethet (8). Az antibiotikum faktorokat különböző rovarok (pl. házi legyek) és állatok is szállíthatják, ami egyre több virulens E. faecalis-t eredményez.
Pathology
a nozokomiális fertőzések egyik fő oka az Enterococcus faecalis, ezen a csoporton belül az Enterococcus faecalis okozza az emberi enterococcus fertőzések többségét. Ezek a fertőzések lehetnek lokálisak vagy szisztematikusak, ide tartoznak a húgyúti és hasi fertőzések, sebfertőzések, bakterémia és endocarditis (2). Mivel az E. faecalis számos környezeti kihívást képes túlélni (például a hőmérsékleti szélsőségeket és az epesók jelenlétét), és mivel több antibiotikummal szembeni rezisztenciát szerezhetnek, ezek a baktériumok jelentős egészségügyi problémává váltak. Az Országos nozokomiális Fertőzésfelügyeleti rendszer (NNIS) 1989 óta a vankomicin-rezisztens enterococcusok (VRE) okozta fertőzések előfordulásának növekedéséről számolt be (1). Ez súlyos egészségügyi problémákat jelenthet, például a VRE-fertőzésekre rendelkezésre álló antibiotikum-terápia hiányát, mivel a legtöbb VRE-törzs a vankomicinen kívül több antibiotikummal is rezisztenciát mutat (például aminoglyskoidokkal és ampicillinnel). A vanocmicin-rezisztens gének vre-ről más Gram-pozitív kórokozókra történő átvitele komoly közegészségügyi probléma. A leggyakoribb módja annak, hogy az E. faecalis fertőzést okoz egy kórházban/hosszú távú gondozási létesítményben, az E. faecalis átadása a betegek között (8). Az enterococcusokat az egészségügyi dolgozók kezében lehet szállítani (átvinni) egyik betegről a másikra. Kimutatták, hogy a kezekben lévő VRE akár 60 percig is fennállhat (8). Az egészségügyi dolgozó kezéből a betegbe történő átvitel a beteg intravénás vagy húgyúti katéterével való érintkezéskor történhet. A rektális hőmérők, amelyeket használat után nem tisztítanak megfelelően, továbbíthatják a VRE-t a betegről a betegre is. Néha az átvitel a páciens GI-traktusának kolonizációját eredményezheti a megszerzett törzssel. Az új törzs ezután a beteg endogén flórájának részévé válik (8). A megszerzett törzs, amely antibiotikum-rezisztencia géneket hordoz, képes a GI-traktusban élni. A fertőzések ezután ezekből az újonnan szerzett E. faecalis törzsekből származnak.E. a faecalis számos fertőzést okozhat az emberi szervezetben. Az enterococcusok által okozott leggyakoribb fertőzés a húgyúti fertőzés. Az E. faecalis alacsonyabb húgyúti fertőzéseket (UTI) okozhat, mint például cystisis, prostatitis és epididymitis (8). Az E. faecalis intraabdominális, kismedencei és lágyszöveti fertőzésekben is megtalálható. Az E. a faecalis nosocomiális bakterémiát okozhat. A bakterémia forrása leggyakrabban a húgyúti, amely fertőzött intravénás katéterből származik. Az Endocarditis a legsúlyosabb Enterococcus fertőzés, mivel a szívbillentyűk gyulladását okozza. Sok esetben az endocarditis, antibiotikum kezelés sikertelen, műtét, hogy távolítsa el a fertőzött szelep van szükség (8). Az E. faecalis által okozott kevésbé gyakori fertőzések közé tartozik a meningitis, hematogén, osteomyelitis, szeptikus ízületi gyulladás és (nagyon ritkán) tüdőgyulladás. Az enterococcusok sok antibiotikummal szembeni rezisztenciája miatt ezeknek a fertőzéseknek a kezelése nehéz.
A biotechnológia alkalmazása
az enterococcusokat probiotikumként való lehetséges felhasználásra vizsgálták (olyan étrend-kiegészítő, amely ÉLŐ, nem virulens mikrobiális sejteket tartalmaz, amelyek lenyeléskor úgy gondolják, hogy kedvezően befolyásolják a bél mikroflóra összetételét). Kimutatták, hogy az E. faecalis törzs alkalmazása csökkenti a hasmenést. Az E. faecalis probiotikumokat csirke / sertés / szarvasmarha takarmányban használják az állatok hasmenésének csökkentésére (8).
az E. faecalis tulajdonságait okozó magas betegség miatt sokkal több kutatást végeztek az E. faecalis virulenciájának megállítására, mint az E. faecalis előnyös alkalmazására.
jelenlegi kutatás
1.) Az Enterococcus faecalis által okozott fertőzések reménye (4)
ismert, hogy a vankomicin-rezisztens baktériumok (pl. faecalis) számos problémát jelentenek a társadalom számára, ami olyan bakteriális fertőzéseket okoz az emberekben, amelyeket nehéz kezelni. Az enterokokkusz fertőzések kihívást jelentenek, mivel az organizmusok képesek gyorsan megszerezni és terjeszteni a rezisztencia géneket. A Ceftobiprole-t (BPR) vizsgálati cefalosporinként alkalmazták Gram-pozitív coccusok ellen. A BPR egy széles spektrumú parenterális cefalosporin, amely gram-pozitív és Gram-negatív penicillin-kötő fehérjékből áll. Stabilitást mutat a β-laktamázok hidrolízisével szemben is.Ez a tanulmány a BRP aktivitását vizsgálta az E. faecalis nagy gyűjteményével szemben, a vankomicin-rezisztens izolátumok elleni BPR baktericid aktivitást vizsgálva. A tanulmány megállapította,hogy az E. faecalis-ban a BPR-re érzékenységet nem befolyásolja a vankomicin rezisztencia vagy a β-laktamáz termelés. Az E. faecalis törzsekben, amelyek vankomicin rezisztenciát (VanA és VanB fenotípusok) vagy Ampicilin rezisztenciát mutattak, a BPR baktericid volt. A kutatók kimutatták, hogy a BPR baktericid aktivitást mutatott az E. faecalis ellen 750 mg dózisban, gátolva az E. faecalis aktivitásának 100% – át. Bár a β-laktamáz enzim jelenléte ritka E. faecalis-ban, jelenléte veszélyezteti a leghatékonyabb anti-Enterococcus β-laktámok (például ampicillin) alkalmazását. A BPR a β-laktamáz enzim gyenge szubsztrátja, amely megmagyarázza kiváló aktivitását az E. faecalis-t termelő β-laktamáz ellen.Ez a kutatás kimutatta, hogy a BPR erős aktivitást mutat az E. faecalis nagyon nagy gyűjteményével szemben. A BPR aktivitását nem befolyásolta a vankomicin rezisztencia vagy a β-laktamáz termelése. Ezért a BPR reményteljes szer a β-laktamáz-termelő és vankomicin-rezisztens E. faecalis fertőzések kezelésére emberben.
2.) Annak vizsgálata, hogy az Enterococcus faecalis rezisztenssé válik a linezolid (5)
gyógyszerrel szemben, amikor antibiotikumokat használnak bakteriális fertőzés kezelésére, hatással lehetnek a bélflórára. A rezisztens baktériumok kiválaszthatók a kezelés során, például az enterococcusok, amelyek potenciálisan patogének. A rezisztencia kialakulása problémát jelent az új antibiotikumok számára, mivel veszélyeztetheti az antibiotikumok hasznosságát.Ez a tanulmány az E. faecalis antibiotikumokkal szembeni rezisztenciájának kialakulását vizsgálta. Pontosabban, a kutatók a linezoliddal szembeni rezisztenciát vizsgálták (az első az “oxazolidinonok”néven ismert új antibiotikum-osztályból). A Linezolid alkalmazható többszörös gyógyszerrezisztens Gram-pozitív coccusok ellen, beleértve a VRE-t is. Gátolja a bakteriális fehérjeszintézist azáltal, hogy kifejezetten egy doménhez kötődik az 50-es riboszomális alegységben, és nem befolyásolja az egyéb antibiotikumokat befolyásoló rezisztencia mechanizmusok. Ez a vizsgálat a linezolid-rezisztens E. faecalis mutánsok kialakulásának sebességét vizsgálta a gnotobiotikus egerek emésztőrendszerében. A linezolid do-ját vízben táplálták, 0,5, 0,005-0,005 g/l dózisokkal. a mutánsok mind a megadott linezolidtól függtek, a rezisztencia szintje az expozíció időtartamával nőtt. Linezolid hiányában nem izoláltak mutánsokat, ami arra utal, hogy a linezoliddal szembeni de novo rezisztencia ritka volt az Enterococcusokban.A kutatás megállapította, hogy egyetlen 23S rRNA gén mutációja volt a linezolid rezisztencia kialakulásának kritikus lépése. Az egyedülálló mutánsokkal történő primer kolonizációt már a kezelés megkezdése után 5 nappal megfigyelték egerekben.Ezek az egerekkel végzett kísérletek segítenek megmagyarázni a klinikai izolátumokban megfigyelt linezolid-rezisztencia kialakulásának mintáját. A kutatócsoport kimutatta,hogy az adag kritikus az ellenállás dinamikájához. Ezeknek az eredményeknek segíteniük kell meghatározni a legjobb terápiás stratégiákat, hogy minimalizálják a rezisztencia kialakulását a klinikai környezetben, esetleg sok életet megmentve.
3.) Az Enterococcus faecalis-ban található SER/Thr kináz az antimikrobiális rezisztenciát közvetíti (6)
az Enterococcus faecalis számos antibiotikum-rezisztens fertőzést okoz kórházakban, ami bizonyos antibiotikumokkal szembeni inherens rezisztenciájának, valamint a béltraktusban való túlélésre és proliferációra való képességének a következménye.A genetikai alapja a rezisztencia látható E. a faecalis nem ismert, ez a kutatás megpróbálja azonosítani az ellenállás okát. A kutatók kimutatták, hogy a PrkC, egykomponensű jelző fehérje, amely eukarióta típusú Ser/Thr kináz domént tartalmaz, lehetővé tette az E. faecalis inherens antimikrobiális rezisztenciáját és intesztinális perzisztenciáját. Megállapították, hogy a PrkC-t nem tartalmazó E. faecalis mutáns az antimikrobiális stressz hiányában vad típusú ütemben nőtt, de fokozott érzékenységet mutatott a sejtburok-aktív vegyületekkel szemben, beleértve a sejtfal biogenezisét és az epe-tisztítószereket célzó antibiotikumokat is.A PrkC szabályozza az E. faecalis élettani folyamatait, amelyek kulcsfontosságúak a nozokomiális kórokozó sikeréhez. A kutatók prkc becsült szerkezete egy citoplazmatikus kináz domén volt, amelyet egy transzmembrán szegmens választ el, amely úgy gondolta, hogy összekapcsolja az uncross-linked peptidoglikánt. Ez azt sugallta, hogy a PrkC egy transzmembrán receptor, amely figyeli az E. faecalis sejtfal integritását, és adaptív válaszokat közvetít az intergritás fenntartása érdekében. A PrKC fontos az E. számára. a faecalis nozokomiális fertőzéseket okoz, ami arra utal, hogy a jelző fehérje célpontja az antibiotikum-rezisztens enterococcusok által okozott fertőzések megelőzésére szolgáló terápiák kifejlesztésének.
1.) I. T. Paulsen, L. Banerjei, G. S. A. Myers, K. E. Nelson, R. Seshadri, T. D. Read, D. E. Fouts, J. A. Eisen, S. R. Gill, J. F. Heidelberg, H. Tettelin, R. J. Dodson, L. Umayam, L. Brinkac, M. Beanan, S. Daugherty, R. T. DeBoy, S. Durkin, J. Kolonay, R. Madupu, W. Nelson, J. Vamathevan, B. Tran, J. Upton, T. Hansen, J. Shetty, H. Khouri, T. Utterback, D. Radune, K. A. Ketchum, B. A. Dougherty, C. M. Fraser. “A mobil DNS szerepe a vankomicin-rezisztens Enterococcus faecalis kialakulásában.”Tudomány. 2003. március. Vol. 299, 5615. p. 2071-2074
2.) Murrary BE. 1998. május. “Sokszínűség a multirezisztens enterococcusok között.”Feltörekvő Fertőző Betegségek. Vol. 4, 1. p. 46-65.
3.) De la Maza, Luis M., Marie T. Pezzlo és Janet T. Shigei. Az orvosi Bakteriológia színes atlasza. Washington, DC: American Society for Microbiology Press, 2004.
4.) Arias C., Singh K., Panesso D., Murray BE. “Time-Kill and Synergism Studies of Ceftobiprole against Enterococcus faecalis, Including ß-Laktamase-Producing and Vankomycin-Resistant Isolates.”Antimikrobiális szerek és kemoterápia. 2007. június. Vol. 51., 6. p. 2043-2047.
5.) Bourgeois-Nicolaos N., Massias L., Couson B., Butel MJ, Andremont A., Doucet-Populaire F.”.”The Journal of Infectious Diseases. 2007. Vol. 195. p. 1480-1488.
6.) Kristich C., Wells C., Dunny G. “Az Enterococcus faecalis-ban található eukarióta típusú Ser/Thr kináz antimikrobiális rezisztenciát és bél perzisztenciát közvetít.”Proceedings of the National Academy of Sciences of the United States of America. 2007. február. Vol. 104, 9. p. 3508-3513.
7.) Macovei, L., Zurek, L. ” az antibiotikum-rezisztencia gének ökológiája: az enterococcusok jellemzése Az élelmiszer-környezetben gyűjtött Háziasításokból.”Applied and Environmental Microbiology. 2006. június. Vol. 72., 6. p. 4028-4035.
8.) Gilmore, Michael. Az enterococcusok: patogenezis, molekuláris biológia és antibiotikum rezisztencia. Washington, DC: American Society for Microbiology Press, 2002.
9.)Nallapareddy SR, Singh KV, Sillanpää J, Garsin DA, Höök M, Erlandsen SL, Murray BE.. “Endocarditis and biofilm-associated Pili of Enterococcus faecalis.”A Journal of Clinical Investigation. 2006. október. A 116. p.2799-2807.
szerkesztette Richard A. Martinez, az UC San Diego, diák Rachel Larsen.