Célok
- Ismert, majd ismeretlen megoldások a fém ionok \(\ce{Ag^{+}}\), \(\ce{Fe^{3+}}\), \(\ce{Co^{2+}}\), \(\ce{Cu^{2+}}\), valamint a \(\ce{Hg^{2+}}\) elemzik papírt használ, kromatográfiás módszerrel.
- egy ismeretlen megoldás, amely ezen kationok egy részét tartalmazza, az ismert oldatok festett foltjainak Rf értékeihez és színeihez viszonyítva kerül azonosításra.
a legtöbb vegyésznek és sok más tudósnak rutinszerűen el kell különítenie a keverékeket és azonosítania kell azok összetevőit. A mintában található anyagok minőségi azonosításának képessége kritikus lehet. Például egy szennyezett talajvíz mintáit vizsgáló környezetvédelmi vegyész tudni akarja, hogy mely mérgező ionok lehetnek jelen a mintában.
a kromatográfia az ilyen helyzetekben használt első eszközök egyike. Ebben a technikában sokféle keverék elkülöníthető a komponens tiszta anyagokra; a standard mintához képest minden egyes összetevő anyag kísérleti jelleggel azonosítható.
a kromatográfia számos fajtája létezik, mindegyik a keverékek meghatározott típusainak elválasztására szolgál. A kromatográfia minden típusának közös jellemzője, hogy egy mozgó fázist (folyadékot vagy gázt) egy álló fázison (szilárd anyagon) keresztül tolnak át. Az 1. táblázat a kromatográfia számos fajtáját és a fázisok jellemző identitását sorolja fel. Ebben a kísérletben papírkromatográfiát használnak.
|
Type of Chromatography |
Mobile Phase |
Stationary Phase |
|---|---|---|
|
Gas (GC) |
inert gas (helium) |
waxy liquid or silicone inside narrow tubing |
|
Liquid |
solvent/solvent Mixture (organic or aqueous) |
solid packing (silica, alumina) |
|
Paper |
solvent/solvent Mixture (organic or aqueous) |
paper |
|
Thin-Layer (TLC) |
solvent/solvent Mixture (organic or aqueous) |
silica/alumina coated glass, plastic or metal |
az oszlopkromatográfia példája (1.ábra) bemutatja az analitikai technikában található tipikus jellemzőket. Az ábra egy kísérletet mutat, ahol egy kétkomponensű keveréket oszlopkromatográfiának vetnek alá. Az oszlop szilárd anyaggal van ellátva, amelyet helyhez kötött fázisnak neveznek. Az oszlopba folyékony oldószert vagy eluáló oldatot öntünk, majd teljesen átitatjuk a szilárd csomagolóanyagot. Ezután a keveréket a nedves oszlop tetejére töltjük, majd több eluenst adunk hozzá. A gravitáció lehúzza a mozgó fázist az álló fázison keresztül, és a keverék komponensei különböző sebességgel mozognak az oszlopon. Az ábrán az a komponens gyorsabban mozog, mint a B komponens; így a B komponens hosszabb ideig megmarad az oszlopon, mint az A. komponens.általában ez annak köszönhető, hogy a két vegyület oldhatósága különbözik az oldószerben és/vagy a szilárd csomagolóanyaghoz való vonzódás különbsége. Mivel az oszlop tetejére több eluent kerül, az összetevők végül külön kilépnek az oszlopból. Az oszlopból való kilépéshez szükséges idő, az úgynevezett retenciós idő minden egyes komponens esetében reprodukálható lesz az adott meghatározott feltételek mellett-Mobil és álló fázisazonosságok, hőmérséklet és oszlopszélesség. Amint az összetevők kilépnek az oszlopból, az oldószer elpárologtatással eltávolítható, a tiszta komponensek pedig tovább elemezhetők vagy azonosíthatók.
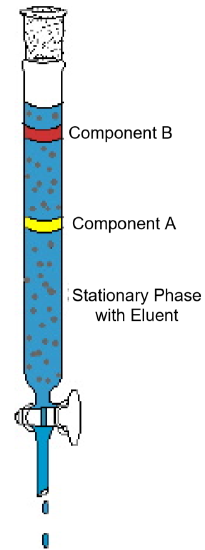
1. ábra: egy tipikus oszlopkromatográfiás kísérlet egy kétkomponensű keverék elválasztását mutatja.
az összetevők előzetes azonosítása úgy érhető el, hogy összehasonlítjuk az ismeretlen keveréket egy gondosan elkészített ismert keverékkel: ha egy ismert komponens ugyanolyan retenciós idővel rendelkezik, mint egy ismeretlen komponens azonos körülmények között, valószínű—de nem meggyőző—, hogy a két összetevő azonos. További elemzésre lehet szükség a hipotézis megerősítéséhez. Ha az ismert és az ismeretlen eltérő retenciós idővel rendelkezik, akkor nem valószínű, hogy a két összetevő azonos lenne.
a kromatográfia egyéb változatai kapilláris hatást alkalmaznak-a folyadék szilárd felületre való vonzása-az oldószer szilárd anyagon keresztül történő húzásához. A papírkromatográfia informális változata akkor figyelhető meg, ha egy tintával írt oldal vízzel vagy más folyadékokkal érintkezik. A tinta fut, és több szín van elválasztva a tinta csík.
az alábbi ábra (2.ábra) egy vékony rétegű kromatográfiás kísérlet eredményét mutatja. Két fekete tintafolt a szilárd felületen volt egy oldószer áthaladt rajtuk. Az oldószer víz vagy más folyadék, amelyet kapilláris hatással húznak át az álló fázison. Ebben a példában egy por alakú szilárd anyaggal bevont műanyag darabot használnak helyhez kötött fázisként. Alternatív megoldásként egy darab szűrőpapír használható álló fázisként. A kísérlet azt mutatja, hogy a fekete tinta több különböző színű anyagot tartalmazó keverék. Minden komponensnek kissé eltérő oldhatósága van a mobil fázisban, így amikor a folyadékot az álló fázison keresztül húzzák, minden komponens eltérő sebességgel mozog, elválasztva a tintát különböző színű foltokká.

2. ábra: a fekete tinta vékony rétegű kromatográfiája a fejlesztés után. Ez a kép egy gyakori problémát mutat, ahol a foltok kibővülnek, amikor felfelé mozognak a lemezen, végül összeolvadnak a lemez tetején.
ebben a kísérletben hasonló elveket alkalmaznak több fém kation elválasztására papírkromatográfiás eljárással. A fémionok- \ (\ce{Ag^{+}}\), \(\ce{Fe^{3+}}\),\(\ce{Co^{2+}}\), \(\ce{cu^{2+}}\), és \(\ce {Hg^{2+}}}\) – eltérő oldhatósággal rendelkeznek a mobil fázisban—vizes \(\ce{HCl}\) etil-és butil-alkohollal -, és különböző sebességgel mozognak a papír felett. A különböző fém-ion oldhatóságok valószínűleg annak köszönhetőek, hogy különböző vegyületek képződnek a kloridionnal, és változó oldódási képességük van a szerves oldószerben.
a papír elkészítésének módját bemutató diagram az alábbiakban látható. Ezen ionok mindegyikét tartalmazó Standard oldatokat kapilláris csővel, valamint mind az öt iont tartalmazó standard oldattal látják el a papírra. Egy ismeretlen is foltos lesz a papírra. Miután elkészült a papír, úgy fejlesztik ki, hogy a papírt az eluensbe helyezik. 75-90 perc elteltével a papírt kálium-jodidot, \(\ce{KI}\) és kálium-ferrocianidot tartalmazó vizes oldattal nedvesítjük. \(\ce{K4}\). Az egyes ionokra megfigyelt egyedi színt a vizualizációs oldattal végzett kémiai reakció hozza létre. Ez az egyik hasznos módja annak, hogy azonosítsuk, mely ionok vannak jelen egy ismeretlen keverékben.
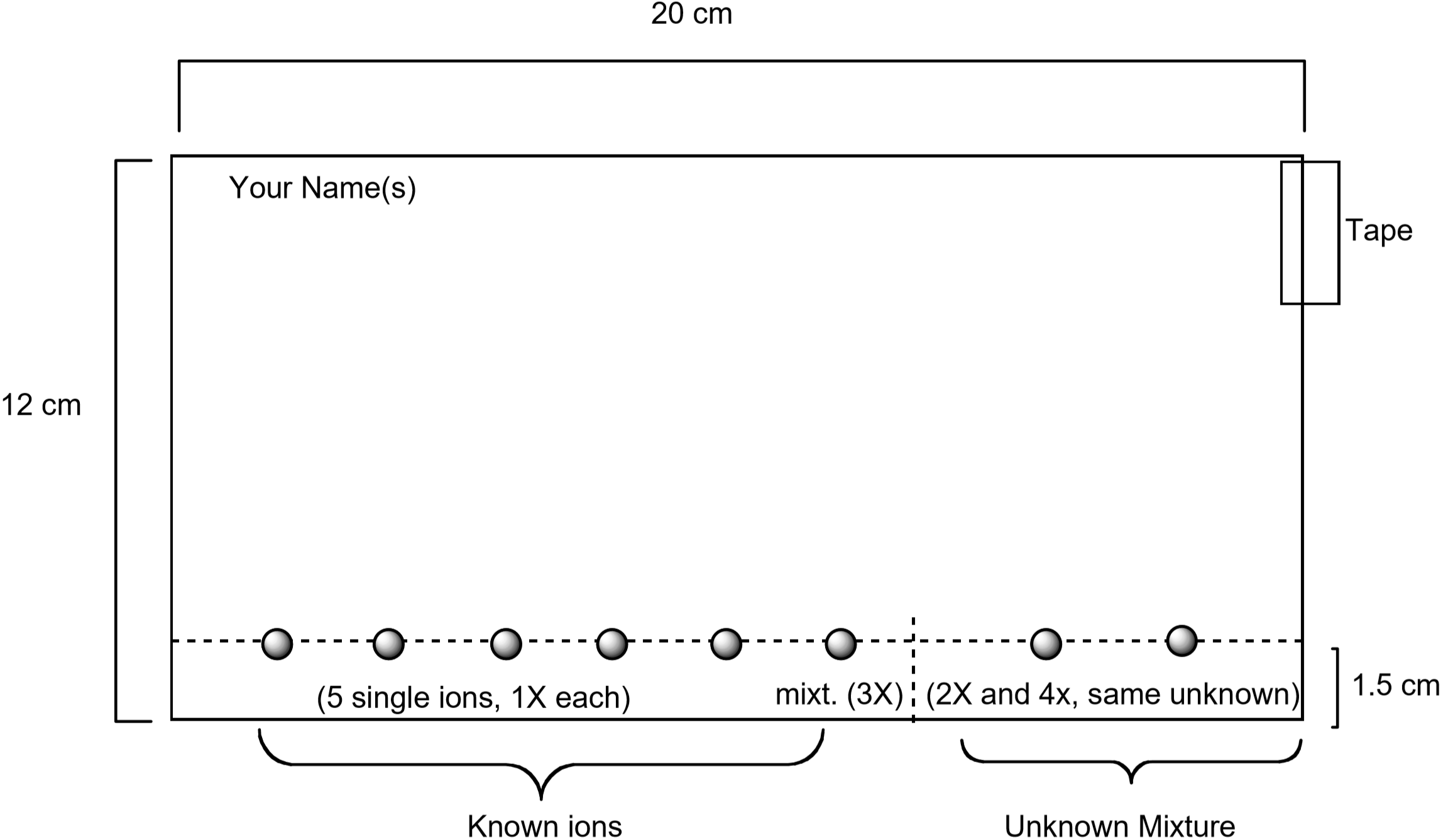
3. ábra: ábra, amely bemutatja, hogyan készítsük el a papírt a kromatográfiás kísérlethez
a távolság, amelyet az ion felfelé mozog, a papír is felhasználható az ion azonosítására. Mivel azonban a hallgatók kromatográfiás kísérleteiket különböző ideig, kissé eltérő körülmények között fejlesztik, minden hallgatónak kissé eltérő mért távolsága lesz egy adott ionhoz. Az ion (\(D\)) által az oldószer (\(F\), oldószer front) által mozgatott távolsághoz viszonyított távolság aránya jellemző, és közel azonos minden diák esetében. Ezt az arányt Rf-nek vagy “retenciós tényezőnek” nevezik.”
\
eljárás
anyagok és berendezések
vegyi anyagok: 0.1 M \(\ce{AgNO3}\), \(\ce{Hg(No3)2}\), \(\ce{Fe(NO3)3}\), \(\ce{Co(No3)2}\) és \(\ce{Cu(NO3)2}\) vizes oldata etil-és butil-alkohollal; vizualizáló oldat (\(\ce{KI}\) és \(\CE{K4}\)).
felszerelés: tiszta kromatográfiás papír; eldobható Latex kesztyű (a Nitrilkesztyű a raktárban a latexre allergiás emberek számára); 600 mL főzőpohár; műanyag csomagolás; csipesz vagy főzőpohár fogó; vonalzó *
*a raktárból nyert tételek
biztonság
kerülje a fémionoldatokkal, az eluáló oldószerrel és a vizualizáló oldattal való érintkezést. Viseljen eldobható kesztyűt, hogy megérintse a kromatogramot az elúció után, valamint a kísérlet hátralévő részében. Ne lélegezze be az eluáló oldószer vagy a vizualizáló oldat gőzét. Helyezze a nedves kromatogramot egy papírtörlőre, nem közvetlenül a laboratóriumi padra. A vizualizáló megoldást csak az oktató által biztosított helyen használja. A kesztyűket és a kromatogramot a kísérlet befejezése után dobja a megadott hulladéktartályba. Alaposan mosson kezet, miután kapcsolatba lépett a laboratórium összes megoldásával.
a kromatográfiás papír előkészítése
- minden diákpárnak meg kell szereznie egy szűrőpapírt a 3. ábrán látható méretekkel. Győződjön meg róla, hogy a papír tiszta, könnyek vagy hajtások nélkül. Használjon ceruzát – nem tollat – és vonalzót, hogy a papír hosszú szélétől egy cm-re húzzon egy vonalat a papíron. A fémion oldatokat ezen a vonalon fogja észrevenni. Írja be a nevét ceruzával a papír bal felső sarkában.
- gyakorlat pecsételő víz és / vagy ion oldatok rá egy csík szűrőpapír, hogy tudja, hogyan kell létrehozni foltok a megfelelő méretű. Használjon üveg kapilláris csöveket, hogy az ionokat a papírra helyezze. Az oldatot úgy alkalmazzuk, hogy könnyedén, gyorsan megérintjük a kapilláris csövet, amely az oldatot tartalmazza a papírra rajzolt vonalra. A foltoknak 5-8 mm átmérőjűnek kell lenniük. Az ennél nagyobb foltok túlzottan elterjednek a kísérlet során, és megnehezítik az elemzést.
- ismert 0.1 M a \(\ce{AgNO3}\), \(\ce{Hg(No3)2}\), \(\ce{Fe(NO3)3}\), \(\ce{Co(NO3)2}\) és \(\ce{Cu(NO3)2}\) vizes oldatai vizsgálati csövekben vannak elhelyezve, amelyek mindegyike két vagy három kapilláris csövet tartalmaz. A bal oldalon kezdve jelölje meg az ion azonosságát az egyes pontok alatt egy ceruzával; majd óvatosan helyezze az egyes ismert ionokat a vonalra. Ügyeljen arra, hogy ne szennyezze a kapilláris csövet más ionokkal, majd cserélje vissza a kapilláris csöveket a megfelelő kémcsőbe. Mind az öt Ion ismert keverékét tartalmazó kémcsövet kapilláriscsövek sorozatával is ellátják. Helyezze ezt a keveréket a vonalra is. Mivel ez az oldat hígabb, mint az egyionos ismert oldatok, háromszor alkalmazza az ismert keveréket, hagyva, hogy a folt megszáradjon az egyes alkalmazások között. A hő lámpa segít a folt gyorsabb szárításában.
- több ismeretlent is biztosítanak a kémcsövekben, kapilláris csövekkel együtt. Az oktató megmondja, hogy melyik ismeretlent kell használni. Az ismeretlenek egy-négy kationot tartalmaznak, és hígabbak, mint az egyionos ismert oldatok. Az ismeretlent szintén két-négy alkalommal kell alkalmazni a két kísérlethez, hagyva, hogy a folt megszáradjon az egyes alkalmazások között. Hiba esetén az ismeretlent két helyen kell észlelnie a vonal mentén, hogy két vizsgálat álljon rendelkezésre elemzésre.
a kromatográfiás papír kifejlesztése
- helyezzen egy darab szalagot a jobb felső él mentén, a 3.ábrán látható módon. Ezután alakítson ki egy hengert úgy, hogy a papír két rövid szélét összekapcsolja a szalaggal. Ügyeljen arra,hogy a szélek ne érintkezzenek. A papírnak hasonlónak kell lennie a 4. ábrához.
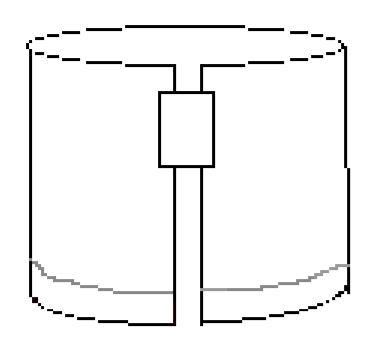
4. ábra: a hajtogatott papírnak így kell kinéznie a kísérlet kidolgozása előtt.
- szerezzen be 15 mL eluáló oldatot. Ennek az oldószernek egy részét óvatosan öntse egy 600 mL-es főzőpohárba, majd egy-két másodpercig óvatosan forgassa. Vigyázat: ne lélegezze be a gőzöket ebből a megoldásból! Győződjön meg róla, hogy a folyadék szintje a papír foltvonala alatt lesz, miután a papírt a fejlődő kamrába helyezték.
- helyezze a papírhengert a főzőpohárba a megjelölt éllel lefelé. A foltoknak az oldószer szintje felett kell lenniük. A papírnak nem szabad megérintenie a főzőpohár oldalát. Óvatosan fedje le a főzőpoharat műanyag csomagolással, majd 75-90 percig helyezze a motorháztetőbe. Az oldószernek el kell kezdenie felfelé mozgatni a papírt. Miután a főzőpoharat lefedték, győződjön meg róla, hogy szintje van, és ne zavarja a fejlesztési időszak alatt. Lehet, hogy az oktatónak van egy feladata, hogy dolgozzon, amíg vár.
a papír vizualizálása és elemzése
- miután a fejlesztési időszak véget ért, viseljen eldobható kesztyűt, és vegye le a papírt a főzőpohárról. A laborban Latex kesztyűk állnak rendelkezésre, a raktárban pedig nitril kesztyűk állnak rendelkezésre Latex allergiások számára. Hagyja, hogy az oldószer visszaszivárogjon a főzőpohárba, majd távolítsa el a szalagot. Helyezze a kromatográfiás papírt egy papírtörlőre, majd azonnal jelölje meg az oldószer elejét ceruzával. Öntsük a használt eluáló oldószert a mellékelt hulladéktartályba. Szárítsa meg a papírt egy meleg lámpa alatt a motorháztetőben. Vigyázat: Ne lélegezze be a gőzöket! Ügyeljen arra, hogy ne égesse el a papírt a lámpa alatt.
- miután a papír megszáradt, vigye a papírtörlő vizualizációs állomására. Röviden mártsa be a papírt a füstölőben lévő sekély edényben található vizualizáló oldatba. Azonnal emelje ki a papírt az oldatból, és hagyja, hogy a felesleges csepp le az állomáson. Helyezze a nedves papírt egy száraz papírtörlőre, majd azonnal szárítsa meg hőlámpa alatt, majd vigye a padra elemzésre.
- először keresse meg az egyes ismert egyionokat, majd jegyezze fel a megfigyelt színeket. Egyes foltok idővel elhalványulhatnak, ezért rögzítse a színeket, amíg a papír még nedves. Mérjük meg a távolságot minden helyszínen mozgott, D, egy vonalzó. Mérje meg az egyes helyek középpontját. Rögzítse adatait az adattáblázatban.
- mérje meg az oldószer elülső részétől való távolságot, F. az F értéknek megközelítőleg azonosnak kell lennie az egész papíron. Használja ezeket az értékeket az Rf kiszámításához minden egyes ion esetében. Végezze el a méréseket az 5. ábrán látható módon. Minden megfigyelt helynek saját Rf értéke van. Rögzítse eredményeit az adattáblázatban.
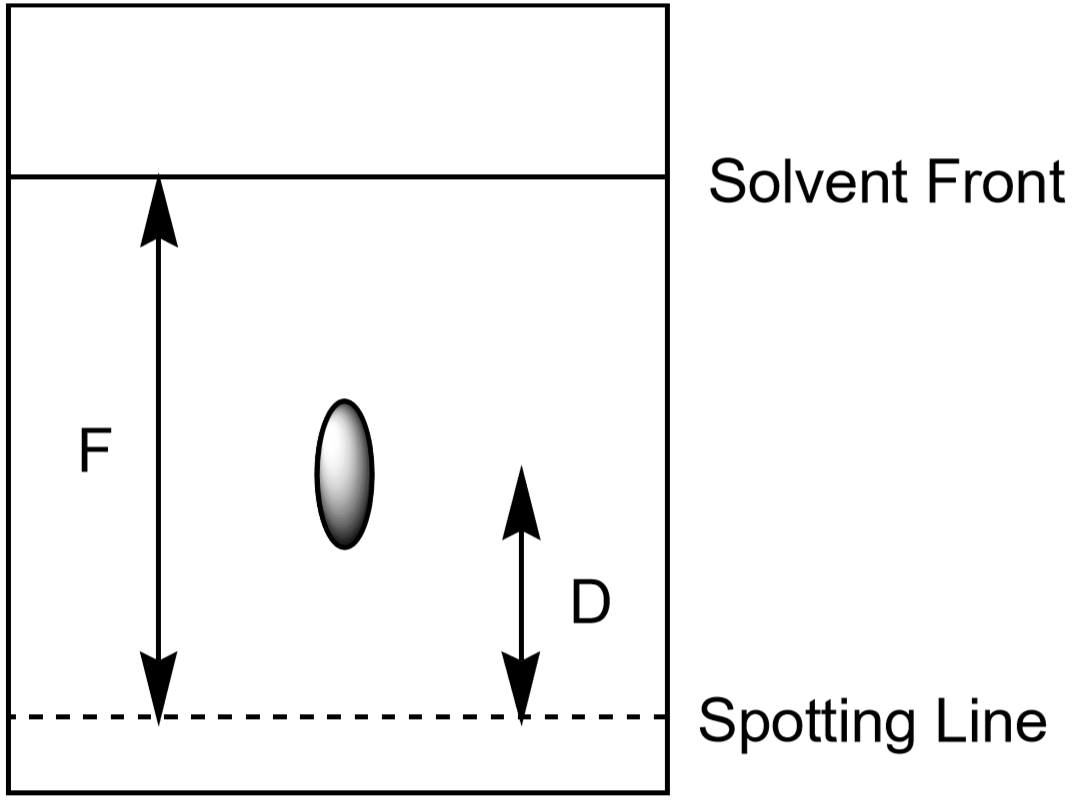
5. ábra: Az RF kiszámításához használt távolságok mérése egy helyszínen.
- a keveréket tartalmazó sávban keresse meg az egyes ionokat, és rögzítse az egyes ionok által mozgatott távolságot. Számítsa ki az Rf-t minden egyes ionra ebben a sávban. Az értékeknek szorosan illeszkedniük kell az egyionos köpenyekben megfigyelt értékekhez.
- az ismeretleneket tartalmazó sávban keresse meg a megfigyelt helyek középpontját, rögzítse annak távolságát, és számolja ki az Rf értékeket. Használja azt a sávot, amelyen a legtisztább foltok vannak. Az ismeretlen foltok szín-és Rf-értékeinek szorosan illeszkedniük kell az ismert ionok egy részéhez. Most képesnek kell lennie arra, hogy azonosítsa, mely ionok vagy ionok találhatók az ismeretlenben. Rögzítse adatait a megfelelő táblázatban.
- Készítsen vázlatot a kromatogramjáról a laborjelentési űrlapon megadott helyen, ügyelve arra, hogy jelezze a papír minden egyes helyének helyzetét és hozzávetőleges méretét és alakját. A papírt a kijelölt hulladéktárolóban dobja ki.
helyezze a kromatográfiás papírt és a használt kesztyűt a mellékelt hulladéktárolóba. A használt eluáló oldatot már egy másik hulladéktartályba kellett volna helyezni. Ne feledje, hogy két különböző hulladéktartályok biztosítják ezt a kísérletet, így biztos, hogy olvassa el a címkéket, így fogja használni a megfelelőt! Ügyeljen arra, hogy alaposan mosson kezet, mielőtt elhagyja a laboratóriumot.
laboratórium előtti hozzárendelés: Papírkromatográfia
- a kétkomponensű keveréket papírkromatográfiával elemezzük. Az a komponens jobban oldódik a mobil fázisban,mint a B komponens. Számítsa ki az egyes komponensek Rf-jét, majd jelölje meg az egyes helyek azonosítóját.
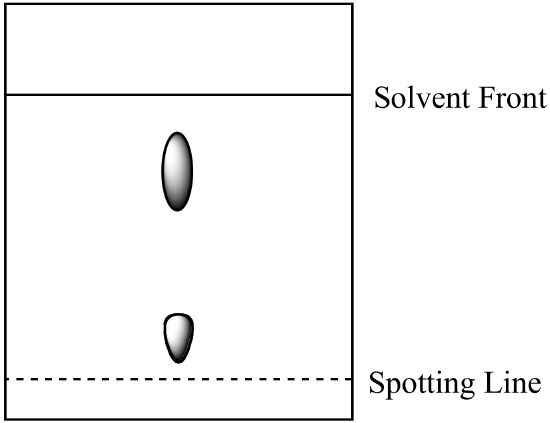
- az 1. kérdésből (fent) származó keveréket oszlopkromatográfiával elemezzük ugyanazon mozgó fázis és szilikagél álló fázis segítségével. Melyik komponensnek van rövidebb retenciós ideje? Magyarázza el a választ. (Tegyük fel, hogy az összetevők és az álló fázis között azonos típusú kötési erők vannak jelen mind a papírkromatográfiában, mind az oszlopkromatográfiában.)
- egy ismeretlen folyadékmintát elemeznek papírkromatográfiával x oldószerrel, mint mobil fázist. Egy folt figyelhető meg a lemez kifejlesztése és vizualizálása után. Ugyanazt az ismeretlen anyagot újra elemezzük az Y oldószerrel, mint a mobil fázis. Ezúttal három folt figyelhető meg a lemez kifejlesztése és vizualizálása után.
- az ismeretlen minta tiszta anyag vagy keverék? Magyarázza el a választ, beleértve a két kísérlet különböző megfigyeléseinek lehetséges okait.
Lab Report for Paper Chromatography
Data, Observations, Calculations and Analysis Known Ions
Known Ions
|
Ion |
Spot Color (Stained) |
D (Single- Ion) |
F (Single- Ion) |
Rf |
D (Ion Mixt.) |
F (Ion Mixt.) |
Rf |
|---|---|---|---|---|---|---|---|
|
\(\ce{Ag^{+}}\) |
|||||||
|
\(\ce{Co^{2+}}\) |
|||||||
|
\(\ce{Cu^{2+}}\) |
|||||||
|
\(\ce{Fe^{3+}}\) |
|||||||
|
\(\ce{Hg^{2+}}\) |
Unknown ID Code _________________
Unknowns
|
Spot Number (from lowest Rr) |
Spot Color (Stained) |
D (Unknown) |
F (Unknown) |
Rf |
Identity of Spot |
|---|---|---|---|---|---|
- Sketch of Chromatogram:
Summary:
| Ismeretlen ID Kód | Ionok Azonosított |
|---|---|
Kérdések, Következtetések
- Milyen kritériumokat használtak, hogy azonosítsa a ion(s) található az ismeretlen? Magyarázza el válaszát legalább három mondatban. Tartalmazza az ionok azonosításának nehézségeit.
- ha hagyja, hogy a kísérlet csak 30 percig futjon, mi lenne a valószínű eredmény? Felmerül-e bármilyen probléma az ismeretlen azonosításában?
- Ha \(\ce{Co^{2+}}}\) és \(\ce{cu^{2+}}\) a foltok azonos színűek lennének, nehezebb lenne egy ismeretlen azonosítása? Magyarázza el a választ.