i vægtforøgelsen forbundet med behandlingen af Schisofreni: en seks måneders dobbeltblind randomiseret parallelgruppestudie
Enric*; Miguel Bernardo L. Montejo * * * *
* Institut for psykiatri. Hospital De La Santa Creu i Sant Pau. CIBERSAM, universitetet i Barcelona, IBSantpau Barcelona. Spanien
** Institut for Psykiatri, Hospital Clinic de Barcelona, CIBERSAM, universitetet i Barcelona, IDIBAPS, Barcelona. Spanien
* * * Universitetshospital kompleks af Badajose. Ekstremadura Sundhedsvæsen, Badajose. Spanien
**** Universitetshospital i Salamanca. School of Medicine, universitetet i Salamanca, Salamanca. Spanien
denne undersøgelse blev finansieret af Pfis.
korrespondance
abstrakt
baggrund og mål: Tidligere data fra sikkerhedsanalysen tyder på, at der kan forekomme betydelig vægtforøgelse, mens der ikke er observeret nogen ændring med ciprasidon. Fedme kan være en trussel mod helbredet og få forsøgspersoner til at afbryde deres antipsykotiske medicin. For yderligere at evaluere de differentielle virkninger af siprasidon og olansepin på vægtøgning blev der udført en undersøgelse med kropsvægt som det primære effektendepunkt.
metoder: En seks måneders randomiseret, dobbeltblind, parallel undersøgelse blev udført hos mandlige og kvindelige forsøgspersoner i alderen 18-70 år med en primær diagnose af schisofreni (DSM-IV-TR) og en klinisk tilstand, der kræver behandlingsstart med et nyt antipsykotisk middel. Halvtreds patienter blev inkluderet. Effektresultaterne blev vurderet ved baseline og ved uge 1, 4, 12, 18 og 24. Det primære effektendepunkt var den procentvise ændring i kropsvægt i uge 24 fra baseline. Sikkerheden blev også vurderet.
resultater: I uge 24 var der en signifikant større stigning i kropsvægt (7,5%, p <0,0001) hos patienter, der blev behandlet med ciprasidon, og antallet af personer, der havde en vægtøgning > 7% var signifikant højere i ciprasidon-gruppen (n = 11 ) vs N = 3 ; eller = 6.246, p-værdi = 0.0150). PANNS-N faldt signifikant i begge grupper. De fleste Ae ‘ er var moderate eller milde i begge grupper.
konklusioner: Olanapin øger kropsvægten betydeligt i uge 24. Imidlertid forbedrede behandlingen med enten PANSS positive, negative og generelle psykopatologiske score og tolereredes godt.nøgleord: antipsykotiske midler, vægtøgning, fedme.patienter viser en højere prævalens af fedme, glukoseintolerance og type 2-diabetes mellitus med en genetisk forbindelse til glykolyse1,2 og en højere frekvens af kardiovaskulære hændelser3. Desuden er mange anden generation antipsykotika forbundet med en højere risiko for vægtforøgelse2,4, insulinresistens, hyperglykæmi og dyslipidæmi5. Kombinationen af disse forskellige faktorer, genetisk modtagelighed, en stillesiddende livsstil og dårlig diæt og de negative bivirkninger af den antipsykotiske behandling udgør en vigtig risikofaktor for hjerte-kar-sygdom hos patienter behandlet med atypiske antipsykotika6. Fedme er ikke kun en trussel mod sundhed og lang levetid, men det kan også få forsøgspersoner til at afbryde deres antipsykotiske medicin7.dette er en af de mest almindelige typer af antipsykotika, der anvendes til behandling af sygdomme. Atypiske antipsykotiske lægemidler viser bedre effektivitet og mindre negative bivirkninger end typiske antipsykotika8,9. De er dog stadig tilbøjelige til at forårsage uønskede virkninger, herunder hypostatisk hypotension10, søvnighed11, vægtøgning 1,2, dyslipidæmi12, hyperglykæmi og diabetes mellitus5 og hyperprolactinæmi, som kan generere fertilitetsproblemer, seksuel dysfunktion og nedsat knoglemineraltæthed13,14.
tidligere undersøgelser har ikke vist ændringer i vægt eller metabolisme hos personer behandlet med siprasidon1,2,15, Siprasidon viser lav tilbøjelighed til at forårsage ekstrapyramidale bivirkninger (EPS) eller laboratorie abnormiteter8,16,17 og påvirker ikke den seksuelle funktion hos schisofreniske patienter18. Det er rapporteret,at siprasidon forårsager vægttab og reduktion i serumlipidniveauer19, 20.er en af de hyppigst ordinerede antipsykotiske lægemidler, med dokumenteret effekt for schisofreni symptomer21-23. Imidlertid er olanapin blandt de atypiske antipsykotiske lægemidler, der inducerer vægtforøgelse24, 25, der også er forbundet med betydelige stigninger i total cholesterol, triglycerider,LDL og fastende insulin20,26, 27. I tidligere undersøgelser, der udelukkende eller kombineret med andre behandlinger, viste olanapin signifikant større stigninger i vægt og BMI og en højere sandsynlighed for hurtig vægtøgning end nogen anden behandling7,20,26,27. Imidlertid havde alle disse undersøgelser en effektvariabel som den primære variabel, idet vægtvurdering kun var en del af sikkerhedsundersøgelsen.
antipsykotiske behandlinger er ofte langsigtede, og det er nødvendigt at overveje den øgede risiko for metaboliske ændringer i patientplejen. Derfor blev denne randomiserede, dobbeltblinde undersøgelse designet til specifikt at behandle spørgsmålet om vægtøgning på lang sigt (6 måneder), hvilket er den primære variabel. I betragtning af at andre faktorer er relateret til patientens disposition og overholdelse af behandlingen, vurderede denne undersøgelse livskvalitet, generel funktion, præferencer og holdning til behandling for at give mere information om spørgsmål, der skal behandles i disse langvarige behandlinger og for at diskutere deres forhold til hovedformålet.
metoder
en seks måneders randomiseret, multi-center, parallel, dobbeltblind undersøgelse blev udført fra April 2003 til februar 2007 for at estimere og sammenligne virkningerne af siprasidon versus olansepin på kropsvægt i behandlingen af personer med schisofreni.
undersøgelsen blev udført på 11 centre i hele Spanien. Mandlige eller kvindelige forsøgspersoner i alderen 18-70 år med en primær diagnose af schisofreni ifølge DSM-IV-TR28 og en klinisk tilstand, der kræver behandlingsstart med et nyt antipsykotisk lægemiddel, blev tilmeldt. Patienter eller deres juridiske repræsentant gav deres informerede samtykke. > 500 ms), klinisk signifikante unormale laboratorieværdier, epilepsi, anfald, psykokirurgi, manglende respons eller tidligere intolerance over for olanapin eller siprasidon; graviditet eller amning serologisk bevis for HIV eller hepatitis; behandling med begge lægemidler inden for de 6 måneder forud for screening; patient ude af stand til eller med vanskeligheder med at overholde undersøgelsesprotokollen; øjeblikkelig risiko for at begå skade på sig selv eller andre; samtidig behandling med antipsykotiske midler efter randomisering; depot antipsykotisk medicin inden for en måned efter indrejse; behandling med antidepressiva eller humørstabilisatorer inden for to uger efter randomisering; stofmisbrug inden for de foregående 3 måneder; organisk psykisk sygdom; behandling med kliniske lægemidler inden for 30 dage før randomisering.
undersøgelsen blev udviklet i overensstemmelse med erklæringen fra Helsinki29, og undersøgelsesprotokollen blev godkendt af de etiske udvalg, der svarer til de involverede Centre, og af afdelingen for lægemidler til Human brug for det spanske agentur for medicin og sundhedsprodukter (AEMPS).
forsøgspersoner blev inkluderet i undersøgelsen 12 timer efter den tidligere antipsykotiske dosis, bortset fra forsøgspersoner behandlet med et depot-antipsykotisk middel (se ovenfor) og blev tilfældigt fordelt i et forhold på 1:1.
behandlingsdosis og besøgsplan
dosering var fleksibel inden for 3 niveauer: Lav (40 mg BID eller 5 mg BID), Medium (60 mg BID eller 15 mg gang) og høj (80 mg BID eller 10 mg BID). Behandlingen blev initieret med lav dosis i dag 1-7, og fra dag 3 og fremefter kunne dosis justeres.
behandlingsfasen (6 måneder) omfattede 6 besøg: dag 1 (uge 0), uge 1, uge 4, uge 12, uge 18 og uge 24. Opfølgningsbesøg (uge 48) udført seks måneder efter afslutningen af behandlingen. Studiemedicin blev rapporteret fra Besøg 1 til 6. Forsøgspersoner, der viste utilstrækkelig respons på ethvert tidspunkt i løbet af undersøgelsen, som angivet ved en klinisk Global Impression of Improvement (CGI-i) score på karrus 6, blev trukket tilbage.
effekt-og sikkerhedsvurderinger
de målte effektresultater var vægt, BMI og taljeomkreds (toilet); blodtryk og puls; den positive og negative syndromskala (PANSS)30; den kliniske globale indtryk (CGI) skala31 og en anden til forbedring (CGI-I); patientens fysiske aktivitet; patientpræferenceskalaen (PPS) for at måle patientens tilfredshed med medicin; den spanske version af Sundhedsforsyningsindekset-Mark 3 (HUI-3)32,22. Appetit blev målt ved en visuel analog skala (VAS), en subjektiv kvantificeringsmetode. Patienten markerer sit appetitniveau siden sidste besøg på en vandret linje markeret 0 (ingen appetit) venstre og 10 (ekstremt sulten) til højre. Afstanden fra 0 måles derefter i cm og appetitniveauet kvantificeres.
alle effektresultater blev vurderet ved besøg 1 (baseline-værdier) og desuden: CGI-s, CGI-i og PANSS fra Besøg 2 til 7, appetit og patientens fysiske aktivitet fra besøg 3 til 6, PPS og HUI-3 ved besøg 4 og 6
sikkerhedsevalueringer omfattede klinisk overvågning, elektrokardiogrammer, vitale tegn, bivirkninger (AEs) og sikkerhedslaboratorietest. Sikkerhedsvurderinger blev rapporteret i henhold til verdensomspændende sikkerhedsstandarder (VSS) Version 3 krav.
statistisk analyse
alle analyser blev udført på intent-to-treat (ITT) – populationen ved hjælp af SAS-kur version 8.2 eller nyere. Statistiske tests var 2 tailed og p-værdier på 0.05 eller mindre blev betragtet som statistisk signifikante. Behandling blev monteret som en kategorisk. 95% konfidensintervaller (CI) blev konstrueret omkring alle estimerede behandlingsforskelle. Alle ændringer blev analyseret ved analyse af kovarians (ANCOVA) inklusive effekter for behandlingsgruppe og baseline værdi (hvis relevant). Beskrivende statistik blev brugt til at opsummere alle sikkerhedsvurderinger. Bivirkninger blev kodet i henhold til Medical Dictionary for Regulatory Activities (MedDRA). Der blev ikke udført nogen formel statistisk test af sikkerhedsparametre.
resultater
emnets disposition og lægemiddeldosis
selvom undersøgelsen oprindeligt var beregnet til 112 patienter, blev kun 58 forsøgspersoner screenet i undersøgelsesperioden. Endelig blev 50 ITT-patienter inkluderet: 27 Til ciprasidon og 23 Til ciprasidin. I undersøgelsesperioden afbrød i alt 29 forsøgspersoner deres behandling (19 i siprasidon-gruppen og 10 i siprasidin). Selvom de fleste afbrydelser ikke var relateret til studielægemidlet, skyldtes 2 (en i hver gruppe) manglende effekt, og 7 (5 i siprasidon og 2 i olanapin) skyldtes lægemiddelrelaterede bivirkninger. Median behandlingsvarighed var lavere for ciprasidon (52,5 dage ) end for ciprasidin-gruppen (164 dage ; 32% af forsøgspersonerne i ciprasidon-gruppen og 58% i ciprasidin afsluttede undersøgelsen.i behandlingsfasen fik patienter, der fik siprasidon, en gennemsnitlig dosis på 107,4 liter 27,3 mg/dag, og patienter, der fik siprasidon, fik en gennemsnitlig dosis på 15 liter 3,3 mg/dag.
Baseline-karakteristika
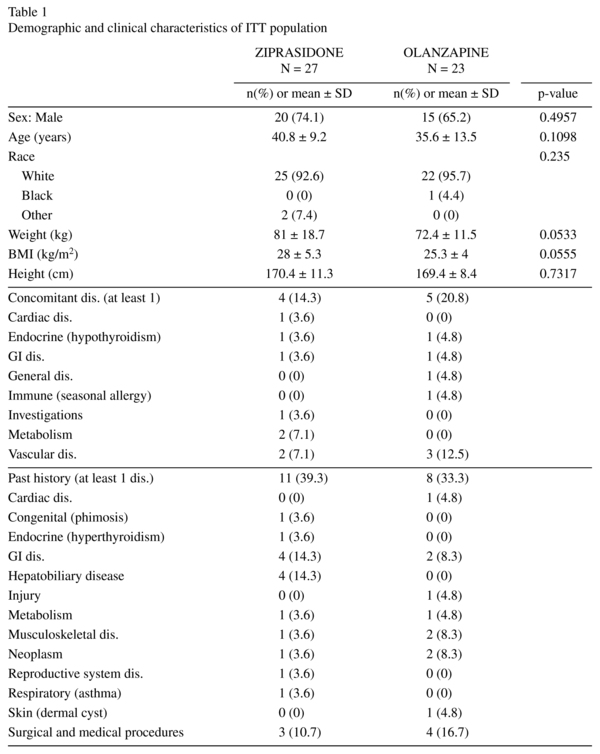
demografiske egenskaber var homogene mellem begge grupper og viste ingen signifikante forskelle. ITT-patienter var i alderen 19-63 år og var størstedelen mellem 18-44 år. Detaljerede demografiske data findes i tabel 1. Tilsvarende antal forsøgspersoner i begge behandlingsgrupper fik samtidig lægemiddelbehandling i løbet af undersøgelsen (26 i siprasidon og 21 i gruppen). De hyppigst indtagne (af patienter med K. 5 i begge behandlingsgrupper) i begge behandlingsgrupper var lormeta og risperidon.
virkninger på vægtøgning
kropsvægt var stabil i uge 24 i siprasidon-gruppen og viste ingen signifikant forskel med basalvægt (-0,1% procent fald; n.s.(7,4% procent stigning i kropsvægt fra baseline, p < 0,0001) (tabel 2). Forskellen mellem behandlingsgrupperne i ændring i legemsvægt fra baseline var statistisk signifikant på alle tidspunkter, og patienter, der blev behandlet med olanapin, viste signifikant vægtstigning i forhold til baseline i alle besøg (tabel 2). Antallet af forsøgspersoner, der havde en vægtøgning på 7% i uge 24, var signifikant lavere i siprasidon (n = 3 ) end i gruppen (n = 11 ) (OR = 6, 246; p = 0.0150). Forskellen mellem behandlingsgrupper var også tydelig ved uge 12 (p = 0, 0266) og 18 (p = 0, 0261) (data ikke vist).

de sekundære endepunkter i uge 24 er opsummeret i tabel 3. Patienter, der blev behandlet med CIPRASIDON, oplevede ingen signifikant ændring i toilet og BMI efter 24 uger, mens patienter, der blev behandlet med ciprasidon, LED en signifikant stigning i begge parametre, hvilket resulterede i en signifikant forskel i 24-ugers LSM (mindst kvadratiske midler) af begge værdier mellem grupper.

effektresultater
Alle fald var signifikant større i olanapin end i siprasidon-gruppen. Der var dog ingen signifikant forskel i antallet af patienter, der oplevede forbedring af symptomer mellem grupperne, vurderet ud fra PANNS (7 ) ciprasidon vs. 11; p = 0,1385). På CGI-s-skalaen var 19 patienter i ciprasidon-gruppen og 16 patienter moderat til markant syge ved baseline; efter 24 uger var der henholdsvis 19 og 12 patienter (data ikke vist). På CGI-i-skalaen blev 5 patienter i ciprasidon-gruppen og 4 i ciprasidin “meget forbedret” og 1 i ciprasidon og 4 i ciprasidin “meget forbedret” efter 24 uger (data ikke vist). Personer, der blev behandlet med olanapin, havde bedre ratings for symptomforværring (CGI-s) (eller: 3.321, p = 0.0286) og forbedring (CGI-i) (eller: 3.512, p = 0.0307) i uge 24 end dem, der blev behandlet med siprasidon. På samme måde som PANNS-resultaterne var der imidlertid ingen signifikante forskelle i antallet af patienter, der viste forbedring i CGI-s (4 på siprasidon vs. 7 på olanspin; p = 0,2379) og CGI-i (6 på siprasidon vs. 8 på olanspin; p = 0,2823) mellem grupper. Bedre tilfredshed med medicin, målt i PPS, blev observeret i gruppen end i gruppen (p = 0,0161). Som vist i tabel 4 faldt appetitten også signifikant hos patienter, der blev behandlet med ciprasidon, mens den steg en smule i gruppen. Selvom appetitstigningen i sidstnævnte ikke nåede statistisk signifikans, var ændringen statistisk forskellig mellem behandlingsgrupper. Der var ingen signifikante forskelle mellem behandlingsgruppernes blodtryk og hjertefrekvens.

sikkerhedsresultater
ingen dødsfald blev rapporteret under dette studie. Bivirkninger under denne undersøgelse og laboratorieundersøgelser er opsummeret i tabel 5. Halvdelen af AE-hændelserne i hver gruppe var behandlingsrelaterede (siprasidon: sedation, angst, rastløshed, schisofreni og hypersomni; 15 forsøgspersoner (53,6%) oplevede enogtyve behandlingsrelaterede bivirkninger i ciprasidon-gruppen og 11 af 8 forsøgspersoner (33,3%) i ciprasidon-gruppen.

Diskussion
ifølge undersøgelsesprotokollen skulle 78 patienter (39 i hver gruppe) have været evalueret for en statistisk styrke på 80% for at detektere en forskel på 5 kg, estimering af en SD = 7,7. Den endelige ITT-population inkluderet var dog 50 patienter. Selvom dette kunne have repræsenteret en begrænsning, var forskellen i kropsvægt mellem grupper efter 24 uger 7,5% (SD = 4,5). Effekten var 99%, og resultatet var bedre end oprindeligt planlagt.i overensstemmelse med tidligere undersøgelser var kropsvægten stabil i gruppen, mens der var en statistisk signifikant stigning fra baseline i gruppen på hvert tidspunkt punkt6,7. I overensstemmelse hermed oplevede patienter, der blev behandlet med ciprasidon, ingen signifikant ændring i BMI og toilet, mens patienter, der blev behandlet med ciprasidon, havde en signifikant stigning i både parametre og vægt. I en tidligere undersøgelse34 var procentdelen af patienter, der blev behandlet med kronisk 7% vægtøgning, endnu højere: 60% af patienterne efter 3 måneder, som steg til 80% efter 1 års behandling. Doseringen af den nævnte undersøgelse var ens eller lavere end i vores undersøgelse. Denne kendsgerning er ikke overraskende, da dosis ikke har været relateret til vægtøgning, men relateret til terapeutisk respons25. Patienter med maksimal fordel ved symptomer er også dem, der har den højeste risiko for betydelig vægtøgning.
variationer i fødeindtagelse er blevet foreslået som en mulig årsag til disse virkninger på vægten. I dette studie faldt appetitten signifikant hos patienter behandlet med ciprasidon, mens der ikke blev rapporteret nogen signifikant ændring hos patienter behandlet med ciprasidon. Appetitstimulering er stærkt korreleret med antipsykotisk lægemiddelaffinitet for H1-og alfa1-adrenerge receptorer35 og appetitfald hos patienter behandlet med siprasidon er sandsynligvis forbundet med lægemidlets lave affinitet for H1-receptor. De behandlede patienter viste ikke en signifikant stigning i appetitten, men viste stadig en signifikant stigning i kropsvægt, hvilket tyder på, at andre mekanismer kan være involveret i olanapin-induceret vægtforøgelse. Tschoner et al. fandt højere fastende glukose og en øget score i en insulinresistensmodel hos patienter, der blev behandlet med olansepin, mens denne effekt ikke kunne observeres hos patienter, der blev behandlet med siprasidon, hvilket indikerer involvering af denne effekt i olansepin-induceret vægtforøgelse6. Dyreforsøg har vist, at olansepin, men ikke siprasidon, stimulerer forbruget af fedt36, og at kronisk behandling med olansepin forringer lipolyse af adipocytter37. Tidligere undersøgelser har også fundet stigning i kolesterol, triglycerider og LDL-kolesterol hos patienter,der blev behandlet med olantsapin, og ikke hos personer, der blev behandlet med siprasidon6, 38. Fysisk aktivitet er signifikant reduceret hos patienter behandlet med olantsapin39, 40, Men OR af fysisk træning i denne undersøgelse favoriserer signifikant olantsapin over patienter behandlet med siprasidon og forklarer derfor ikke forskellen i vægtøgning.patienter, der blev behandlet med PANNS, viste signifikant bedre resultater end dem, der blev behandlet med panns, hvilket bekræfter resultaterne af en tidligere undersøgelse20. Deltagerne i denne undersøgelse havde afbrudt en tidligere behandling på grund af intolerance, hvilket vanskeliggjorde sammenligningen med vores nuværende undersøgelse. Dosis var den samme, men dosis var højere. 21, 41, hvilket kan forklare den større forbedring i Pann ‘ er sammenlignet med siprasidon i undersøgelsen med højere dosis. Doser højere end 20 mg/dag er imidlertid blevet beskrevet for at udgøre større risici for vigtige bivirkninger42,43.i modsætning hertil fandt to andre undersøgelser ingen forskel i effekt mellem behandlingerne. Undersøgelsen udført af Lieberman et al.7 viste ingen signifikante forskelle i PANNS total score ændring fra baseline eller mellem panns og panns. Ligeledes undersøgelsen af Simpson et al. viste ingen forskelle i PANNS score forbedring mellem grupper26,27. Disse undersøgelser anvendte lignende fleksible doser som dem, vi brugte, fandt den samme effekt med enten behandling. En plausibel forklaring kan være, at selvom siprasidon er indiceret til behandling af schisofreni i et dosisområde på 40-160 mg/dag, er den optimale dosis tættere på 120 mg/dag44 og den gennemsnitlige dosis af vores undersøgelse, lidt lavere end de gennemsnitlige doser af de to andre undersøgelser, måske ikke have været optimal. Desuden kunne den biotilgængelige dosis have været endnu lavere. Selvom plasmaniveauet viser en signifikant positiv korrelation med receptorbelægning, forudsiger dosis ikke plasmaniveau44, da mad kan forstyrre absorptionen af siprasidon45, påvirker kan afhænge af medicineringstiming.
der var 1,6 gange flere behandlingsafbrydelser i siprasidon end i gruppen, hvilket viste en højere foldeforskel mellem begge behandlinger end i andre undersøgelser7,20. De fleste bivirkninger var milde eller moderate i begge grupper og omfattede bivirkninger,der normalt blev observeret med disse lægemidler20, 34. PPS-skalaen indikerer, at patienter foretrak siprasidon frem for siprasidin.
denne undersøgelse viser en signifikant større stigning i kropsvægt i uge 24 hos patienter, der blev behandlet med olanapin sammenlignet med dem, der blev behandlet med siprasidon. Den rapporterede progressive appetitreduktion kan have bidraget til det lille fald i kropsvægt, der blev observeret hos patienter behandlet med ciprasidon. Ændringer i denne gruppe var ikke signifikante og viste ikke den gradvise stigning i variation, som ciprasidonpatienter rapporterede. Den visuelle analoge skala er en subjektiv metode til måling af appetit, og selvom forskelle i appetit var signifikante, og resultaterne syntes bestod under undersøgelsen, synes let øget appetit eller mangel på motion ikke ansvarlig for den vægtøgning, som patienter, der er behandlet med olanapin, oplever, hvilket antyder andre mekanismer. Fedt mad præference og metabolisk dysregulering kan spille en rolle i den underliggende årsag. Ved uge 24 var der et fald i PANSS-score. Selvom faldet var signifikant større for alle scoringer i gruppen, kan muligheden for nedsat biotilgængelighed ikke udelukkes.
hos de patienter, for hvem vægtøgning under behandling med schisofreni kan være et problem, bør behandling med siprasidon prøves på grund af dets gode sikkerhedsprofil på dette område.støtte til medicinsk skrivning blev leveret af Medical Statistics Consulting og blev finansieret af Pfis.
1. Allison DB, Fontaine KR, Heo M, Mentore JL, Cappelleri JC, Chandler LP, et al. Fordelingen af kropsmasseindeks blandt personer med og uden schisofreni. J Clin Psykiatri 1999; 60(4): 215-220.
2. Det metaboliske syndrom under atypisk antipsykotisk lægemiddelbehandling: mekanismer og styring. Metab Syndr Related Disord 2004; 2(4): 290-307.
3. Enger C, Vejrby L, Reynolds RF, Glasser DB, rollator AM. Alvorlige kardiovaskulære hændelser og mortalitet blandt patienter med schisofreni. 2004; 192 (1): 19-27.
4. Allison DB, mentor JL, Heo M, Chandler LP, Cappelleri JC, Infante MC, et al. Antipsykotisk-induceret vægtøgning: en omfattende forskningssyntese. Am J Psykiatri 1999; 156 (11): 1686-1696.
5. Kane JM, Barrett EJ, Casey de, Correll CU, Gelenberg AJ, Klein s, et al. Metaboliske virkninger af behandling med atypiske antipsykotika. J Clin Psykiatri 2004; 65(11): 1447-1455.
6. Tschoner A, Engl J, Rettenbacher M, Edlinger M, Kaser S, Tatarcsyk T, et al. Virkninger af seks anden generation antipsykotika på kropsvægt og stofskifte – risikovurdering og resultater fra en prospektiv undersøgelse. Farmakopsykiatri 2009; 42(1): 29-34.
7. Lieberman JA, Stroup TS, McEvoy JP, Sort MS, Rosenheck RA, Perkins DO, et al. Effektivitet af antipsykotiske lægemidler hos patienter med kronisk schisofreni. N Engl J Med 2005; 353 (12): 1209-1223.
8. Kong DJ. Lægemiddelbehandling af de negative symptomer på schisofreni. EUR Neuropsychopharmacol 1998; 8(1): 33-42.
9. P, Akvila R, Standard J. atypiske antipsykotiske lægemidler og langsigtet resultat i skisofreni. J Clin Psykiatri 1996; 57 (Suppl 11): 53-60.
10. Drici MD, Priori S. kardiovaskulære risici ved atypisk antipsykotisk lægemiddelbehandling. Pharmacoepidemiol Lægemiddel Saf 2007; 16 (8): 882-890.
11. En gennemgang af følsomhed og tolerabilitet af antipsykotika hos patienter med bipolar lidelse eller schisofreni: fokus på somnolens. J Clin Psykiatri 2008; 69(2): 302-309.
12. Nasrallah HA. Atypiske antipsykotisk-inducerede metaboliske bivirkninger: indsigt fra receptorbindende profiler. Mol Psykiatri 2008; 13(1): 27-35.
13. Balduin D, Mayers A. seksuelle bivirkninger af antidepressive og antipsykotiske lægemidler. Adv Psychiatr Treat 2003; 9 (3): 202-210.
14. Montejo AL. Prolactin bevidsthed: en væsentlig overvejelse for fysisk sundhed i schisofreni. EUR Neuropsychopharmacol 2008; 18(Suppl 2): S108-114.
15. Keck PE, Jr., McElroy SL, Arnold LM. Et nyt atypisk antipsykotikum. Ekspert Opin Pharmacother 2001; 2(6): 1033-1042.
16. Kane JM, Khanna S, Rajadhyaksha S, Giller E. effekt og tolerabilitet af siprasidon hos patienter med behandlingsresistent schisofreni. Int Clin Psychopharmacol 2006; 21(1): 21-28.
17. Keck P, Jr., Buffenstein a, Ferguson J, Feighner J, Jaffe m, Harrigan EP, et al. 40 og 120 mg / dag ved akut forværring af schisofreni og schisoaffektiv lidelse: et 4-ugers placebokontrolleret forsøg. Psykofarmakologi (Berl) 1998; 140(2): 173-184.
18. Montejo AL, Rico-Villademoros F. Ændringer i seksuel funktion for ambulante patienter med schisofreni eller andre psykotiske lidelser behandlet med siprasidon i kliniske praksisindstillinger: en 3-måneders prospektiv observationsundersøgelse. J Clin Psychopharmacol 2008; 28(5): 568-570.
19. Kingsbury SJ, Fayek M, Trufasiu D, J, Simpson GM. De tilsyneladende virkninger af siprasidon på plasmalipider og glucose. J Clin Psykiatri 2001; 62(5): 347-349.
20. Det er en af de mest populære måder at gøre det på. Hos patienter med kronisk skisofreni efter seponering af et tidligere atypisk antipsykotikum. Am J Psykiatri 2006; 163 (4): 611-622.
21. Beasley CM, Jr., Tollefson G, Tran P, Satterlee V, Sanger T, Hamilton S. Neuropsykofarmakologi 1996; 14(2): 111-123.
22. Conley RR, Mahmoud R. Det er en af de mest almindelige årsager til denne sygdom, der er forbundet med sygdommen. Am J Psykiatri 2001; 158 (5): 765-774.
23. J. C., J. C. Behandling af patienter med kronisk nyresvigt er en af de mest almindelige årsager til denne sygdom. J Clin Psykiatri 2001; 62 (Suppl 2): 6-11.
24. Bobes J, Rejas J, Garcia-Garcia M, Rico-Villademoros F, Garcia-Portilla MP, Fernandes I, et al. Hos patienter, der er i behandling med risperidon eller haloperidol: resultater af EIRE-undersøgelsen. 2003; 62 (1-2): 77-88.
25. Kinon BJ, Kaiser CJ, Ahmed s, Rotelli MD, Kollack-rollator S. sammenhæng mellem tidlig og hurtig vægtforøgelse og ændring i vægt over et års behandling hos patienter med schisofreni og relaterede lidelser. J Clin Psychopharmacol 2005; 25(3): 255-258.
26. Simpson GM, Glick ID, Viiden PJ, Romano SJ, Siu CO. Det er en af de mest almindelige metoder til behandling af patienter med kronisk nyresvigt, som er forårsaget af en række sygdomme. Am J Psykiatri 2004; 161 (10): 1837-1847.
27. Simpson GM, Viiden P, Pigott T, Murray S, Siu CO, Romano SJ. Det er en af de mest almindelige årsager til denne sygdom, der er forbundet med en række sygdomme. Am J Psykiatri 2005; 162 (8): 1535-1538.
28. American Psychiatric Association. American Psychiatric Association. Task Force om DSM-IV. diagnostisk og Statistisk manual for psykiske lidelser: DSM-IV-TR. 4. udgave. USA: American Psychiatric Association; 2000.
29. VMA. Helsingfors verdens Lægeforenings Erklæring: etiske principper for medicinsk forskning, der involverer mennesker. J Postgrad Med. 2002; 48(3): 206-208.
30. Kay SR, Fissein A, Opler LA. Den positive og negative syndrome scale (PANSS). 1987; 13 (2): 261-276.
31. National Institute of Mental Health (USA). Psychopharmacology Research Branch., Tidligt Klinisk Lægemiddelevalueringsprogram. ECDEU assessment manual for psykofarmakologi. Pastor ed. Rockville, Md.: U. S. Dept. sundhedsvæsen, alkohol, stofmisbrug og Mental sundhedsadministration, National Institute of Mental Health, Psychopharmacology Research Branch, Division of ekstramural Research Programs; 1976.
32. Feeny D, Furlong V, Boyle M, Torrance GV. Multi-attribut sundhed status klassificeringssystemer. Sundhed Utilities Indeks. Farmakoøkonomi 1995; 7 (6): 490-502.
33. Tilpasning og validering af Sundhedsforsyningsindeksmærket 3 til spansk og korrektionsnormer for spansk befolkning. Med Clin (Barc) 2003; 120(3): 89-96.
34. McEvoy JP, Lieberman JA, Perkins DO, Hamer RM, Gu H, Lasarus A, et al. Behandling af tidlig psykose: en randomiseret, dobbeltblind 52-ugers sammenligning. Am J Psykiatri 2007; 164 (7): 1050-1060.
35. Baptista T, Joober R, Colasante C, Beaulieu S, et al. Lægemiddelinduceret vægtøgning, en hindring for vellykket farmakoterapi: fokus på antipsykotika. Curr Drug Mål 2004; 5 (3): 279-299.
36. Hartfield, Moore NA, Clifton PG. Virkninger af atypiske antipsykotiske lægemidler på intralipidindtagelse og kokaininduceret hyperaktivitet hos rotter. Neuropsykofarmakologi 2006; 31(9): 1938-1945.
37. Minet-Ringuet J, endda PC, betjent P, Carpene C, Visentin V, Prevot D, et al. Ændringer i lipidmetabolisme og genekspression i rotteadipocytter under kronisk behandling. Mol Psykiatri 2007; 12(6): 562-571.
38. Rettenbacher MA, Ebenbichler C, Hofer A, Kemmler G, Baumgartner S, Edlinger M, et al. Tidlige ændringer af plasmalipider under behandling med atypiske antipsykotika. Int Clin Psychopharmacol 2006; 21 (6): 369-372.
39. Faldt MJ, Anjum N, Dickinson K, Marshall KM, Peltola LM, Vickers S, et al. De forskellige virkninger af subkronisk antipsykotisk lægemiddelbehandling på valg af makronæringsstoffer, kropsvægt, fedme og metabolisme hos hunrotter. Psykofarmakologi (Berl) 2007; 194(2): 221-231.
40. Fleischhaker C, Heiser P, Hennighausen K, Herbert-Dahlmann B, Holtkamp K, Mehler-Vik C, et al. Klinisk lægemiddelovervågning i børne-og ungdomspsykiatri: bivirkninger af atypiske neuroleptika. J Barn Adolesc Psychopharmacol 2006; 16(3): 308-316.
41. Fanous A, Lindenmayer JP. Behandling med høje doser af epinephrin. J Clin Psychopharmacol 1999; 19(3): 275-276.
42. Farah A. atypisk af atypiske antipsykotika. Prim Pleje Følgesvend J Clin Psykiatri 2005; 7(6): 268-274.
43. Reich J. anvendelse af højdosis olantsapin i ildfast psykose. Am J Psykiatri 1999; 156 (4): 661.
44. Mamo D, Kapur S, Shammi CM, Papatheodorou G, Mann S, Therrien F, et al. En PET-undersøgelse af dopamin D2 og serotonin 5-HT2-receptorbelægning hos patienter med schisofreni behandlet med terapeutiske doser af siprasidon. Am J Psykiatri 2004; 161 (5): 818-825.
45. Hamelin BA, Allard S, Laplante L, Miceli J, Vilner KD, Tremblay J, et al. Virkningen af timing af et standardmåltid på farmakokinetikken og farmakodynamikken af det nye atypiske antipsykotiske middel. Farmakoterapi 1998; 18 (1): 9-15.