Generic Name: fluocinonid
Léková Forma: Mast
Lékařsky přezkoumány Drugs.com. Naposledy aktualizován dne 22. Prosince 2020.
- Přehled
- Nežádoucí Účinky
- Dávkování
- Odborné
- Interakce
- Další
Rx Pouze
Lidex značka byla ukončena v USA, Pokud generické verze tohoto produktu byly schváleny FDA, tam může být generické ekvivalenty k dispozici.
Lidex popis
Lidex® (fluocinonid) masť 0,05% je určena k topickému podání. Aktivní složkou je kortikosteroid fluocinonid, což je 21-acetát ester fluocinolon acetonid a má chemický název těho-1,4-dien-3,20-dion,21-(acetyloxy)-6,9-difluoro-11-hydroxy-16,17–,(6α,11beta,16α)-. Má následující chemickou strukturu:
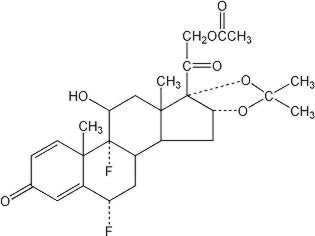
Lidex masť obsahuje fluocinonid 0.5 mg/g ve speciálně formulovány mast skládající se z glycerol-monostearát, bílá vazelína, propylen karbonát, propylenglykol a bílý vosk. Poskytuje okluzivní a zvláčňující účinky žádoucí v masti.
v této formulaci je účinná látka zcela v roztoku.
Lidex-Klinická farmakologie
lokální kortikosteroidy mají protizánětlivé, antipruritické a vazokonstrikční účinky.
mechanismus protizánětlivé aktivity topických kortikosteroidů je nejasný. K porovnání a predikci účinnosti a/nebo klinické účinnosti lokálních kortikosteroidů se používají různé laboratorní metody, včetně vazokonstrikčních testů. Existují důkazy, které naznačují, že existuje rozpoznatelná korelace mezi vazokonstrikční účinností a terapeutickou účinností u člověka.
Farmakokinetika
rozsah perkutánní absorpce lokálních kortikosteroidů je dána mnoha faktorech, včetně vozidla, integrity epidermální bariéry a použití okluzivních obvazů.
lokální kortikosteroidy mohou být absorbovány z normální neporušené kůže. Zánět a / nebo jiné chorobné procesy v kůži zvyšují perkutánní absorpci. Okluzivní obvazy podstatně zvyšují perkutánní absorpci topických kortikosteroidů. Okluzivní obvazy tak mohou být cenným terapeutickým doplňkem pro léčbu rezistentních dermatóz(viz dávkování a podávání).
po vstřebání kůží jsou lokální kortikosteroidy léčeny farmakokinetickými cestami podobnými systémově podávaným kortikosteroidům. Kortikosteroidy jsou vázány na plazmatické proteiny v různé míře. Kortikosteroidy se metabolizují primárně v játrech a poté se vylučují ledvinami. Některé topické kortikosteroidy a jejich metabolity se také vylučují do žluči.
Indikace a Využití pro Lidex
Lidex Mast je indikován pro zmírnění zánětlivých a svědivých projevů kortikosteroidy-citlivé dermatózy.
kontraindikace
topické kortikosteroidy jsou kontraindikovány u pacientů s anamnézou přecitlivělosti na kteroukoli složku přípravku.
bezpečnostní Opatření
Obecné
Systémová absorpce lokálních kortikosteroidů má za následek reverzibilní hypotalamus-hypofýza-nadledviny (HPA) osy, potlačení, projevy Cushingův syndrom, hyperglykémie a glykosurie u některých pacientů.
podmínky, které zvyšují systémovou absorpci, zahrnují aplikaci silnějších steroidů, použití na velkých plochách, dlouhodobé užívání a přidání okluzivních obvazů.
Proto, pacienti, kteří dostávají velkou dávku silné lokální steroidy aplikovány na velké plochy nebo pod okluzivní obvaz by mělo být hodnoceno pravidelně pro důkazy o HPA ose potlačení pomocí močový volný kortizol a ACTH stimulační testy. Pokud je zaznamenáno potlačení osy HPA, měl by být proveden pokus o stažení léku, snížení frekvence aplikace nebo nahrazení méně účinného steroidu.
obnovení funkce osy hPa je obecně rychlé a úplné po přerušení léčby. Zřídka se mohou objevit příznaky a příznaky stažení steroidů, které vyžadují doplňkové systémové kortikosteroidy.
děti mohou absorbovat proporcionálně větší množství lokálních kortikosteroidů, a proto jsou náchylnější k systémové toxicitě (viz opatření-pediatrické použití). Pokud dojde k rozvoji podráždění, je třeba léčbu lokálními kortikosteroidy přerušit a zahájit vhodnou léčbu.
stejně jako u jiných lokálních kortikosteroidních přípravků může dlouhodobé užívání vyvolat atrofii kůže a podkožních tkání. Při použití na intertriginózních nebo flexorových oblastech nebo na obličeji se to může objevit i při krátkodobém použití.
v případě dermatologických infekcí by mělo být zahájeno použití vhodného antifungálního nebo antibakteriálního činidla. Pokud se příznivá odpověď neobjeví okamžitě, kortikosteroid by měl být vysazen, dokud nebude infekce dostatečně kontrolována.
Informace Pro Pacienta
Pacienti používají lokální kortikosteroidy by měly zobrazit následující informace a instrukce:
- Tento lék se používá podle pokynů lékaře. Je určen pouze pro vnější použití. Zabraňte kontaktu s očima.
- pacienti by měli být poučeni, aby tento lék nepoužívali pro jiné poruchy, než pro které byl předepsán.
- ošetřené oblasti kůže by měly být ovázanou nebo jinak zakryty nebo zabalené tak, aby být okluzivní, pokud podle pokynů lékaře.
- pacienti by měli hlásit jakékoli známky lokálních nežádoucích účinků, zejména pod okluzivním obvazem.
- Rodiče dětských pacientů by měla být nedoporučuje používat těsně přiléhající plenky nebo plastové kalhoty na dítě léčen v plenkové oblasti, jako jsou tyto oděvy mohou představovat okluzivní obvazy.
laboratorní testy
následující testy mohou být užitečné při hodnocení potlačení osy HPA:
Močový volný kortizol test
ACTH stimulační test,
Karcinogeneze, Mutageneze, Poškození Fertility
dlouhodobé studie na zvířatech nebyly provedeny pro vyhodnocení kancerogenního potenciálu nebo vliv na plodnost lokálních kortikosteroidů.
studie ke stanovení mutagenity s prednisolonem a hydrokortizonem odhalily negativní výsledky.
Kategorie těhotenství C
kortikosteroidy jsou obecně teratogenní u laboratorních zvířat, pokud jsou podávány systémově v relativně nízkých dávkách. Ukázalo se, že účinnější kortikosteroidy jsou teratogenní po dermální aplikaci u laboratorních zvířat. Neexistují adekvátní a dobře kontrolované studie teratogenních účinků lokálně aplikovaných kortikosteroidů u těhotných žen. Proto by se topické kortikosteroidy měly používat během těhotenství pouze tehdy, pokud potenciální přínos odůvodňuje potenciální riziko pro plod. Léky této třídy by neměly být používány rozsáhle u těhotných pacientů, ve velkém množství nebo po delší dobu.
kojící matky
není známo, zda by lokální podávání kortikosteroidů mohlo vést k dostatečné systémové absorpci k produkci detekovatelných množství v mateřském mléce. Systémově podávané kortikosteroidy se vylučují do mateřského mléka v množství, které pravděpodobně nebude mít škodlivý účinek na kojence. Při podávání topických kortikosteroidů ošetřující ženě je však třeba postupovat opatrně.
Použití v Pediatrii
Dětské pacienty může prokázat větší náchylnost k topické kortikosteroidy indukované hypothalmic-hypofýza-nadledviny (HPA) osy, potlačení a Cushingův syndrom než zralé pacientů, protože větší kožní plochy povrchu k tělesné hmotnosti poměr.u dětí užívajících topické kortikosteroidy byla hlášena suprese osy HPA, Cushingův syndrom a intrakraniální hypertenze. Projevy adrenální suprese u dětí zahrnují lineární retardaci růstu, zpožděný přírůstek hmotnosti, nízké hladiny kortizolu v plazmě a nepřítomnost odpovědi na stimulaci ACTH. Projevy intrakraniální hypertenze zahrnují vypouklé fontanely, bolesti hlavy a bilaterální papilém.
podávání topických kortikosteroidů dětem by mělo být omezeno na nejmenší množství slučitelné s účinným terapeutickým režimem. Chronická léčba kortikosteroidy může interferovat s růstem a vývojem dětí.
Nežádoucí Účinky
následující místní nežádoucí účinky jsou hlášeny zřídka s lokálními kortikosteroidy, ale může dojít častěji při použití okluzivní obvazy. Tyto reakce jsou uvedeny v přibližném sestupném pořadí výskytu:
| Burning | Perioral dermatitis |
| Itching | Allergic contact dermatitis |
| Irritation | Maceration of the skin |
| Dryness | Secondary infection |
| Folliculitis | Skin atrophy |
| Hypertrichosis | Striae |
| Acneiform eruptions | Miliaria |
| Hypopigmentation |
Overdosage
Topically applied corticosteroids can be absorbed in sufficient amounts to produce systemic effects (see PRECAUTIONS).
Lidex Dávkování a způsob Podání
Lidex Mast se obvykle aplikuje na postižené oblasti jako tenký film dva až čtyři krát denně v závislosti na závažnosti stavu.
okluzivní obvazy mohou být použity k léčbě psoriázy nebo vzpurných stavů.
Pokud se infekce vyvine, je třeba podávání okluzivních obvazů přerušit a zahájit vhodnou antimikrobiální léčbu.
jak se Lidex dodává
Lidex® (fluocinonid) mast 0.05% je dodáván v
15 g Trubka –NDC 99207-514-13
30 g Trubka –NDC 99207-514-14
60 g Trubka –NDC 99207-514-17
120 g Trubka –NDC 99207-514-22
Skladujte při pokojové teplotě. Vyhněte se teplotě nad 30°C (86°F).
US Patent Č. 4,017,615
Vyrobeno pro:
MEDICEJSKÝM, Dermatologie Společnosti®
Scottsdale, AZ 85258,
: Patheon, Inc.
Mississauga, Ontario
Canada L5N 7K9
IN-5070/S
| Lidex fluocinonide ointment |
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
|
|||||||||||||||||||
Labeler – MEDICIS
Frequently asked questions
- Is it used for hair loss?
- What is a substitute for fluocinonide cream?
- Is fluocinonide an antifungal cream?
- How long should you use fluocinonide for?
- What is fluocinonide cream good for?
- lze fluocinonid použít k léčbě vyrážky jedovatého břečťanu?
- je to steroid?
- je to antibiotikum?
Více o Lidex (fluocinonid aktuální)
- Nežádoucí Účinky
- Během Těhotenství nebo Kojení
- Dávkování Informací
- lékové Interakce
- 8 Recenze
- Generic Dostupnost
- třídy Drog: lokální steroidy
Spotřebitelské zdroje
- Pokročilé Čtení
- Lidex Mírné (Pokročilé Čtení)
- Lidex Pravidelné (Pokročilé Čtení)
Odborné zdroje
- Předepisování Informace
- Lidex Aktuální Řešení (FDA)
- Lidex Gel (FDA)
Jiných značek Vanos, Lidex-E
Související léčba vodítka
- Atopické Dermatitidy
- Ekzém
- Dermatitida
- Lupénka
Medical Disclaimer